서 론
해양 생태계는 지구상에 존재하는 생물계의 95%를 차지하고 있으며 육상생물에 없는 특유의 대사과정과 독특한 환경으로 인하여 다양한 신규 생리활성물질의 탐색 가능성을 가지고 있다(Mehbub et al., 2014). 또한 육상생물은 이미 많은 연구가 진행되었지만, 해양생물은 고대로부터 내려오는 해양생물을 이용한 민간요법의 부재, 해양생물수집의 어려움 등의 이유로 제한된 연구만이 이루어져 앞으로 해양생물을 이용한 미지의 천연 물질의 개발에 대한 기대가 높이 평가되고 있으며, 우리나라는 삼면이 바다로 둘러싸인 해양 국가이기 때문에 확보할 수 있는 다양한 해양생물자원을 갖고 있고, 이를 이용한 새로운 기능성 식품이나 약효 식품의 개발은 많은 잠재력을 가진 분야로 주목받고 있다(Mehbub et al., 2014; Ulagesan et al., 2022).
굴은 연체동물로 Eutaxodonta 목(order)의 굴(Ostreidae)과에 속하는 패류로서 세계적으로 100여 종 이상 알려져 있고, 우리나라 연안에는 참굴(Crassostrea gigas), 바윗굴(Crassostrea nippona), 벗굴(Ostrea denselamellosa) 등이 있으며, 이중 우리나라에서 산업적으로 생산되고 있는 것은 참굴이다(Choi et al., 2012; Negara et al., 2022). 참굴은 둥근 형에서부터 가늘고 긴 형에 이르기까지 형태가 일정하지 않으나, 일반적으로 각고가 10 cm, 각장이 7 cm 정도이다. 동의보감에서는 굴은 숙취 시 발생하는 갈증의 해소에 좋다고 명시되어 있으며, 오늘날에 이르러 굴의 다양한 영양적 가치로 주로 단백질과 탄수화물로 구성되어 있으며, 그 중에서도 타우린과 글리코겐의 함량이 높은 것으로 알려져 있다(Ulagesan et al., 2022).
최근 유산균을 굴에 접종하여 발효한 후 유용 물질을 추출한 발효굴추출물(fermented oyster extract)이 뼈의 형성과 키 성장, 그리고 운동수행능력의 개선 효과가 있다는 것이 보고되었다(Kim et al., 2019; Lee et al., 2020; Molagoda et al., 2020; Reid et al., 2020; Jeong et al., 2021). 또한 굴 단백질을 가수분해하여 높은 생리활성을 가지는 굴 단백질 가수분해산물이나 펩타이드 관련 연구가 보고되고 있으며 항산화, 항염, 항암, 면역증강제, 항균, 항진균, 미백, 항주름 효과 등 다양한 생물학적 활성을 가지며 안정성이 높아 최근에 기능성 소재로 많은 주목을 받고 있다(Liu et al., 2008; Cheong et al., 2013; Kang et al., 2013; Hao et al., 2021; Ulagesan et al., 2022).
이에 본 연구에서는 다양한 효능을 가진 굴을 이용하여 굴 발효배지를 제조하고, 사천 지역 특산물로부터 유산균을 분리 및 동정하고 분리한 유산균을 굴 발효배지에 접종하고 배양을 통하여 굴 발효물을 제조하여 항산화 효과를 확인하였으며, 이중 항산화 효과가 가장 높은 굴 발효물의 사용하여 굴 추출물을 제조한 후 항염증과 항당뇨 효과의 생리활성 기능을 평가하였다. 본 연구를 통하여 사천 지역 특산물에서 분리한 유산균의 산업적 활용 가능성을 확인함과 동시에 미생물 자원의 가치를 제고하고자 하였다.
재료 및 방법
국내 사천 지역 특산물 중에서 곤양면의 가나안목장에서 젖소의 원유, 초유 및 축사 토양, 사천읍의 성시영-가내양조에서 동아(박과의 덩굴성 식물)막걸리 발효원액과 제품, 곤명면의 새미골농원에서 십전대보 발효차, 저도(일명 딱섬)어촌계의 죽방렴에서 멸치 등으로부터 유산균 분리(Table 1)를 수행하였다. 이를 위해 각각의 샘플 1 g을 멸균된 0.85% 생리식염수에 첨가하여 vorterxer로 현탁하였다. 현탁한 샘플 1 mL를 사용하여 10–1~10–4배로 단계희석한 후, 일반 증식배지로 유산균 배양 전용 배지인 MRS agar (BD, USA) 배지를 제작하여 희석액을 도말하고 37°C에서 배양하였다. 배양 후 선택적으로 배지 상에 나타나는 균의 크기, 모양, 색깔 등 형태학적 모습을 관찰한 후 동일한 고체배지를 사용하여 추가적으로 single colony isolation을 수행하였다.
국내 사천 지역 특산물로부터 분리된 유산균의 분자생물학적 동정을 위해 MRS agar (BD, USA) 배지에서 분리 배양하였고, ㈜마크로젠에 16S rRNA 염기서열 분석을 의뢰하였다. 분석된 염기서열은 ㈜천랩의 EzBioCloud (https://www.ezbiocolud.net/)를 이용하여 근연 균주가 확인되었고, accession number 포함해 NCBI에 등록되었다(Table 2).
분리된 유산균들의 세포외 분해 효소 amylase, lipase, cellulase, protease 생산능 확인을 위하여 각각의 효소와 특이적으로 반응할 기질 성분이 포함된 고체 평판 선별배지를 사용하였다. 먼저 amylase 생산능은 0.2% soluble starch (BD, USA)를, lipase 생산능은 1% Tween 80 (BD, USA)을, cellulase 생산능은 1% CMC (BD, USA)를, protease 생산능은 20% skim milk (BD, USA)를 기질로 선택하여 MRS agar (BD, USA) 배지에 각각 첨가하여 제조하였으며 분리된 균주를 직접 접종하여 37°C에서 7일 배양한 후 투명환(clear zone)의 직경으로 조사하였다. 분리된 균주의 효소활성 분해능 평가는 배양 후 나타나는 접종균 주위의 투명환의 크기(+++: >7 mm, ++: >4~6 mm, +: 1~3 mm)로 나타내었다.
본 연구에 사용된 굴은 서포면 비토리의 낙지포항의 자연산 굴(대표적인 서포굴)로서, 같은 지역의 명승 횟집을 통해 얻었다. 발효에 용이한 굴분말을 제조하기 위해 원물의 굴 100 g을 121°C에서 15분간 멸균을 한 후 60°C에서 24 h 동안 건조시켰다. 건조 후 건조물의 온도를 떨어뜨리기 위해 쿨링시킨 후 분쇄기를 이용하여 건조물을 분말 형태로 파쇄한 후 밀봉된 상태로 실온에서 보관하며 굴 발효배지 제조 시 굴 성분으로 사용하였다.
굴 발효물 제조를 위해 1차 증류수에 제조한 굴 분말 2%, NaCl 3%, yeast extract 0.1%를 넣어 혼합하고 고압증기멸균기에서 121°C, 15분 동안 멸균하여 굴 발효배지를 제조하였다. 선별된 유산균을 MRS broth에서 전 배양하고, 굴 발효배지에 1%의 전배양액을 접종하여, 37°C에서 4일 동안 180 rpm으로 진탕 배양하여 배양상등액을 굴 발효물로 회수하였다.
그리고 굴 발효추출물의 제조를 위해 선별된 유산균을 MRS broth에서 전 배양하고, 1 L 굴 발효배지에 1%의 전배양액을 접종하여 항산화 효능이 가장 높았던 조건인 24시간, 37°C, 180 rpm으로 진탕 배양하였다. 1:1:1 비율로 Amberlite Resin XAD7HP, XAD4, XAD16N (Merck KGaA, Darmstadt, Germany)을 혼합하여 20g을 준비하고 3차 증류수로 세 번 세척 후 발효가 완료된 굴 발효 배양액에 첨가하였다. 2시간 동안 180 rpm으로 진탕하며 활성 성분을 Resin에 흡착시켰다. 흡착 후 면보로 거른 Resin을 Acetone 150 mL에 첨가하여 2시간 이상, 180 rpm으로 상온에서 활성물질을 탈착시켰다. Whatman NO. 2 필터지(Whatman International Ltd., Maidstone, UK)로 여과하여 Resin을 제거하고 여과된 Acetone은 Rotary Evaporator (Sunileyea, Seongnam, Korea)로 농축한 후, 질소가스를 이용한 Gas Evaporator (Miulab, Hangzhou, China)로 최종적으로 건조하여 분말 형태로 제조하였다.
각각의 분리된 유산균을 활용한 굴 발효물의 항산화 효과를 검증하기 위해 ABTS radical scavenging activity를 확인하였다. ABTS radical scavenging activity를 측정하기 위해 7 mM ABTS와 2.45 mM potassium persulfate를 1:1 비율로 섞어 혼합하고 16시간 동안 암실에 방치하여 ABTS 용액을 제조(OD value: 0.7±0.02)하였다. 96 well plate에 굴 발효물 20 μL와 상기 제조된 ABTS 용액 180 μL를 넣은 후 잘 섞어서 상온에서 2분 동안 반응시켜 흡광도 734 nm로 측정하여 분석하였다.
굴 발효추출물의 항염증 효과는 세포 내 ROS(활성 산소종) 소거 효능 시험법인 DCFH-DA (Tyagi et al., 2022) 시험방법으로 측정하였다. Raw264.7 세포를 96 well plate에 DMEM 배지(10% fetal bovine serum, 1% penicillin-streptomycin)를 넣어 5% CO2 인큐베이터에서 37°C, 24시간 배양하여 배양액을 제거하고, 5 μM CM-H2DCFDA가 포함된 DMEM 배지를 80 μL 넣어, 5% CO2, 37°C 인큐베이터에서 30분 동안 반응시키고, 제조된 굴 발효추출물 또는 양성대조군(ascorbic acid, α- tocopherol, dexamethasone, L-NIL)을 첨가하여 5% CO2, 37°C 인큐베이터에서 30분 동안 반응시킨다. 이후 LPS (Lipopolysaccharides from Escherichia coli O55:B5) 1 μg/mL를 첨가하고 5% CO2 인큐베 이터에서 37°C, 24시간 동안 반응시켜, 염증반응을 EnVision기기(EnVision XCite 2105 Multimode Plate Reader, PerkinElmer)를 이용하여 485/535 nm에서 DCF의 형광을 측정하여 분석하였다.
굴 발효추출물의 항당뇨 효과를 검증하기 위해 chromogenic 방법을 이용한 α-glucosidase 저해 활성을 측정하여 분석하였다(Zhang et al., 2020). 96 well plate에 2 g/L bovine serum albumin 및 0.2 g/L NaN3이 포함된 인산염 버퍼와 굴 발효추출물 또는 양성 대조군(acarbose)을 넣어 5분 동안 반응한다. 인산염버퍼와 굴발효추출물 또는 양성 대조군이 포함된 반응물에 p-nitrophenyl-α-D-glucopyranoside 기질 용액을 넣어 37°C에서 5분 동안 반응하고, Microplate reader (Epoch, BioTek, USA)를 이용하여 흡광도 405 nm에서 측정하여 α-glucosidase 저해 활성을 분석하였다.
결과 및 고찰
유산균은 예전부터 발효 식품에 활용되어 온 유용한 미생물로써 연구자들의 많은 주목을 받아왔으며 현재에도 유산균의 활용한 인체의 생리활성 기능을 향상시키기 위한 새로운 기능성 제품 개발에 지속적으로 활용되어 오고 있다(Choi, 2019; Wang et al., 2021). 이러한 연구 동향에 맞춰 새로운 유산균의 탐색을 위한 연구도 지속적으로 이루어지고 있는 것으로 사료된다.
본 연구에서도 국내 사천 지역 특산물로부터 유산균을 분리하고자 MRS agar 배지를 사용하여 균주 분리를 수행하였다. 그 결과 Table 1에서 나타낸 것처럼 가나안 농장 젖소의 원유와 초유, 그리고 축사 토양로부터 8 균주, 동아 막걸리 발효 원액과 제품으로부터 7 균주, 새미골 농원 십전대보 발효차로부터 2균주와 죽방렴 멸치로부터 1균주의 유산균이 분리되었으며, 본 실험을 통하여 유산균 미생물 총 18 균주를 순수 분리하였다.
다음으로 분리된 18 균주의 16S rRNA 염기서열을 바탕으로 NBLAST program과 EzBioCloud를 사용하여 미생물 동정을 실시한 결과 Lacticaseibacillus paracaseisubsp. tolerans, Latilactobacillus curvatus, Enterococcus lactis와 Lactiplantibacillus argentoratensis의 유산균 4 종류를 확인하였다. 가나안 농장 젖소 원유와 초유에서는 Lc. paracaseisubsp. tolerans 1 종류의 유산균만 분리되었으며 축사 토양에서는 Lat. curvatus와 E. lactis의 2 종류가 분리되었다. 동아 막걸리 발효 원액과 제품에서는 Lat. curvatus와 L. argentoratensis의 2 종류가 분리되었으며 나머지 분리원에서는 동일한 종의 유산균이 분리되었다. 이는 국내 사천 지역 특산품으로부터 유산균의 분리가 가능함을 나타냄과 동시에 추가적인 지역 특산품을 분리원으로 사용하면 다양한 유산균의 분리 가능성을 확인할 수 있을 것으로 사료된다.
단백질가수분해효소(protease)는 단백질을 펩타이드 단위로 가수분해하는 생물학적 촉매로 다양한 산업 분야에서 활용되고 있으며, 이중에서도 단백질분해효소를 세포 밖으로 분비하는 세균 유래의 단백질분해효소에 대한 연구 개발이 지속적으로 산업화를 목적으로 이루어지고 있다(Razzaq et al., 2019). 세균이 생산하는 세포 외로 분비되는 단백질가수분해효소의 경우 배지 내에 존재하는 거대 고분자인 단백질을 영양원으로 사용하기 위해 저분자성인 아미노산 단위로 분해한 후 세포 내로 흡수하기 위하여 분비하는 것으로 중요한 의미가 있다(song et al., 2023).
본 연구에서 분리한 유산균을 동물 또는 식물 유래 천연물의 고부가치화가 가능한 제품 개발을 위한 발효 균주로 사용하기 위해 세포외 분비 단백질가수분해효소 활성뿐만 아니라 탄수화물과 지방분해효소의 활성을 평가하였다. 세포외 가수분해 효소 생산 능력의 분석을 실시한 결과 Table 2에 나타낸 것처럼 분리된 18 균주 중 4 균주(22.2%)에서 protease 활성이 존재하는 것을 확인하였으며, CMCase, amylase와 lipase 활성은 나타나지 않았다. 단백질가수분해효소 활성을 나타낸 균주들 모두 동아 막걸리 발효 원액과 제품에서 분리한 균주로 Lat. curvatus 종으로 확인되었으며 같은 종의 Lat. curvatus 균주이지만 단백질가수분해효소 활성을 보이지 않는 균주들도 있었다. 이는 단백질분해효소 활성을 나타내는 Lat. curvatus 균주와 그렇지 못한 Lat. curvatus 균주의 전장 유전체 분석을 수행하고 이의 분석 결과를 활용한 비교유전체학 연구를 통해 같은 Lat. curvatus 종에서 단백질분해효소 생산 유전자의 특정이나 그와 관련된 유전자 발현 메커니즘 관련 연구가 가능할 것으로 사료된다. 또한 Lat. curvatus 균주의 경우 유럽식품안전청(European Food Safety Authority)에서 사용이 추천되는 프로바이오틱스 균주로 등록되어져 있으며, 육류의 발효 제품 생산 시 다양한 병원균의 생육을 저해할 수 있는 생물학적 보호제로서의 기능도 알려져 있다(Chen et al., 2020). 따라서 국내에서 분리된 Lat. curvatus 균주를 활용한 새로운 프로바이오틱스 균주로 활용이 가능할 것으로 사료됨과 동시에 국내 유산균 생물 자원의 다양성 확보 차원에서 큰 의미를 찾을 수 있을 것으로 예상된다.
최근 굴을 사용해 유산균 발효를 통해 만들어지는 굴 발효추출물에 대한 생리활성 향상 효과를 임상시험을 통해 검증한 연구 결과들이 지속적으로 발표되고 있다(Kim et al., 2019; Lee et al., 2020; Molagoda et al., 2020; Reid et al., 2020; Jeong et al., 2021). 이에 본 연구에서 분리된 유산균을 활용하고 균주 발효를 통해 생물 자원이 가지고 있는 생리활성을 향상시키기 위한 발효원으로 다양한 영양적 가치를 가지고 있으며, 타우린의 함량이 높아 심장 건강에 도움을 주며 피부 건강에도 도움을 줄 수 있는 것으로 알려져 있는 굴을 선택하고(Ulagesan et al., 2022), 유산균 배양을 위한 배지 제조를 위해 참굴을 배지 성분으로 사용하기 위해 분말화 하였다. 참굴 분말이 포함된 굴 발효배지에 protease 활성을 가지는 4 종의 유산균을 접종하고 배양하여 배양 일별로 배양 상등액을 회수하여 굴 발효산물을 획득하였다.
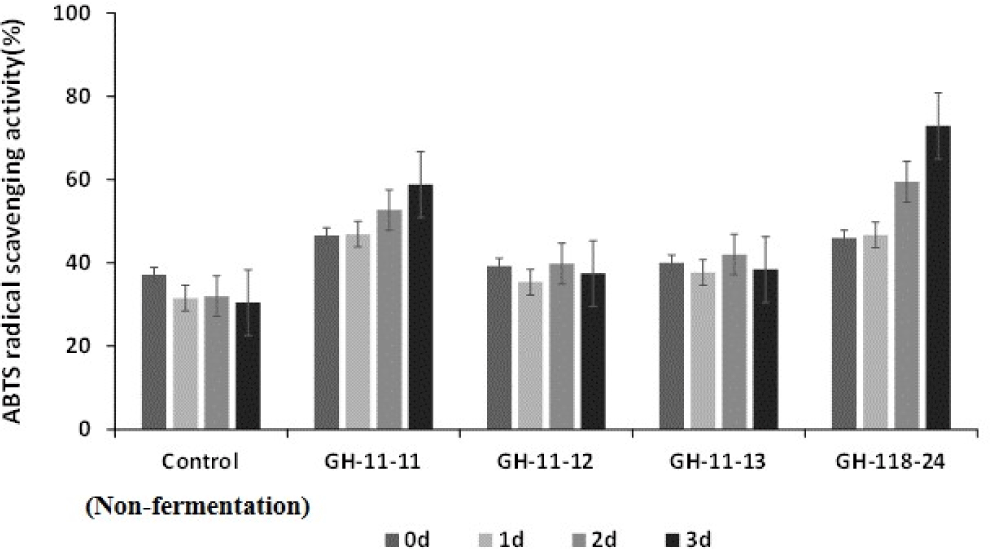
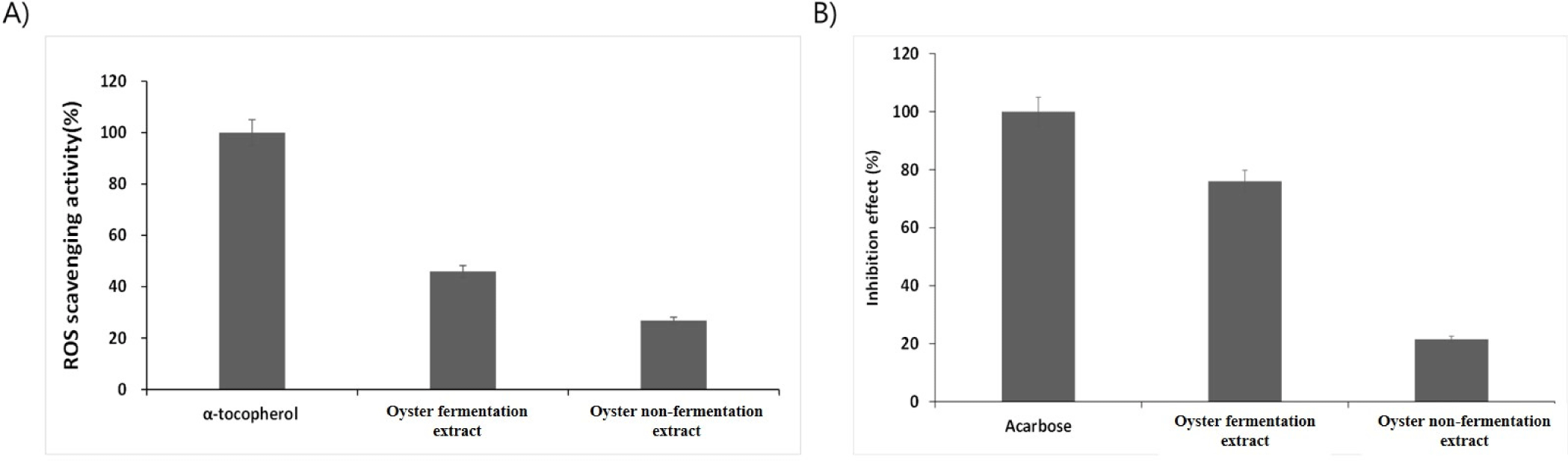
먼저 획득한 굴 발효산물의 생리활성을 확인하기 위해 항산화 활성을 ABTS radical scavenging activity를 측정하여 확인한 결과, Fig. 1에서 나타낸 것처럼 isolate number가 GH-11-11과 GH-118-24인 Lat. curvatus 균주를 사용한 경우에 분리 균주를 접종하지 않고 배양한 굴 발효산물에 비해 높은 항산화 활성을 나타내는 것을 확인하였고 특히 GH-118-24인 Lat. curvatus 균주를 사용한 경우에서 배양 3일째의 굴 발효산물에서는 139.2%의 항산화 활성이 증가하는 것을 확인하였다. 분리된 유산균의 발효에 따른 항산화 효과가 향상되는 결과를 바탕으로 추가적인 생리활성을 평가하기 위해 isolate number가 GH-118-24인 Lat. curvatus 균주를 발효 균주로 사용하고 배양 3일째의 굴 발효산물을 사용하여 굴 발효추출물을 제조하여 항염증과 항당뇨 활성을 평가하였다(Fig. 2). 먼저 항염증 활성을 평가하기 위해 Raw264.7 macrophage에 LPS로 염증 스트레스를 유도 후, DCFH-DA 시험방법으로 ROS 저해활성을 측정하였다. 실험 결과, GH-118-24를 접종한 참굴발효배양액의 추출물은 미생물 접종하지 않은 참굴비발효배양액의 추출물 대비 71.2%의 항염증 활성이 증가하는 것을 확인하였다. 특히, positive control인 강력한 천연 항산화제인 α-tocopherol (40 μg/mL)과 비교하여 참굴발효배양액은 발효 추출물임에도 45.9% (% of positive control)의 ROS 저해활성을 보여주었다. 굴에는 항염증 활성이 뛰어나다고 알려진 carotenoid류와 xanthophyll류 성분이 풍부한 것으로 알려져 있으며, 발효로 인해 항염증 compound의 활성 및 성분이 더욱 향상된 것으로 사료된다. 다음으로 동일한 시료를 사용하여 항당뇨 활성을 검증하기 위해 chromogenic 방법을 이용한 혈당 개선 및 당뇨 질환 개선을 위한 주요 타겟 효소인 α-glucosidase 저해 활성을 측정하였다. 실험 결과, 참굴발효배양액의 추출물은 비발효배양액의 추출물과 비교하여 253.8%의 α-glucosidase 저해 활성의 향상이 확인되었다. 특히, 제2형 당뇨병 환자의 혈당강하제로 처방되는 약물인 acarbose를 positive control로 비교한 결과, 약 80%의 활성을 나타내는 것을 확인하였다. 따라서 참굴발효배양액의 추출물은 장내 효소 활성을 효과적으로 저해하고, glucose 유리를 지연시켜 혈장 당 수지 감소에 기여할 수 있을 것으로 사료된다.
이는 Lactobacillus brevis 유산균 발효에 따른 참굴의 항산화와 항염증 활성에 미치는 영향 관련 연구결과(Kang et al., 2013)와 발효에 사용된 유산균의 종류는 다르지만 유사한 연구결과로 생각되며, 국내에서 분리된 새로운 유산균을 사용하여 제조한 굴 발효추출물의 식품이나 화장품 기능성 소재로서의 산업적 활용 가능성을 확인한 것으로 사료되며, Lat. curvatus GH-118-24는 한국생명공학연구원 생물자원센터에 특허 균주로 기탁하여 특허 균주 번호로 KCTC 19050P를 부여받았다.
요 약
본 연구는 국내 사천 지역의 특산물로부터 유산균을 분리하고자 하여 18 균주를 분리하고 16S rRNA 염기서열 분석을 통하여 동정을 실시하였다. 분리한 균주들의 가수분해효소 생산능을 확인하여 4 균주만이 단백질 가수분해효소 활성이 있는 것을 확인하였다. 4균주를 참굴 분말이 포함된 발효를 위해 배양하여 항산화 활성을 평가하기 위해 배양 상등액을 회수하였다. 각각의 배양 상등액들의 항산화 활성을 확인한 결과, Latilactobacillus curvatus GH-118-24 균주를 사용한 참굴 발효 배양 상등액의 경우에서 유산균을 접종하지 않은 참굴 비발효 배양 상등액에 비해 139.2%의 항산화 효과가 증가하는 것을 확인하였다. 그리고 항산화 활성이 가장 높은 배양 상등액에 해당하는 참굴-GH-118-24 발효배양액의 추출물을 제조한 후 항염증과 항당뇨 활성을 분석한 결과, 참굴비발효배양액의 추출물 대비 71.2%와 253.8%의 각각의 활성이 향상되는 것을 확인하였다. 이는 본 연구를 통하여 분리한 균주들의 식품 산업에서의 활용 가능성과 국내 유전자원 확보 확장에 도움이 될 것으로 생각된다.







