서 론
저항전분(resistant starch; RS)은 건강한 사람의 소장 안 에서 소화되지 않는 전분 및 부분적으로 가수분해된 전분 으로서 정의된다(Higgins, 2004). 저항전분은 식이섬유와 프리바이오틱스(prebiotics)처럼 포만감을 주고 대장건강을 향상시키고, 체중의 감소 및 유지에 도움을 줄 뿐만 아니 라, 혈당반응조절 및 혈중지질조성을 개선시키는 것으로 알려져 있다(Higgins, 2004; SharMa et al., 2008; Lee et al., 2012). 그래서 저항전분은 대사성 질환을 억제하고 건 강을 증진시키는 생리학적으로 유용한 식품원료로 인식되 고 있다. 저항전분은 4가지 형태로 분류할 수 있으나, 저 항전분의 정의에 따르면 4형 저항전분(RS4)인 화학적 변성 전분들 중 인산화 가교전분(phosphorylated cross-linked starch)이 소화효소에 의한 저항전분의 가수분해 지연 및 난소화성 측면에서 가장 효과적인 것으로 알려져 있다 (Englyst et al., 1992). 총 식이섬유 정량법(AOAC, 2000)에 의한 인산화 가교전분의 저항전분 함량은 법규 내에서 인 (phosphorus) 함량이 증가하면서 증가하였다(Woo & Seib, 2002). 그러나 이를 과도한 물에 분산시켜 열처리한 후 Englyst et al. (1992)에 의해 고안된 pancreatic α-amylase를 이용한 in vitro 소화도 시험법으로 분석하였을 때는 낮은 수준의 저항전분 함량을 나타내었다(Woo & Seib, 2002; Hwang et al., 2009). 인산화 가교전분이 포함된 고지방식 이를 쥐에 급여하였을 때 고지방식이 만을 급여한 쥐에 비 해 체중감소와 혈중지질조성의 개선 효과를 나타내었다 (Koo et al., 2010; Lee et al., 2012). 따라서 분석법에 따 른 인산화 가교전분의 저항전분 함량에 대한 논란에도 불 구하고 이는 저항전분 소재로서 받아들여지고 있다.
한편 화학적으로 합성되는 변성전분의 안전성에 대한 소 비자들의 우려가 증가하는 실정이며(Kim & BeMiller, 2012), 생리활성효능을 기대하기 위해 규제한도까지 변성처 리된 인산화 가교전분은 천연전분에 비해 팽윤력 적고 페 이스팅 점도가 발달하지 않는 등 제한된 가공적성을 나타 낸다(Woo & Seib, 2009; Lee et al., 2012). 그래서 인산화 가교화 전분들을 대체할 수 있고, 이의 잠재적인 문제점들 을 개선하며, 높은 저항전분을 보유한 starch citrate가 개발 되었다(Xie & Liu, 2004; Xie et al., 2006). Starch citrate 는 수분함량 10% 이하의 전분과 구연산 혼합물을 120°C 이상의 온도에서 가열할 때 구연산은 탈수반응을 통해 무 수구연산(citric anhydride)으로 전환되고 이는 전분의 hydroxyl 작용기와 추가적인 탈수반응에 의해 ester 화합물 을 형성한다. 추가적인 가열처리를 통해 starch monocitrate 는 인접하는 전분분자와 다시 ester 화합물을 형성함으로 써 전분 분자들을 가교화한다(Xie & Liu, 2004). 이와 같 은 전분과 구연산 사이의 다중 에스테르화 반응(multiple esterification)을 위해 주로 컨벡션 오븐을 반응기로 하여 합성된다(Xie & Liu, 2004; Xie et al., 2006; Ma et al., 2008). 약 93%의 저항전분을 함유한 starch citrate가 보고 되었지만, 반응온도와 반응시간이 증가할수록 갈변현상이 진행되며, 팽윤력이 급격히 감소하고, 페이스팅 점도가 발 달하지 않는 등 인산화 가교전분과 유사한 제한된 가공적 성을 나타낸다(Xie & Liu, 2004; Xie et al., 2006). 최근에 는 압출성형공법(Ryu et al., 2006; Wang et al., 2007)과 마이크로웨이브 조사(Jyothi et al., 2007)를 이용하여 starch citrate를 합성하는 방법들이 보고되었다. 이러한 방 법들은 천연전분에 비해 가공적성은 개선시킬 수 있었으나 2-18%의 저항전분 함량을 나타내어 저항전분 형성을 위해 서는 적절치 못하였다(Ryu et al., 2006; Jyothi et al., 2007; Wang et al., 2007). 따라서 본 연구는 쌍축압출성형 기를 반응기로 사용하여 starch citrate의 저항전분 함량에 대한 반응압출성형 공정요인의 영향을 조사하였으며, 형성 된 starch citrate들의 페이스팅 점도 특성의 평가를 통해 고 함량의 저항전분을 함유하면서 가공적성이 개선된 starch citrate를 개발하였다.
재료 및 방법
옥수수전분(수분 11.5%, 아밀로오스 26.5%)은 삼양제넥 스(Seoul, Korea)로부터 구입하여 추가적인 정제과정 없이 사용하였다. 무수구연산과 저항전분함량분석 kit (total resistant starch assay kit)는 덕산화학(Ansan, Gyeonggi, Korea)과 Megazyme (Wicklow, Ireland)에서 각각 구입하였 다. 이외에 시료 제조와 분석에 사용한 시약들은 ACS 등 급 이상의 것을 사용하였다.
무수구연산은 탈이온수에 용해시키고 10 N NaOH를 가 하여 pH 3.5로 조정하였다. 무수구연산의 농도는 전분의 건조중량 대비 10%와 40%가 되도록 하였다. 구연산 용액 1 kg과 전분 1 kg (dry basis, d.b)은 반죽기(Hobart Co., Troy, OH, USA)를 이용하여 상온에서 20분간 혼합한 후 스 테인리스강 쟁반으로 옮기고 50°C의 강제순환 열풍건조기 (OF-G, Jeio Tech Co., Ltd., Daejeon, Korea)에서 수분함량 7.5% 이하로 건조하였다. 건조된 전분-구연산 혼합물은 가 정용 믹서기(HMF-3450S, Hanil Electric, Incheon, Korea)를 이용하여 분쇄하고 50 mesh 표준체망(No. 500, Chunggye, Seoul, Korea)을 통과시켜 전분과 구연산 사이의 에스테르 화 반응을 위한 반응혼합물을 제조하였다.
제조된 반응혼합물의 반응압출성형은 성형노즐(die)이 제 거된 쌍축압출성형기(Incheon Machinery Co., Incheon, Korea)를 이용하여 수행하였다. 쌍축압출성형기의 스크류의 직경은 3 cm이고 스크류의 길이와 직경비(L/D ratio)는 25:1이었다. 시료의 주입구로부터 배출구 사이의 배럴온도 (반응온도)는 전열기와 냉각수 순환장치를 사용하여 일정하 게 유지되었으며 반응혼합물은 50 g/min의 속도로 쌍축압 출성형기에 투입하였다. 반응온도(130-190°C), 스크류 회전 속도(10-50 rpm)와 반응혼합물의 쌍축압출성형기 통과회수 (1-7 pass)를 반응압출성형 공정변수로 하여 starch citrate를 제조하였다. 대조군은 반응혼합물을 150°C의 컨벡션오븐 (FO-600M, Jeio Tech Co., Ltd., Daejeon, Korea)에서 1시 간 동안 반응시켜 제조하였다. 제조된 starch citrate들은 상 온(~24°C)으로 냉각한 후 과량의 50% 에탄올 수용액을 가 하여 10분간 교반한 후 감압여과하고 여과지 위의 전분 케이크는 과량의 50% 에탄올 수용액에 다시 분산시켰다. 이 세척조작은 총 3회 반복하였으며 마지막 세척과정에서 회수한 전분 케이크는 무수에탄올에 분산시켜 10분간 교반 하고 감압여과한 후 45°C에서 24시간 동안 건조하여 분석 시료로 하였다.
무수에탄올 150 mL는 5 N HCl 15mL와 혼합하여 에탄 올-HCl 혼합용액을 제조하였다. Starch citrate에 이온결합 된 나트륨염을 제거하기 위해 starch citrate (2 g, d.b)는 에탄올-HCl 혼합용액(50 mL)에 분산시켜 30분간 상온에 서 교반한 후 유리필터 부크너 깔때기(FN1160-011G/G4, Joylab, Seoul, Korea) 위에서 감압여과하여 전분시료를 회 수하였다. 회수된 전분시료는 80% 에탄올 수용액(100 mL) 을 가하여 10분간 상온에서 교반하고 감압여과였다. 이러 한 세척과정은 여액의 pH가 7-7.5가 될 때까지 반복하였다 (총 500 mL의 80% 에탄올 수용액이 사용되었다). 마지막 세척과정에서 회수된 전분시료는 무수에탄올(50 mL)에 분 산시켜 상온에서 10분간 교반하고 감압여과하여 45°C에서 건조하여 몰치환도 측정을 위한 시료로 하였다. 동일한 절 차를 거친 생전분을 공시험을 위한 시료로 하였다(Liu et al., 2012). 제조된 분석시료(1 g, d.b)는 250 mL 삼각플라스 크에서 75% 에탄올 수용액(30 mL)과 혼합하여 50°C에서 30분 동안 진탕하고 상온으로 냉각한 후 0.5 N NaOH (10 mL)을 가하여 상온에서 24시간 동안 교반하였다. 24시 간 후 페놀프탈레인용액을 3방울 가하고 0.1 N HCl 표준 용액(F=1.002, Duksan Co., Ansan, Gyeonggi, Korea)을 이 용하여 역적정(back-titration)하고 2시간 동안 상온에서 방 치한 후 추가로 적정하였다. 2차에 걸쳐 소비된 0.1 N HCl의 양으로부터 starch citrate에서 유리된 구연산 함량을 결정하였다. Starch citrate의 무수포도당에 대한 구연산의 몰수의 비율로 starch citrate의 몰치환도(molar degree of substitution)를 계산하였다(Ma et al., 2008).
생전분과 starch citrate의 FT-IR 스펙트럼은 Spectrum One System (Perkin-Elmer, Waltham, MA, USA)을 이용하 여 조사하였다. 브롬화칼륨(FT-IR grade, >99%; Sigma- Aldrich Co., St. Louis, MO, USA)과 전분 시료를 9:1의 중량비율로 혼합하고 타정하여 FT-IR 분석용 펠릿을 제조 하였다. FT-IR 스펙트럼은 400-4,000 cm–1의 파장범위에서 4 cm–1의 해상도로 분석하였다.
생전분과 starch citrate의 저항전분 함량은 AACC법 (approved method 32-40)에 따라 저항전분함량분석 kit (total resistant starch assay kit, Megazyme Int., Wicklow, Ireland)를 이용하여 분석하였다(AACC, 2000).
생전분과 starch citrate의 페이스팅 특성은 신속점도분석 기(RVA-4D, Newport Scientific, NSW, Australia)를 이용하 여 조사하였다. 전분시료(2.24-3.36 g, d.b)을 알루미늄 용기 에 직접 칭량하고 총 28 g이 되도록 탈이온수를 가한 후 spatula와 플라스틱 회전축을 이용하여 전분시료를 완전하게 분산시켜 분석시료(고형분 함량 8.0-12.0%, w/w)를 제조하 였다. 신속점도분석기는 2분간 50°C로 유지하고 95°C까지 4분에 걸쳐 가열하여 95°C에서 2분간 유지시킨 후 50°C까 지 4분에 걸쳐 냉각하고 50°C에서 2분간 유지시켜 페이스 팅 점도 프로파일을 얻었다. 플라스틱 회전축은 신속점도분 석기가 조작되는 동안 160 rpm으로 일정하게 회전시켰다.
결과 및 고찰
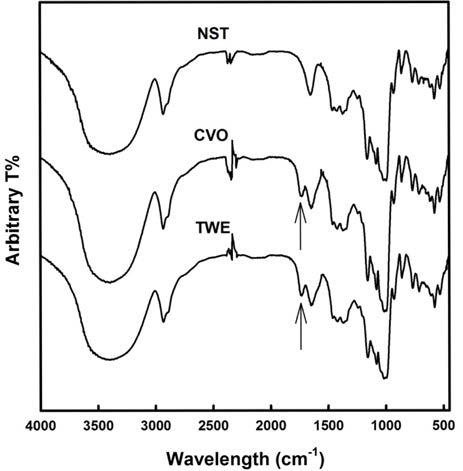
반응기로서 쌍축압출성형기를 이용하여 starch citrate를 합성하였을 때 전분분자들과 구연산 사이의 ester 결합 형 성여부를 확인하기 위해 전분-구연산 반응혼합물은 배럴 반응온도 150°C, 스크류 속도 50 rpm의 쌍축압출성형기를 5회 통과시켜 starch citrate (TWE)을 제조하고 FT-IR 스펙 트럼을 조사하였다(Fig. 1). 대조군으로는 동일한 반응혼합 물을 150°C의 컨백션 오븐에서 1시간 동안 처리하여 제조 한 starch citrate (CVO)를 사용하였다. 생전분은 전형적인 전분의 FT-IR 스펙트럼들을 나타내었다(Fig. 1, NST) (Xie et al., 2006; Ma et al., 2008). 반면에 컨백션 오븐(Fig. 1, CVO)과 쌍축압출성형기(Fig. 1, TWE)를 이용하여 제조한 starch citrate들은 ester 결합의 carbonyl 작용기에 의한 stretching vibration으로부터 형성되는 1720-1,750 cm–1의 새로운 피크가 형성되었다(Fig. 1, arrow) (Xie et al., 2006; Ma et al., 2008). 따라서 쌍축압출성형기를 반응기로 사용 하는 경우에도 전분분자와 구연산 사이의 에스터화반응이 일어나는 것을 확인할 수 있었다.
반응압출성형공정의 운전조건에 따른 starch citrate의 저 항전분 함량 변화를 조사하였다(Fig. 2). 대조군으로써 10%와 40% 구연산의 반응혼합물을 150°C의 컨백션 오븐 에서 1시간 동안 처리하여 제조한 starch citrate로 하였다. Xie & Liu (2004)와 Xie et al. (2006)는 최대 저항전분 함량을 얻기 위해 40% 구연산 농도의 반응혼합물을 140- 150°C의 컨백션 오븐에서 7시간 동안 반응시켜 starch citrate를 제조하였다. 본 연구에서는 대조군의 반응시간을 1시간으로 하였는데, 이는 반응압출성형에 의한 starch citrate의 제조 시 스크류 회전속도 10 rpm에서 운전되는 쌍축압출성형기로 반응혼합물을 7회 통과시킬 때(반응혼합 물이 쌍축압출성형기 내에 가장 오랫동안 체류하는 경우) 54-56분이 소요되었다. 따라서 반응압출성형에 의한 starch citrate의 반응시간과 대조군의 반응시간을 유사하게 하기 위해 1시간으로 하였다. 10%와 40% 구연산 농도에서 컨 백션 오븐을 이용하여 제조한 starch citrate의 저항전분 함 량은 각각 29.3%와 79.5%이었다.
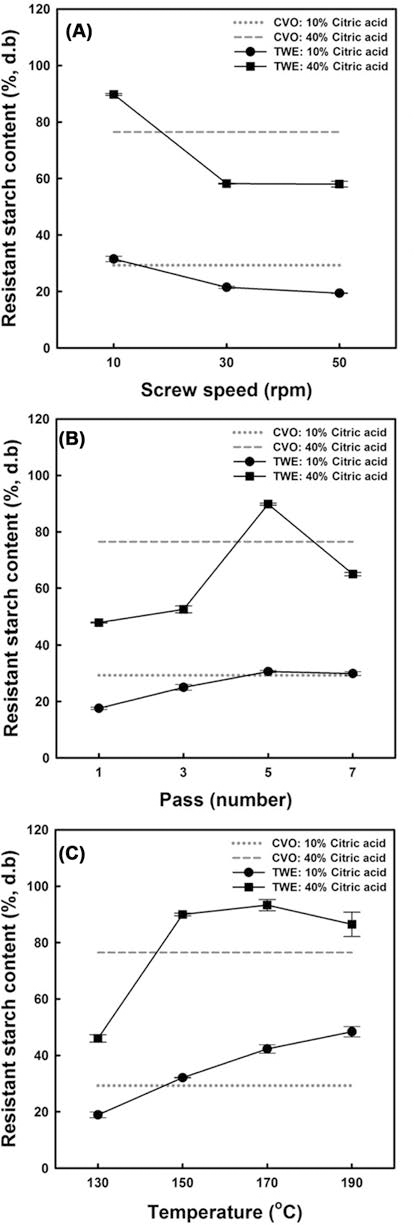
반응온도 150°C와 쌍축압출성형기 통과횟수 5회로 할 때, 스크류 회전속도(10-50 rpm)에 대한 starch citrate의 저 항전분 함량 변화를 조사하였다(Fig. 2A). 10% 구연산 농 도에서 제조된 starch citrate의 저항전분 함량은 스크류 회 전속도가 빨라질수록 32.1%에서 19.4%로 감소하였다. 40% 구연산 농도에서는 스크류 회전속도가 10 rpm에서 30 rpm으로 빨라지면서 저항전분 함량이 90.0%에서 58.2%로 감소하였으나 50 rpm에서는 58.0%로 30 rpm의 경우와 유 의적인 차이를 나타내지 않았다. 또한 스크류 회전속도 10 rpm에서 starch citrate를 합성하였을 때 모든 구연산 농도 에서 대조군의 저항전분 함량을 초과하였다. Wing (1996) 은 전분과 구연산 사이의 반응효율은 반응시간이 증가할수 록 증가한다고 보고하였다. Xie & Liu (2004)는 반응시간 이 7시간까지 증가할수록 starch citrate의 저항전분 함량은 증가한다고 보고하였다. 따라서 스크류 회전속도가 빨라지 면서 starch citrate의 저항전분 함량이 감소하는 일반적인 경향은 반응혼합물이 쌍축압출성형기 내에 체류하는 시간 (반응시간)이 짧기 때문으로 판단된다.
반응온도 150°C와 스크류 회전속도 10 rpm에서 반응혼 합물의 쌍축압출성형기 통과횟수에 대한 starch citrate의 저항전분 함량 변화를 조사하였다(Fig. 2B). 10% 구연산 농도의 반응혼합물은 통과횟수가 5회까지 starch citrate의 저항전분 함량은 지속적으로 증가하여 30.6%에 도달하였 으며 7회 통과한 경우와는 저항전분 함량(29.9%)이 유의적 으로 다르지 않았다(Fig. 2B). 반면에 40% 구연산 농도의 반응혼합물은 통과횟수가 3회에서 5회로 증가하면서 저항 전분 함량은 급격히 증가하여 90.0%에 도달하였고 7회까 지 통과시켰을 때는 65.0%로 감소하였다(Fig. 2B). Xie & Liu (2004)는 반응시간 7시간까지 치환도(degree of substitution)와 저항전분 함량이 지속적으로 증가하였지만 반응시간을 9시간까지 연장하였을 때 전분분자에 치환된 구연산의 해리현상에 의해 치환도와 저항전분 함량이 감소 하였다고 보고하였다. 유사하게 40% 구연산 농도의 반응 혼합물을 7회까지 통과시킬 때 쌍축압출성형기의 체류시간 의 연장은 스크류들의 맞물림 현상에 의해 전분입자들이 손상되어 세척과정에서 치환된 전분분자들의 부분적인 손 실 때문으로 생각된다. 따라서 쌍축압출성형기를 반응기로 활용하여 starch citrate를 합성할 때 반응혼합물을 5회까지 통과시키는 것이 저항전분 함량을 최대로 얻을 수 있을 것 으로 판단된다.
스크류 회전속도 10 rpm과 쌍축압출성형기 통과횟수 5회 로 할 때, starch citrate의 저항전분 함량에 대한 배럴(반응) 온도의 영향을 조사하였다(Fig. 2C). 10% 구연산 농도의 반 응혼합물에 있어서 130°C에서 190°C로 반응온도의 상승과 함께 starch citrate의 저항전분 함량은 18.9%에서 48.4%까 지 지속적으로 상승하였다. 그러나 40% 구연산 농도의 반 응혼합물에 있어서는 130°C에서 150°C로 상승하면서 저항 전분 함량은 46.0%에서 90.0%로 급격히 상승하였으며 170- 190°C에서는 150°C에서의 저항전분 함량과 유의적인 차이 를 보이지 않았다. 이는 Wing (1996)과 Xie & Liu (2004) 들은 본 연구결과와 유사한 현상을 보고하였다. 따라서 배 럴온도 150°C와 스크류 회전속도 10 rpm의 쌍축압출성형기 로 반응혼합물을 5회 통과시키는 것이 가장 높은 함량의 저항전분을 함유한 starch citrate를 빠른 시간 내(starch citrate 1 kg 제조 시 약 45-46분 소요)에 제조할 수 있었다.
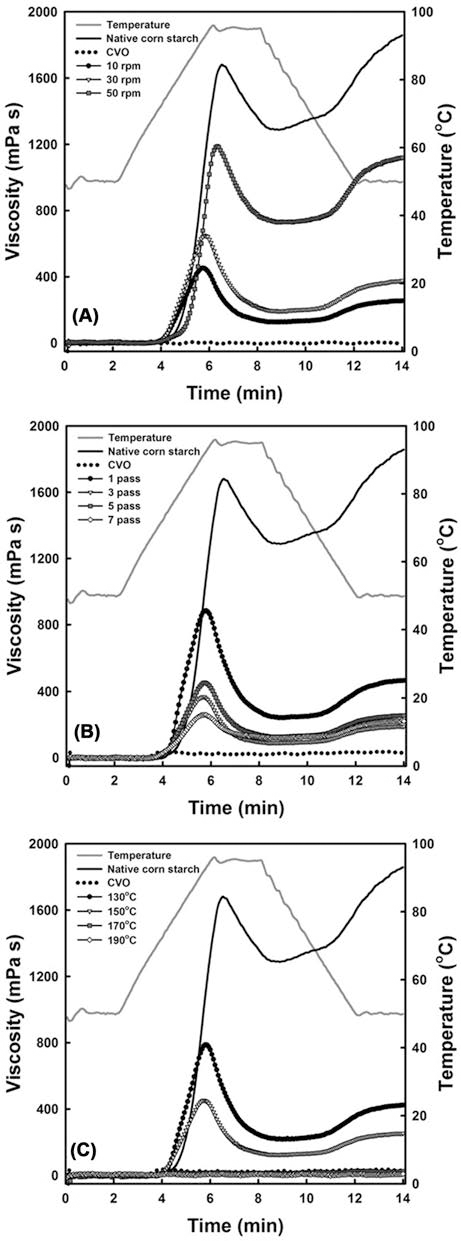
반응압출성형조건들에 의해 형성된 starch citrate들의 페 이스팅 점도 프로파일들은 고형분 함량 8.0% (w/w)에서 신속점도분석기를 이용하여 조사하였다(Fig. 3). 구연산 농 도와 관계없이 컨백션 오븐에서 합성된 starch citrate들은 신속점도분석기에 의해 페이스팅 점도가 발달하지 않았다 (Fig. 3 dotted line). 이와 동일한 결과를 보고한 Xie & Liu (2004)와 Ma et al. (2008)에 의하면 구연산이 전분분 자들 사이에서 다중 에스테르화 반응을 통해 형성된 구연 산과 전분분자들 사이의 가교화 결합은 전분입자의 구조적 안정성을 향상시켜 starch citrate들의 용해도와 팽윤력이 감소시킴으로써 페이스팅 점도가 발달되지 않는다고 보고 하였다. 또한 Xie et al. (2006)은 starch citrate의 결정구조 는 과도한 열처리로 붕괴되었다고 보고하였다. Tester & Morrison (1990)의 전분입자의 팽윤은 아밀로펙틴들 사이 의 상호작용에 의한 체계적인 구조체들 때문이라는 보고에 의하면 컨벡션 오븐에서 형성된 starch citrate들의 페이스 팅 점도가 발달하지 않는 것은 구연산과 전분분자들 사이 의 가교화 결합에 의한 전분입자의 용해도와 팽윤력이 감 소되었거나 결정구조가 손실되었기 때문인 것 같다. 반면 에 쌍축압출성형기에 의한 starch citrate들은 반응조건에 따 라 상이한 점도 수준을 나타내지만 신속점도분석기에 의해 페이스팅 점도가 유의적인 수준으로 발달되었다. 10% 구연 산 농도의 반응혼합물을 이용할 때, 스크류 회전속도가 감 소하면서 페이스팅 점도는 증가하였으며(Fig. 3A), 쌍축압출 성형기 통과횟수의 증가는 페이스팅 점도를 감소시켰다(Fig. 3B). 또한 130°C에서 150°C로 반응온도의 상승은 페이스팅 점도를 감소시켰으며, 170°C와 190°C에서 반응한 starch citrate들은 컨백션 오븐을 이용한 starch citrate들과 동일하 게 페이스팅 점도가 발달하지 않았다(Fig. 3C). 40% 구연산 농도의 반응혼합물을 이용할 때, 반응온도 150°C, 스크류 회전속도 50 rpm, 쌍축압출성형기 통과횟수 5회에서 제조된 starch citrate만이 유의적인 수준의 페이스팅 점도가 발달되 었으며(Fig. 4B), 이외의 다른 조건들에서는 페이스팅 점도 가 발달되지 않았다. 조사된 모든 경우에 있어 열처리 시간 과 정도가 증가할수록 starch citrate의 페이스팅 점도는 감 소하거나 발달하지 않았다. 그럼에도 쌍축압출성형기를 사 용하는 것이 컨백션 오븐에 의한 starch citrate에 비해 페이 스팅 점도를 유의적으로 발달시키는 것은 반응혼합물이 쌍 축압출성형기 내에서 스크류의 회전운동에 의해 지속적으로 이동하면서 가열되기 때문에 전분입자의 열에 의한 손상도 가 컨백션 오븐에 비해 적기 때문으로 생각된다.
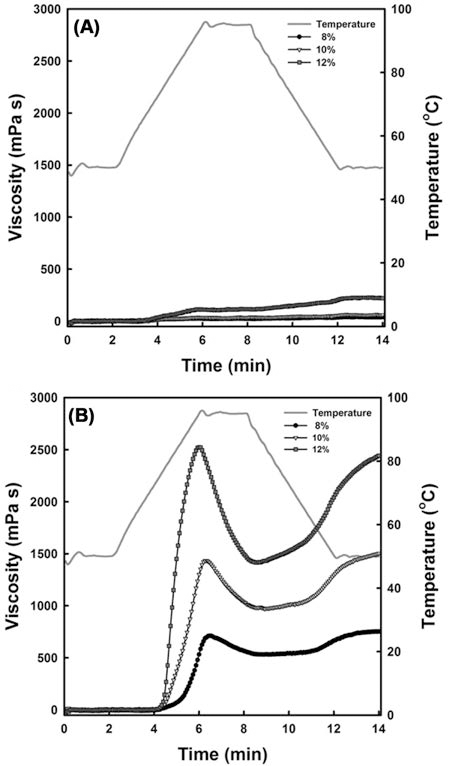
유사한 저항전분 함량을 보유하는 starch citrate들의 페 이스팅 점도 특성에 대한 반응조건의 영향을 조사하였다. 또한 반응압출성형공정에 의한 starch citrate들은 여전히 생전분의 페이스팅 점도에 비해 낮은 수준을 나타내기 때 문에 천연전분의 페이스팅 점도와 유사한 수준의 페이스팅 점도를 starch citrate가 발달시킬 수 있는 농도 범위를 조 사하였다. 40% 구연산 농도의 반응혼합물을 150°C에서 스 크류 회전속도가 30 rpm (TWE-30)과 50 rpm (TWE-50)으 로 달리하여 쌍축압출성형기를 5회 통과시킨 starch citrate 들이 사용되었다(Fig. 4 & Table 1). TWE-30과 TWE-50 의 몰치환도는 각각 0.032와 0.027이었으며, TWE-30이 유 의적으로 높은 수준을 나타내었으나 두 starch citrate들의 몰치환도 차이(ΔMS = 0.005)가 크지 않았다(Table 1). 그 결과 TWE-30과 TWE-50의 저항전분 함량은 각각 58.2% 와 58.0%로 유의적인 차이를 나타내지 않았다(Table 1). TWE-30의 경우 신속점도분석시료의 고형분 함량이 8.0에 서 12.0%로 상승하여도 페이스팅 점도의 발달은 극히 적 었으나(Fig. 4A), TWE-50은 고형분 함량의 증가와 함께 페 이스팅 점도가 급격히 발달하였다(Fig. 4B). 또한 TWE-50에 있어 최고점도(peak viscosity), 최저점도(trough viscosity), 붕괴점도(breakdown viscosity), 최종점도(final viscosity)와 노화점도(setback viscosity)등 페이스팅 점도 특성치들은 신속점도분석시료의 고형분 함량 증가비율보다 급격히 증 가하는 현상을 나타내었다(Table 1). 유사한 저항전분 함량 에도 불구하고 TWE-30과 TWE-50의 페이스팅 점도의 차 이는 이들의 몰치환도의 차이 때문인 것 같다(Xie & Liu, 2004; Xie et al., 2006). 따라서 구연산에 의해 가교화된 starch citrate의 경우에 있어 적절한 가공적성을 보유하기 위해서는 최소한의 열처리가 수반되어야 할 것으로 생각된 다. 한편 TWE-30의 페이스팅 점도가 발달하지 않는 것이 반응혼합물이 쌍축압출성형기를 통과하면서 전분의 입자구 조의 붕괴로 인한 것인지를 조사하기 위해 컨백션 오븐에 의해 제조된 starch citrate (CVO), TWE-30와 TWE-50의 형태학적 특성을 전계방출전자현미경을 이용하여 관찰하였 다(Fig. 5). CVO의 경우에 있어 전분의 입자구조가 붕괴된 조각들과 입자표면이 변형된 전분입자들이 관찰되었으나 대 부분 입자구조를 유지하고 있었다. 이에 비해 TWE-30과 TWE-50의 전분입자의 구조적 손상 정도는 유사하였지만 CVO의 것보다 심하였다(Fig. 5). 이는 전분입자들이 이축 스크류들의 완전맞물림 회전에 의해 발생하는 전단력에 의 해 손상된 것으로 생각된다. 그럼에도 TWE-30과 TWE-50 들은 대부분 전분입자 형태를 유지하고 있는 starch citrate 로 구성되어 있었다(Fig. 5). 따라서 TWE-30의 페이스팅 점 도가 발달하지 않는 것은 전분입자 구조의 손상에 의한 부 분적인 영향일 수 있지만 TWE-30의 몰치환도가 TWE-50 보다 유의적으로 높은 것을 고려할 때(Table 1) 구연산에 의한 전분분자들 사이의 빈번한 가교화 반응이 주요 원인인 것으로 생각된다. 한편 8% 농도의 생전분의 페이스팅 점도 와 유사한 수준의 페이스트를 제조하기 위해서는 starch citrate는 10-12%의 농도로 사용하여야 할 것으로 판단된다.
1) Mean value of two measurement; values within a column sharing the same lowercase letter are not significantly different in a given concentration of citric acid (p<0.05).
2) MS; molar degree of substitution, RS; resistant starch content, TS; total solid content, Tp; Pasting temperature.

Starch citrate의 저항전분 함량에 따른 반응방법의 영향 을 조사하기 위해 저항전분 함량은 유사하면서 컨백션 오 븐(CVO)과 쌍축압출성형기(TWE-5P, TWE-7P)를 이용하여 제조된 starch citrate들에 대하여 12% (w/w) 고형분 함량에 서 페이스팅 점도 특성치들을 조사하였다(Table 1). CVO, TWE-5P와 TWE-7P의 몰치환도는 각각 0.028, 0.011과 0.014로 유의적인 차이를 나타내었으나 이들의 저항전분 함량은 29.3-30.6%의 범위로 통계적으로 유의적인 차이를 보이지 않았다(Table 1). CVO는 12% 고형분 함량에서 페 이스팅 점도를 발달시키지 못했으나 TWE-5P와 TWE-7P 는 유의적인 페이스팅 점도를 발달시켰고 TWE-5P가 TWE-7P보다 높은 수준의 점도특성을 나타내었다(Table 1). 이러한 결과는 구연산과 전분분자들 사이의 가교화 반응의 정도의 차이 때문인 것으로 판단된다. 게다가 쌍축압출성 형기를 5회 통과시킨 TWE-5P의 경우 생전분을 대체하여 사용할 수 있을 만큼 충분한 페이스팅 점도를 발달시켰다 (Table 1). 따라서 starch citrate를 제조할 때 반응혼합물이 정지된 상태에서 열처리하는 것 보다는 열처리하는 동안 반응혼합물을 지속적으로 이동시키는 것이 전분분자와 구 연산 사이의 반응성은 낮지만 유사한 저항전분을 함유하면 서 페이스팅 점도를 성공적으로 발달시킬 수 있는 starch citrate를 제조하는데 적합한 것으로 보인다.
요 약
전분과 구연산 사이의 다중 에스테르화반응에 의한 starch citrate의 저항전분 함량에 대한 반응압출성형조건들 의 영향을 조사하였으며, 이들의 페이스팅 점도 특성을 조 사하여 산업적 활용도가 높은 starch citrate를 제조할 수 있는 반응조건을 탐색하였다. 반응압출성형에 의한 starch citrate를 제조하기 위해 성형노즐을 제거한 쌍축압출성형기 를 사용하여 반응온도, 스크류 회전속도, 반응혼합물의 쌍 축압출성형기 통과횟수를 변수로 하였다. 반응온도가 높아 지면서, 스크류 회전속도가 느려지면서, 쌍축압출성형기 통 과횟수가 증가하면서 starch citrate의 저항전분 함량은 증 가하는 경향을 나타내었다. 40% 구연산 농도의 반응혼합 물을 150°C와 스크류 회전속도 10 rpm의 쌍축압출성형기 를 5회 통과시킬 때 90%의 저항전분을 보유한 starch citrate를 얻을 수 있었다. 또한 40% 구연산 농도의 반응혼 합물을 150°C와 스크류 회전속도 50 rpm의 쌍축압출성형 기를 5회 통과시킬 때 58%의 저항전분을 보유한 starch citrate를 얻을 수 있었으며, 이는 유의적인 페이스팅 점도 를 발달시켜 높은 저항전분 함량에도 불구하고 가공적성이 우수한 starch citrate를 얻을 수 있었다. 또한 starch citrate 의 제조 시 전통적으로 사용되는 컨백션 오븐 보다는 쌍축 압출성형기를 사용하는 것이 가공적성이 우수한 starch citrate를 제조할 수 있을 것으로 보인다. 따라서 본 연구에 서 보고한 50%(s.b) 이상의 저항전분을 보유하면서도 페이 스팅 점도 특성을 잃지 않은 starch citrate와 쌍축압출성형 기를 활용한 starch citrate 제조기법들은 산업적 활용도 높 을 것으로 예상되며 기존의 저항전분 소재들을 대체할 수 있는 잠재력이 높은 저항전분 소재일 것으로 생각된다.







