서 론
최근 서구화된 식습관의 영향으로 비만이 증가함과 동시 에 고지혈증 및 고콜레스테롤증으로 인한 순환기 질환의 발생이 증가하고 있는 가운데 심뇌혈관 질환의 발생을 억 제하는데 도움을 줄 수 있는 건강기능식품 소재로서 폴리 코사놀이 주목을 받고 있다(Oh, 2010). 폴리코사놀은 사탕 수수의 줄기와 잎의 피막부분에서 추출되어 정제된 8개의 고분자량 일차 지방족 알코올의 혼합물인데 HMG-CoA reductase를 직접적으로 억제하기 보다는 조절에 의하여 메 발로네이트 형성 이전에 콜레스테롤의 생합성을 저해하는 것으로 알려져 있다(McCarty, 2002; Singh et al., 2006). 폴리코사놀을 고콜레스테롤 혈중 노인환자 1470명에 대하 여 3년 동안 하루 5 mg을 투여하면 총 콜레스테롤은 22% 까지, LDL콜레스테롤은 30%까지 저하시키고 HDL 콜레스 테롤은 15%까지 증가시켰다고 하는데, 특히 세포 표면의 LDL 콜레스테롤 수용체를 증가시킴에 의해 지질저하 효과 를 나타낸다고 한다(Chen et al., 2005). 또한 폴리코사놀의 투여는 고콜레스테롤 혈중 환자 및 제2형 당뇨병 환자들에 있어서 용량의존적으로 혈소판 응집을 억제하여 관상동맥 질환의 위험을 낮출수 있다고 하였다(Torres et al., 1995; Crespo et al., 1997).
최근 국내외에서는 이들의 생리활성을 활용한 건강기능 식품으로의 상품화가 다양하게 진행되고 있으며(Irmark et al., 2006; Choi et al., 2016) 원료에 대한 기준 및 규격을 설정하기 위하여 폴리코사놀에 들어 있는 각각의 지방족 알코올을 정량분석하는 방법이 검토되고 있는데 MSTFA (N-methyl-N-(trimethylsilyl) trifluoroacetamide)로 유도체화 시킨 후 SPB-5 혹은 그와 동등한 컬럼이 장착된 GC-FID를 이용하여 분석하거나, GC-MS에서 정량분석하는 방법이 제 안되어 있는 실정이다(Gonzalez-Canavaciolo & Magraner-Hernandez, 1999; Dunford et al., 2010; Jung et al., 2011). 하지만 본 연구에서와 같이 폴리코사놀이 유화된 수용액을 분석하는 경우에는 유화제 피크의 영향으로 기존의 방법에 따른 정량분석이 용이하지 않으므로 불순물에 의한 간섭을 최소화하면서 특정이온을 선택하여 고감도의 정량분석이 가능한 selected ion monitoring (SIM) mode에서의 GCMS분석법으로 정량 분석하는 방법을 제안하고 그 적합성 을 검증하고자 하였다.
재료 및 방법
본 실험에서 사용한 폴리코사놀 시료(3%, w/w)는 국내 유통 업체인 (주)뉴트리(Seongnam-Si, Korea)에서 입수하 여 사용하였다. 그 외에 표준품 및 전처리 시약은 Sigma Chemical사(St. Louis, MO, USA) 제품을 사용하였으며, GC-MS (HP 5890/HP5973, Agilent Inc., Santa Clara, CA, USA) 의 분석조건은 Table 1과 같았다.
Hexacosanol, heptacosanol, octacosanol, triacontanol 각각 6.0 mg을 정확히 취하여 한 개의 10 mL 용량 플라스크에 모두 넣어 폴리코사놀 표준품 혼합액을 만들고 증류수로 10 mL 표선에 맞추어 정용하였다. 또한 내부표준물질로서 eicosanol 6.0 mg을 정확히 취하여 별도의 10 mL 용량 플 라스크에 넣고 증류수로 10 mL 표선에 맞추어 정용하였 다. 이 후 폴리코사놀 표준품의 혼합 수용액으로부터 각각 10 μL, 20 μL, 50 μL, 100 μL를 취하여 각각의 바이얼에 담고 내부표준용액(internal standard, ISTD)용액 20 μL와 N-Methyl-N-(trimethylsilyl)trifluoroacetamide (MSTFA) 100 μL를 각각의 바이얼에 넣어 각 바이얼의 용액이 600 μL 가 되도록 클로로포름을 넣었다. 즉 순서대로 470 μL, 460 μL, 430 μL, 380 μL 의 클로로포름을 보충해서 넣 고 80°C 오븐에서 40분간 반응시켜 silyl유도체를 만들고 방냉한 후 GC-MS로 Table 2의 SIM mode에서 분석하였 다.
폴리코사놀 시료 중 폴리코사놀의 실제 함량을 분석하기 위하여 폴리코사놀 3% 시료 0.15 g을 10 mL 용량플라스 크에 취하고 이어서 내부표준물질 용액(eicosanol 60 mg을 100 mL 용량 플라스크에 넣고 클로로포름으로 정용하여 만든 용액)을 넣어 10 mL로 정용한 후 혼합하였다. 여기 에서 100 μL 취하여 바이얼에 옮겨 담고, MSTFA 100 μL과 400 μL의 클로로포름을 넣는 후 80°C 오븐에서 40 분간 반응시키고 실온에서 방냉시킨 뒤 GC-MS로 Table 1 의 조건에서 분석하였다.
또한 폴리코사놀 3% 시료 5 mg을 유화제로 30 mL의 정제수에 유화시켜 만든 폴리코사놀 수용액의 경우에는 동 량(30 mL)의 클로로포름을 넣어 흔들어 섞은 후 클로로포 름 층만 분리하였다. 이어서 농축기로 클로로포름 층의 용 매를 모두 제거한 후 다시 1 mL의 클로로포름으로 시료 를 잘 녹인 후 100 μL를 취하여 새로운 바이알에 옮겨 담 았으며 이어서 내부표준물질인 eicosanol (600 ppm) 용액 100 μL를 넣은 후, MSTFA 100 μL, 클로로포름 300 μL 를 담아 최종 부피가 600 μL가 되게 하였다. 이 후 80°C 오븐에서 40분간 반응시켜 silyl유도체를 만들고 방냉시킨 뒤 GC-MS로 Table 1 및 2의 조건에서 분석하였다.
결과 및 고찰
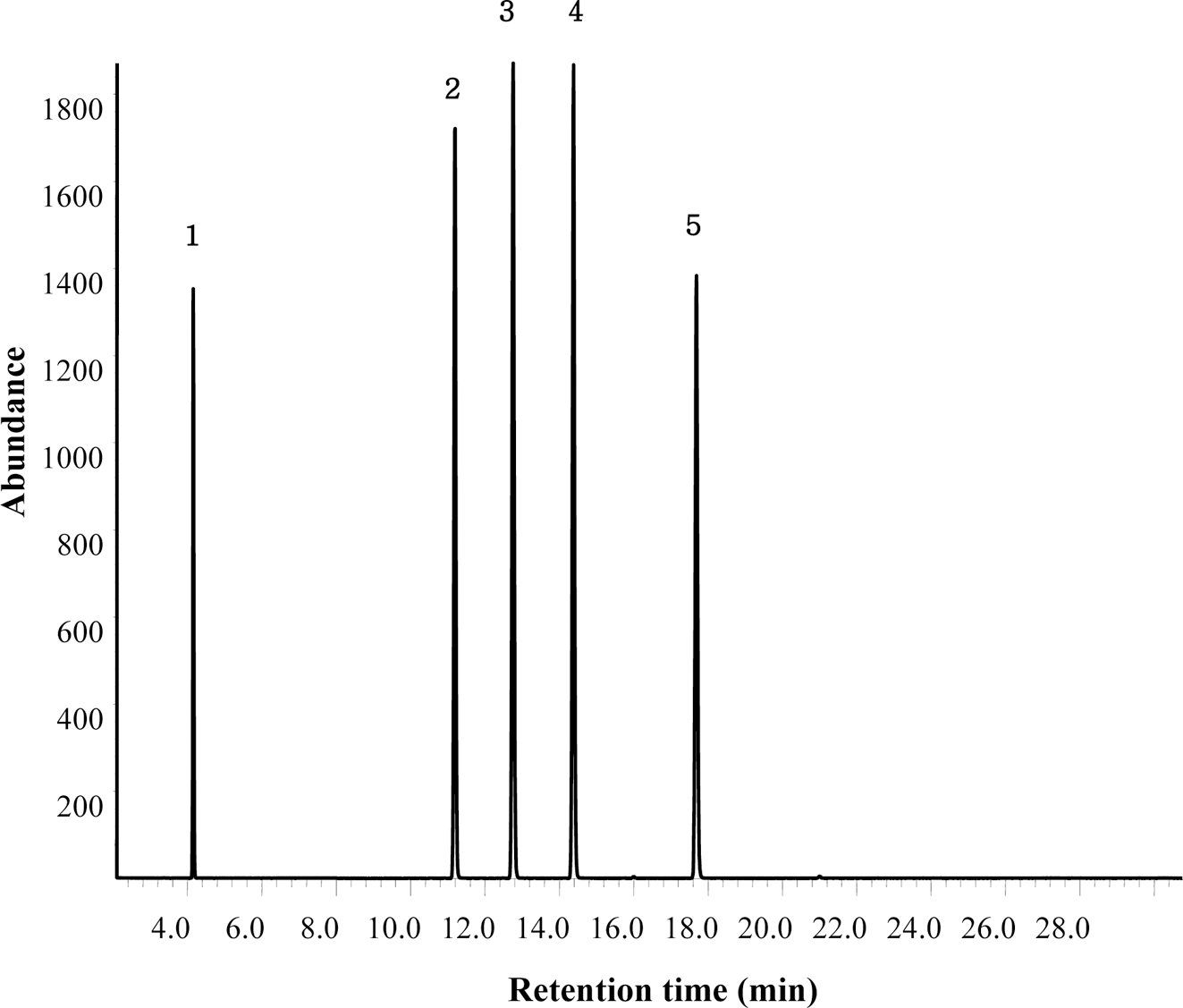
폴리코사놀의 표준품 4종과 내부표준품인 eicosanol을 TMS유도체화하여 GC-MS로 분석하여 얻은 크로마토그램은 Fig. 1과 같다. 폴리코사놀은 탄소수에 따라서 eicosanol이 가장 먼저 용출되었으며 이어서 hexacosanol, heptacosanol, octacosanol, tricontanol 의 순서로 검출되었다. 각 피크의 용출시간은 각 성분의 농도의 증가에 따라서도 일정하였으 며 GC-MS의 SIM mode에서 얻은 크로마토그램에서는 내 부표준품의 피크와도 분명히 분리되어 정량분석에 방해인 자는 없었다.
각 폴리코사놀 표준품의 회수율(recovery, %), 상대표준 편차(CV, coefficient of variation, %), 검출한계(LOD, limit of detection) 및 정량한계(LOQ, limit of quantification)를 Table 3에 나타내었다. 회수율은 폴리코사놀 표준용액을 3 회 분석하여 얻은 각 폴리코사놀의 평균값의 합을 총 함량 으로 나누어 구하였는데 평균 90.5%로서 시료에 포함되어 있는 폴리코사놀 함량의 90% 이상을 분석 가능함을 알 수 있었다.
상대표준편차(CV)는 동일한 폴리코사놀 표준용액을 3회 분석하여 얻은 각 폴리코사놀의 값의 표준편차를 평균으로 나누어 구하였는데 0.48-5.83%로서 동일한 분석방법에 의하 여 얻은 데이터들이 일반적인 수준에서 일치함을 나타내고 있었다. 검출한계(LOD)는 본 연구에서 얻은 검량선을 사용 하여 검출 가능한 최소량으로서 0.000479-0.001314 μg/μL이 었으며 정량한계(LOQ)는 적절한 정밀성과 정확성이 확보되 는 가운데 정량 가능한 최소량인데 본 연구결과에서는 0.001452-0.003983 μg/μL으로서 적절한 수준으로 판단되었다. Gonzalez-Canavaciolo & Magraner-Hernandez (1999)의 폴 리코사놀의 TMS유도체 분석에서 상대표준편차는 0.75%로 서 본 연구에서보다 편차가 적은 것으로 보고하고 있다.
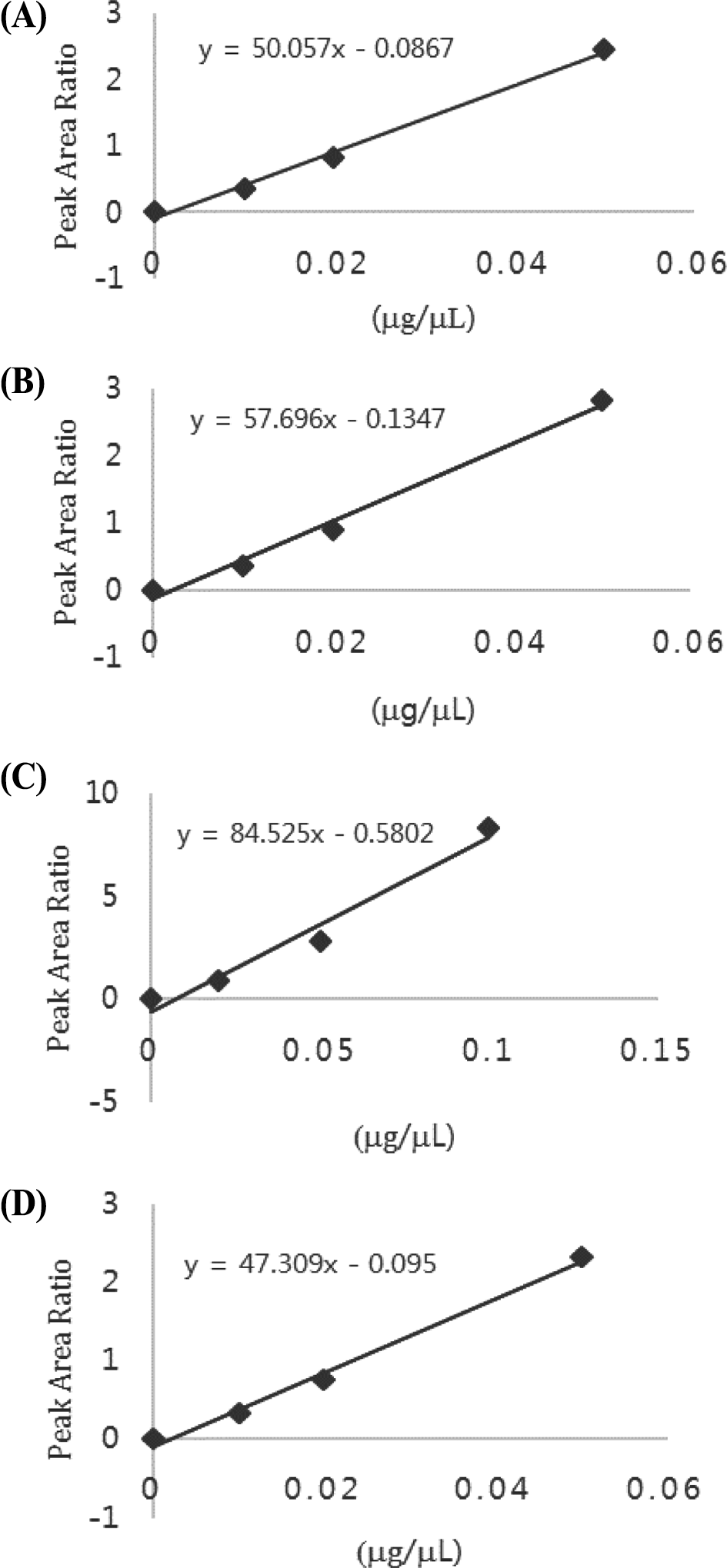
4종류의 폴리코사놀 표준품을 혼합하고 내부표준물질로 eicosanol을 첨가하여 분석 후에 각 폴리코사놀 피크의 면 적을 내부표준물질의 면적으로 나누어 구한 면적비를 Y축, 폴리코사놀의 농도를 X축으로 검량선을 작성한 결과는 Fig. 2와 같았으며 각 검량선의 직선성을 나타내는 상관계 수는 0.974-0.995로서 Gonzalez-Canavaciolo & Magraner-Hernandez (1999)의 보고(0.9996)에 근접한 결과를 얻을 수 있었다.
폴리코사놀 표준품의 농도 별 혼합용액을 TMS유도체화 한 후 GC-MS로 분석하여 얻은 분석결과를 이용하여 일내 정확성과 정밀성을 구하였다. 일내 반복하여 얻은 결과의 정확성은 80.38-108.98%이었으며, 정밀성은 0.01-4.88%인 것으로 나타났다. 본 연구결과의 정확성은 최저정량한계인 80-120% 범위 내에는 포함되었으나, 일반적으로 요구되는 정량한계인 85-115%에는(Seo et al., 2009) 일부 미흡한 것 으로 보이며, CV가 15% 이내 이어야 하는 정밀성은 충족 하는 것으로 판단되었다.
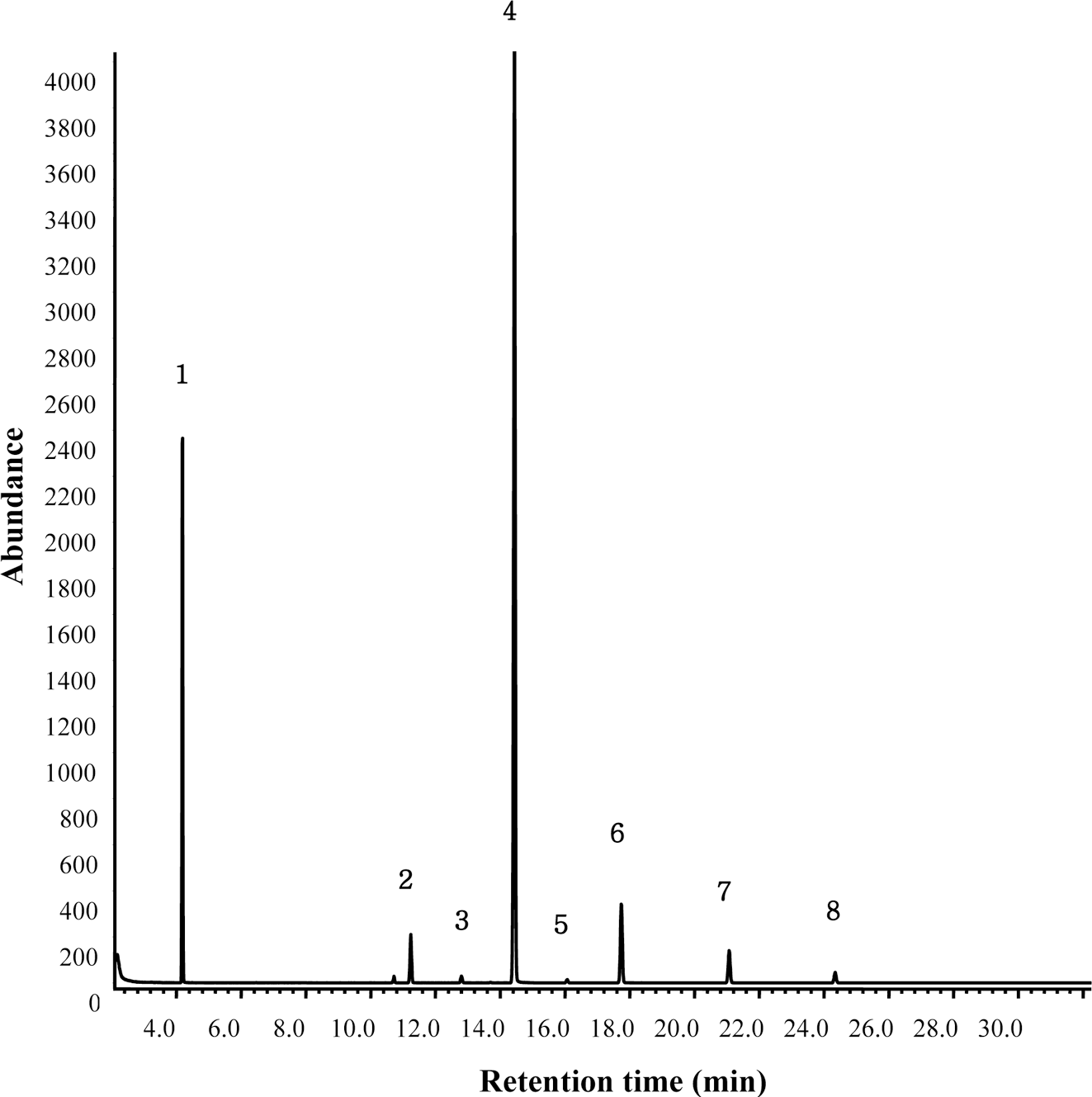
폴리코사놀 3% 시료(0.15 g)에는 4.5 mg의 폴리코사놀이 함유되어 있는데 이를 내부표준물질이 함유된 10 mL 클로 로포름에 용해하였다. 여기에서 취한 100 μL 용액에는 폴 리코사놀이 45 μg 함유되어 있고, 유도체화 시약인 MSTFA 와 용매가 추가되면 반응 후에는 반응액이 600 μL가 되므 로, 반응액 1 μL에는 0.075 μg의 폴리코사놀이 함유되어 있 다. 따라서 GC-MS 분석결과의 시료 중 폴리코사놀 함량 이 0.075 μg으로 계산되면 100%가 정량된 것이므로 시료 의 분석 후 정량된 폴리코사놀 함량(μg)의 비율(%)을 비례 식으로 계산할 수 있었다. 이에 따라 폴리코사놀 시료를 이상과 같이 3회 분석한 결과는 87.43±4.48%로서 시료 중 폴리코사놀 함량은 표시량인 4.5 mg의 80-120% 범위 내에 함유되어 있음을 알 수 있었다. 또한 폴리코사놀 3% 시료 (5 mg)가 30 mL의 정제수에 유화되어 있는 수용액 중에는 폴리코사놀이 150 μg (=5,000 μg×3%) 함유되어있다. 따라 서 30 mL의 클로로포름으로 추출 후 농축한 클로로포름층 1mL에는 150 μg의 폴리코사놀이 함유되어 있으며 이 중 에서 100 μL를 취하여 MSTFA 시약과 클로로포름을 첨가 하여 반응시키면 15 μg의 폴리코사놀이 600 μL의 반응액에 들어있게 된다. 이 중에서 GC-MS 분석에 1 μL를 주입하 게 되므로 0.025 μg의 폴리코사놀을 취하여 분석하는 것이 며 이 때 얻은 TIC는 Fig. 3과 같았다. Fig. 3과 같이 시 료를 3회 분석한 결과는 폴리코사놀의 함량이 각각 87.7, 86.0, 90.3%이었고 평균값은 88±2.2%로서 표시량의 80- 120% 범위에 들어있음을 확인할 수 있었다. 시료로 사용 한 사탕수수에서 추출한 폴리코사놀은 Fig. 3에서와 같이 octacosanol의 함량이 가장 많았던 반면에 미강 왁스로부터 추출한 폴리코사놀에서는 hexacosanol도 octacosanol의 80% 수준으로 함유되어 있었으며(Ishaka et al., 2014) grain sorghum에는 triacontanol의 함량이 octacosanol과 유 사했던 결과(Hwang et al., 2004)와 peanut의 품종에 따라 서도 폴리코사놀의 함량에 차이가 있다는 보고(Cherif et al., 2010)를 고려해 볼 때 폴리코사놀도 추출에 사용한 원 료 및 품종에 따라 그 조성에 상당한 차이가 있음을 예측 할 수 있었다. 본 연구에서와 같이 폴리코사놀 시료뿐만 아니라 폴리코사놀 수용액의 경우에도 클로로포름으로 폴 리코사놀을 추출하여 유도체화 한 후 SIM mode에서 GCMS로 분석하면 첨가제의 간섭없이 정량한계 범위 이내에 서 실제 함량의 정량분석이 가능함을 알 수 있었다.
요 약
폴리코사놀은 다양한 생리활성을 기반으로 최근 건강기 능식품으로의 상품화가 다양하게 진행되고 있으며 기준 및 규격을 설정하기 위하여 폴리코사놀에 들어 있는 각각의 지방족 알코올을 silyl유도체화 시킨 후 GC-FID로 정량분 석하는 방법이 제안되어 있는 실정이다. 하지만 폴리코사 놀을 수용화하여 사용하는 경우에는 첨가제에 의한 간섭으 로 기존의 방법에 따른 정량분석이 용이하지 않으므로 본 연구에서는 폴리코사놀 시료 및 폴리코사놀 수용액 중 폴 리코사놀의 함량을 GC-MS의 SIM mode에서 정량 분석하 는 방법을 제안하고 그 적합성을 검증하고져 하였다. 제안 된 방법에 따라 폴리코사놀 표준품을 분석한 결과 회수율 은 평균 90.5%, 상대표준편차는 0.48-5.83%, 검출한계는 0.000479-0.001314 μg/μL, 정량한계는 0.001452-0.003983 μg/μL, 정확성은 80.38-108.98%, 정밀성은 0.01-4.88%인 것으로 나타났다. 동일한 방법에 의해 폴리코사놀 3% 시 료 분석한 평균값은 87.43±4.48%이었으며 폴리코사놀 유 화액(5 mg)이 30 mL의 정제수에 혼합되어 있는 수용액을 분석한 평균값은 88±2.2%로서 시료 중 표시량의 80-120% 범위 내에 함유되어 있음을 알 수 있었다. 따라서 본 연구 에서와 같이 폴리코사놀 시료뿐만 아니라 폴리코사놀이 유 화된 수용액의 경우에도 클로로포름으로 폴리코사놀을 추 출하여 TMS유도체화 한 후 GC-MS로 SIM mode에서 분 석하면 정량한계 범위 이내에서 실제 함량의 정량분석이 가능함을 알 수 있었다.







