서 론
기능성 식품을 연구 개발하는 과정에서 우선적으로 고려 해야할 사항은 활성성분을 정량 또는 정성 분석하여 약효 발현물질을 균질화 및 표준화하고 안정성을 확보하여 기능 성소재 속 기능성 물질의 약리 기전을 밝히는 것이다. 생 약소재의 기능성을 가진 물질의 기능성분은 대한약전 (Ministry of Food and Drug Safety, 2014), 대한약전외(생 약) 규격집(Ministry of Food and Drug Safety, 2007) 등에 상세한 기준을 제시하고 있다. 그러나 개발 중인 신물질의 분석법 기준은 그 관리가 아직 부족하고, 회사의 자가 기 준 및 외국 저널에 의존하여 기능성 물질을 분석하고 있 는 실정이기 때문에 기능성 물질 탐색 시 약리성분의 정 확한 함량기준을 파악하기 위해서는 체계적인 분석법 검 증을 통해 식품소재의 생리활성성분 정량이 이루어져야 하겠다.
본 연구의 소재는 산수유로 산수유나무(Cornus offcianalis) 는 층층나무과(Cornaceae)의 낙엽교목으로 주로 중부이남 지역에 분포하고 있다. 산수유는 가을에 성숙한 붉은색 열 매의 씨를 제거한 후 건조한 과육을 산수유라 하며(Chung et al., 1993), 산수유에 대한 연구로는 산수유 열매의 화학 성분과 건조에 따른 과육분리특성(Lee et al., 1992), B16/ F10 melanoma 세포주의 멜라닌 생성에 미치는 영향(Yang et al., 2002), 항암물질의 정제 및 특성(Kim et al., 2004), 영양성분과 항암효과(Lee et al., 2006), 산수유 에탄올 추 출물의 항산화, 항 돌연변이 활성 및 암세포 성장 억제 효 과(Jeon et al., 2008), 추출방법에 따른 항산화 기능분석 (Park et al., 2012)등의 연구가 이루어졌다. 특히 산수유 중 loganin은 인지력 향상(Lee et al., 2008;Kwon et al., 2009) 및 실험동물에서 활성 산소 종을 감소시키는 항산화 효과와 지질대사에도 작용하는 것으로 보고되었다(Yamabe et al., 2010;Han et al., 2012). 따라서 산수유가 다양한 기능성을 가지고 있는 식품 재료로써 가치가 높다고 판단 하였으며 산수유의 항산화 효과가 유효함을 확인하였다.
생약인 산수유는 맛이 시고 성질은 약간 따듯하며 간경, 신경에 좋고, 이뇨작용, 혈압강하작용, 단백질의 소화를 돕 는 작용, 항암 및 항균작용 등도 있는 것으로 보고되어 있 으며(Seo et al., 1999), 산수유성분으로는 gallic acid, malic acid, tartaric acid, ursolic acid와 morroniside, loganin, sweroside와 같은 iridoid 배당체 등이 보고되었다 (Kim, 1999). 이러한 성분의 분석법으로는 플라즈마를 사용 한 column-switching HPLC법(Son et al., 2004), capillary- HPLC법(Song et al., 2006), micellar electrokinetic chromatography (MEKC)법(Zhao et al., 2007), HPLC-DAD법 (Yu et al., 2004;Du et al., 2008;Park et al., 2012), UPLC-MS법(Zhao et al., 2016) 등으로 연구되어 있다. 이러한 산수유에 대한 연구 결과들을 토대로 본 연구는 산수유 생약지표성분으로 loganin을 선정하였고, 기존에 연구된 HPLC를 사용한 loganin 분석법을 참고하여 건강 기능식품 기능성원료 개발을 목적으로 loganin의 분석법을 검증하였고 그 유효성을 체계적으로 확인하였다.
재료 및 방법
본 실험에 사용한 산수유는 한약 규격품으로 2015년 6월 한국생약협회를 통해서 국산 3종(전라남도 구례군, 경상북 도 의성군, 경기도 이천시)과 수입산 1종(중국산)의 씨가 제거된 건조과실을 각 6 kg씩 구입하여 사용하였다. 시료의 균질화를 위하여 600 g 소포장된 각 팩에서 100 g씩 각각 취한다음 한곳에 모아 혼합하였고, 액체 질소를 이용하여 급 냉동시켜 분쇄하였다. 분쇄한 각 시료는 100 g씩 소포장 후 -70°C 냉동고에 보관하며 실험에 사용하였다.
본 실험에서 사용된 loganin 표준품은 Sigma Aldrich Co. (St. Louis, MO, USA)의 것을 사용하였다. 추출용매와 표준품 제조 및 이동상에 사용한 용매는 HPLC용 용매를 사용하였다. 검량선 작성을 위해 표준품은 methanol에 녹 여 1 mg/mL이 되도록 고농도 표준용액을 제조한 후 단계 적으로 희석하여 11개 농도(0.03, 0.06, 0.125, 0.25, 0.5, 1, 5, 10, 50, 100, 200 μg/mL)로 조제하였다. Loganin 함량을 구하기 위하여 표준용액의 크로마토그램에서 얻은 피크의 농도별 면적에 대하여 검량선을 작성하였다.
산수유의 loganin 추출 및 분석은 Du et al. (2008)과 Park et al. (2012)의 방법을 참고하여 분석 하였다. loganin 추출은 구례산 산수유를 이용하여 각 조건별로 3반복 이상 최적 추출조건 시험을 하였다. 최적 추출조건은 loganin 추 출에 영향을 미칠 것이라 생각되는 에탄올 농도(0-100%), 추출 용매량(25-200 mL) 및 추출시간(15-120 min)의 조건 을 달리하여 추출한 후 loganin함량을 분석하여 결정하였 다. 즉 산수유 건조분말 0.5 g을 정확히 칭량한 후 정해진 조건에 의해 초음파 추출(WUC-A22H, DAIHAN Scientific, Wonju, Korea)한 후 여과 및 정용하여 분석시료로 사용하 였다. 최종적으로 확인된 80% 에탄올, 50 mL, 초음파 추 출 30 min의 추출조건으로 3회 반복 시험하여 추출액을 만 들고 0.45 μm filter로 vial에 여과 후 HPLC/DAD로 분석 하였다. 함량은 표준용액 크로마토그램의 피크 면적을 통 하여 작성된 검량선에 의해 산수유 중 loganin의 농도를 산출하였다.
HPLC 분석조건은 Table 1에 요약하였다. 분석 컬럼은 X-Bridge C18 (4.6×250 mm, 3.5 μm, Waters corporations, Millford, MA, USA)을 사용하였고, HPLC 장비는 Alliance (Waters e2695), UV/VIS detector (Waters 2996)을 사용하 였다. 데이터의 수집 및 처리는 Empower software program (Waters corporations)을 사용하였다. 이동상은 HPLC용 용 매를 사용하였고 A용매는 water, B용매는 acetonitrile을 사 용하였으며 사용 전 필터로 여과 후 탈기하여 사용하였다. 분석칼럼 유속은 0.6 mL/min, 분석시간은 40분, 이동상 gradient 조건은 Table 1과 같다. UV 분석 파장은 238 nm 에서 측정하였으며, 시료 시험용액은 20 μL를 주입하였다.
산수유 loganin함량 분석법의 검증은 대한민국약전 제 11개정(2014)과 AOAC 가이드라인(2002)에 기초하여 수행 되었다.
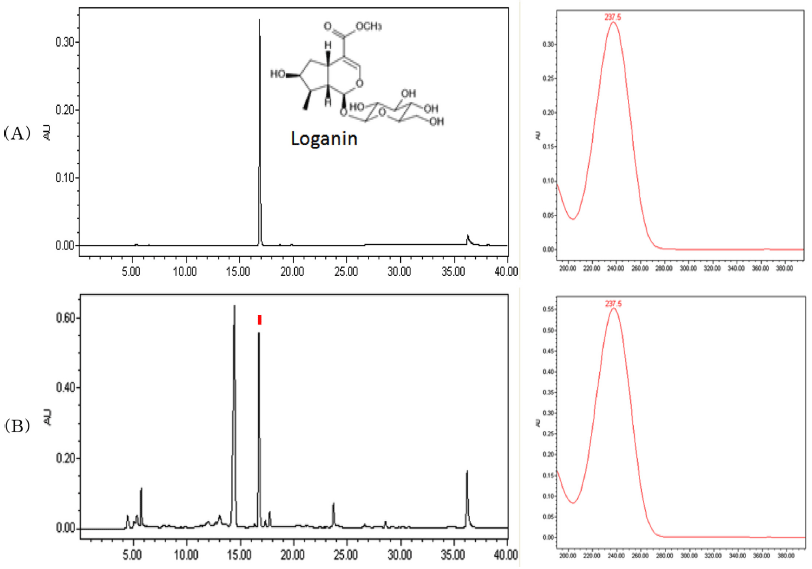
특이성(specificity)의 확인은 loganin 표준용액과 전 처리 한 구례산 산수유추출시험액을 HPLC로 분석하여 크로마 토그램상의 retention time과 UV spectrum을 비교하여 확 인하였다.
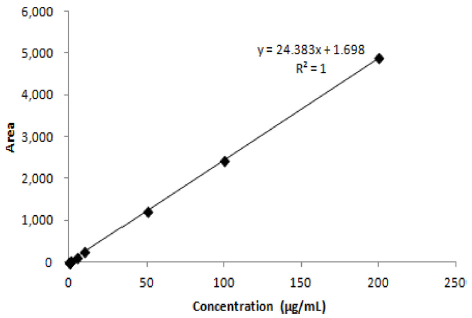
직선(linearity)은 loganin 표준용액을 1 mg/mL 농도로 제 조하고, methanol로 0.03-200 μg/mL 농도(11개 농도)로 3회 이상 반복 단계 희석 및 분석 후 농도에 대한 면적에 대 하여 검량선을 작성한 후 평균값을 이용하여 검량선을 작 성하여 직선성을 확인하였다.
검출한계(LOD, limit of detection)와 정량한계(LOQ, limit of quantitation)는 분석물질인 loganin의 검출 및 정량 이 가능한 최저 농도를 확인하기 위한 검출한계와 정량한 계를 HPLC/DAD로 검출해 얻은 바탕시험용액 크로마토그 램의 신호잡음비(signal-to-noise)값의 평균값과 표준 편차를 구하고, 표준편차에 각각 3과 10을 곱한 값을 평균값에 더 하여 검출한계와 정량한계를 구하였다.
산수유 loganin 성분 분석의 정확성을 위하여 표준품을 3가지 농도(50, 100, 200 μg/mL)로 제조하고, 시료 추출 시 2회 spiking하여 분석 후 시료에 대한 표준품의 농도별(μg/ g) 회수율(%)을 구하여 정확성을 시험하였다.
정밀성 검증은 구례산 산수유를 quality control 물질로 이용하여 하루에 독립적으로 5회 반복 실험하는 일내분석 을 수행하여 반복성을 계산하였고, 4일 동안 하루에 1회씩 2반복 이상 실험하여 이들 간 결과의 일치성을 계산하여 재현성을 시험하였다.
결과 및 고찰
특이성이란 공존이 예측되는 불순물, 간섭물 및 다른 구 성성분들의 존재 시 분석하고자 하는 목적성분을 정확하고 특이적으로 측정할 수 있는지 확인하는 것으로(AOAC, 2002), loganin 표준용액과 구례산 산수유추출액의 HPLC 크로마토그램을 비교하여 loganin peak가 분리되는지 확인 한 결과 Fig. 1과 같이 다른 물질과 간섭 없이 성분이 분 리 되었으며 표준용액과 산수유추출액의 peak 유지시간이 16.3분으로 일치하였다. 또한 표준용액과 시료추출액의 UV spectrum도 정확하게 일치 하는 것을 확인하였다(Fig. 1).
직선성의 성립은 검체 중의 분석대상물(지표성분)의 양 또는 농도에 대하여 측정반응이 직선적인 비례관계를 보이 는 정도로 기대하는 농도 범위 80-120%를 포괄하는 범위 를 검토하며, 0을 제외한 7개 이상의 농도 수준의 표준물 을 각 수준에서 3회 이상 반복 측정한 검량선(calibration curve) 작성 후 측정 평균값으로 얻어진 관계식으로 확인 된다(AOAC, 2002). Loganin 표준용액을 0.03-200 μg/mL의 11개 농도 수준으로 3회 반복 단계 희석 후 HPLC로 분석 하여 얻은 평균값으로 검량선을 작성하였으며 Fig. 2와 같 은 검량선을 나타내었다. 검량선의 상관계수(R2)는 1로 우 수한 직선성을 보였으며, 검출한계는 0.007 μg/mL, 정량한 계는 0.026 μg/mL 수준으로 나타났다(Table 2). 건조된 동 백꽃 및 금은화를 시료로 loganin을 포함한 iridoid 배당체 성분을 분석한 Song et al. (2006)의 연구에서는 검출한계 가 0.0015 μg/mL로 본 연구 보다 낮은 수준을 보였는데 이는 고감도 검출기인 mass spectrometric 검출기와 함께 모세관 고속액체크로마토그래피를 이용하였기 때문으로 사 료된다. 산수유를 시료로 loganin을 포함한 6개 성분을 고 속액체크로마토그래피를 이용하여 동시 분석한 Du et al. (2008)의 연구에서는 검출한계가 0.11-1.69 μg/mL, 정량한 계가 1.48-16.60 μg/mL의 범위를 보였는데 본 연구의 검출 및 정량 한계 값이 더 미량임을 보여 본 연구의 loganin 분석법이 미량농도까지 분석이 가능함을 입증할 수 있다. 또한 산수유 시료의 표준화를 위해 선정된 지표성분의 분 석을 위한 검출한계와 정량한계를 검증한 것으로 기능성 식품 연구에서의 활용성이 높을 것으로 사료된다.
| Regression equation | Correlation coefficient (R2) | LOD | LOQ | |||
|---|---|---|---|---|---|---|
|
|
|
|||||
| μg/mL | ng/injection volume (20 μL) | μg/mL | ng/injection volume (20 μL) | |||
|
|
||||||
| y = 24.383x + 1.698 | 1.000 | 0.007 | 0.140 | 0.026 | 0.520 | |
분석과정의 정확성은 기존에 사용하는 정확성이 입증된 분석법에 의한 분석 값과 근적외부스펙트럼 측정법에 의해 예상한 값이 유사하다는 것을 표현하는 척도이다(Ministry of Food and Drug Safety, 2014). 따라서 본 연구의 정확 성 결과는 Table 3과 같이 loganin의 회수율(%)로 확인하 였다. RSD (Relative standard derivation)는 5% 이내였으 며, 농도별로 50 μg/g에서는 105.45%, 100 μg/g에서는 96.15%, 200 μg/g에서는 95.14%의 회수율을 보였는데 이 는 50 μg/g의 낮은 농도에서도 100%에 가까운 회수율을 보여 줌으로서 본 분석방법의 정확성을 검증하였다. 또한 loganin을 포함한 4개 성분을 동시 분석한 Zhao et al. (2007)의 연구에서 시료추출액에 알고 있는 농도의 표준품 을 spiking한 회수율이 101.8%로 본연구와 유사하게 100% 에 가까운 우수한 회수율을 보임으로 정확성을 입증 할 수 있었다.
| Loganin concentration (μg/g) | Recovery (%) | ||
|---|---|---|---|
|
|
|||
| Mean | SD1) | RSD (%)2) | |
|
|
|||
| 200 | 95.14 | 1.01 | 1.06 |
| 100 | 96.15 | 1.04 | 1.08 |
| 50 | 105.45 | 4.67 | 4.43 |
정밀성이란 제시된 분석조건에서 같은 검체에 대해 일련 의 연속적인 분석으로 얻은 결과간의 유사함을 의미하는 것으로(Ministry of Food and Drug Safety, 2014), 본 연구 에서는 Table 4와 같이 intra-및 inter-day분석에서 RSD (%) 값이 3% 이내로 AOAC 가이드라인(2002)이 요구하는 5% 이하의 값을 보여 일내와 일간의 반복성과 재현성이 우수함을 보여주었다. Du et al. (2008)의 연구에서도 intra- 및 inter-day RSD값은 각 2.53%와 3.17%로 본 분석 방법의 결과와 유사함을 확인하였다.
| Cornus officinalis | Loganin (mg/mL) | |||
|---|---|---|---|---|
|
|
||||
| Intra-day3) | Inter-day4) | |||
|
|
||||
| Mean±SD1) | 8.04±0.14 | 7.79±0.18 | ||
| RSD (%)2) | 1.77 | 2.33 | ||
본 연구의 loganin 분석방법의 검증과정을 통하여 HPLC/DAD 분석법이 산수유 중 존재하는 중요한 약리적 성분의 표준화를 위한 정량에 이용될 수 있는 충분한 감도, 특이성, 직선성, 정확성 및 정밀성을 갖고 있음을 알 수 있었다. 또한 검증된 분석방법으로 재배 지역별 산수유의 loganin 함량을 측정한 결과 3.41-7.81 mg/g 범위의 함량을 보였다. 이는 중국산 산수유 보다 국내산 2종에서 더 높은 loganin 함량분석 결과를 보여줌으로서 본 연구의 loganin 분석법 검증을 통해 loganin 함량이 높은 국내산 산수유의 기능성 원료로서 산업적 가치가 우수함을 확인 하였다.
| Cultivation regions | Loganin content (mg/g)1) |
|---|---|
|
|
|
| Gurye | 7.81±0.01a |
| Uiseong | 3.41±0.05d |
| Icheon | 7.42±0.10b |
| China | 6.52±0.07c |
요 약
본 연구는 다양한 활성을 가진 산수유를 건강기능식품 기능성 원료를 개발하기 위하여 지표성분으로 loganin을 선정하였다. 분석법 검증 지표로는 특이성, 직선성, 검출 및 정량한계 정확성, 정밀성을 HPLC/DAD분석에 의해 검 증하였다. 특이성은 표준용액과 산수유 추출액의 크로마토 그램 비교 결과 peak유지시간이 16.3분으로 일치하였으며 표준용액과 시료추출액의 UV spectrum도 정확하게 일치 하는 것을 확인하였다. 직선성은 검량선의 상관계수 (R2)는 1로 우수한 직선성을 보였으며, 검출한계는 0.007 μg/mL, 정량한계는 0.026 μg/mL 수준으로 나타났다. 정확성은 loganin의 회수율로 확인하였으며, RSD (%)는 5% 이내였고 농도별로 50 μg/g에서는 105.45%, 100 μg/g에서는 96.15%, 200 μg/g에서는 95.14%의 회수율(%)을 보였다. 정밀성은 intra- 및 inter-day 분석에서 RSD값이 3% 이내로 일내와 일간의 반복성과 재현성이 우수함을 확인하였다. 검증된 분석방법으로 재배 지역별 산수유의 Loganin 함량을 측정 한 결과 3.41-7.81 mg/g 범위의 함량을 보였다. Loganin 분 석방법의 검증과정을 통한 HPLC/DAD분석법이 산수유 중 존재하는 중요한 약리적 성분의 표준화를 위한 정량에 이 용될 수 있는 충분한 감도, 특이성, 직선성, 정확성 및 정 밀성을 갖고 있음을 알 수 있었다. Loganin 분석법 검증을 통해 loganin 함량이 높은 국내산 산수유의 기능성 원료로 서 산업적 가치가 우수함을 확인 하였다.