서 론
커피는 세계적으로 가장 많이 음용되는 기호성 음료로 아라비카(Coffea arabica L.)와 로부스타(Coffea canephora L.)의 두가지 품종이 상업적으로 널리 활용되고 있다(Lee et al., 2013). 아라비카종이 로부스타종보다 더 깊은 향과 풍부한 맛을 가지고 있기 때문에 아라비카종은 원두커피 재료로, 로부스타종은 인스턴트커피 재료로 많이 사용된다. 커피의 생리활성 성분으로는 각성 작용을 나타내는 카페인 이 가장 잘 알려져 있고, 카테킨과 안토시아닌 등의 플라 보노이드와 다양한 종류의 폴리페놀 화합물이 커피의 유용 성분으로 보고되어 있다(Kim & Han, 2009). 커피는 항고 혈압(Rufian-Henares & Morales, 2007), 항균(Almeida et al., 2006) 및 항산화(Castillo et al., 2002) 활성을 가지고 있고, 특히 커피에는 다른 식품에 비해 항산화 물질의 함 량이 높아 세포손상 및 산화를 유발하는 자유라디칼을 효 과적으로 소거한다고 알려져 있다(Suh et al., 2014). 커피 의 항산화 물질로는 폴리페놀, 토코페롤 및 커피를 볶는 과정에서 비효소적 갈변 반응으로 생성되는 갈색물질 등이 알려져 있으나, 토코페롤은 물에 잘 용출되지 않기 때문에 음용하는 커피 추출액의 항산화 활성은 주로 페놀성 화합 물 및 갈색 물질에 기인한다(Rhi & Shin, 1993).
이러한 커피를 음용하기 위해서는 배전(roasting) 과정이 필수적이고, 커피의 주된 맛과 향은 배전과정을 거쳐 생성 된다. 볶은 커피에는 10-17%의 카라멜화된 당, 약 4.5%의 클로로젠산(chlorogenic acid), 약 2%의 유기산, 1-2%의 환 원당, 1-2%의 단백질, 약 3%의 무기질, 1-2%의 카페인, 약 1%의 trigonelline 및 약 0.35%의 휘발성 물질이 함유 되어 있어(Nam & Kang, 2015), 커피의 생리 활성은 물론 커피 고유의 색, 맛과 향을 나타낸다(Reneccius, 1995). 커피의 배전 강도에 따라 Maillard 반응, Strecker 분해 및 당분해 반응의 정도가 달라져 커피의 색, 맛, 향의 차이가 발생하고, 커피를 배전함으로써 당과 아미노산의 소실, 클 로로젠산과 trigonelline 등의 분해에 의해 약 800여 가지 이상의 새로운 화학물질이 생성된다(Lee et al., 2013). 또 한, 배전된 커피의 추출과정에서 용매로 사용하는 물의 상 태, 온도와 추출시간이 음용하는 커피의 맛과 향에 영향을 미친다고 알려져 있어, 커피의 추출 방식은 향미를 유지시 키면서 이취를 감소시키는 방향으로 개선되고 있다(Eun et al., 2014).
본 연구에서는 커피의 배전 강도와 추출시간이 커피 추 출액의 갈색도, 폴리페놀 함량, 유리라디칼 소거능 및 카페 인 함량에 미치는 영향을 확인함으로써 커피의 생리활성은 높이면서 관능적으로도 우수한 커피의 배전 강도와 추출 시간을 제시하고자 하였다.
재료 및 방법
본 실험에 사용한 커피 원두는 아라비카(Coffea arabica L.) 품종의 브라질산 Brazil santos fc cerrado 커피(GSC International, Seoul, Korea)를 사용하였다. 배전은 열풍식 배전기(RFB-1, Esso Coffee, Daegu, Korea)를 사용하였다. 생두를 배전기의 내부온도 185°C에서 투입한 후 중배전 (medium roasting)은 5분 10초 동안 수행하여 내부온도 245°C에서 배전을 마쳤고, 강배전(dark roasting)은 6분 동 안 수행하여 내부온도 252°C에서 배전을 마쳤다. 배전된 커피는 실온에서 충분히 냉각시킨 후 폴리에틸렌으로 내부 를 코팅한 알루미늄팩에 넣어 -20°C에서 냉동 보관하였다. 냉동 커피는 상온에서 3시간 해동한 후 커피 그라인더 (M20.07, Petra Electric, Metzingen, Germany)를 사용하여 315-500 μm 정도의 입자 크기로 분쇄하였다. 커피 추출은 침지식 추출방법을 사용하였다. 중배전과 강배전된 커피 분말 시료 10 g을 티백에 넣어 밀봉한 후 온도가 90°C로 유지되는 증류수 200 mL에 넣어 5, 10, 15, 20, 30, 60분 간 각각 추출한 후 티백을 제거하여 추출 시간에 따른 커 피 추출액을 얻었다.
커피 추출액을 Whatmann No.2 여과지로 여과하고 동결 건조기에서 건조한 후 고형물의 무게를 측정하여 추출액의 고형분 함량을 구하였다. 또한, 커피 추출물의 카페인 함량 은 high performance liquid chromatography (HPLC) 방법 을 사용하였다. 분석은 2695 Separation module과 996 photodiode array로 구성된 HPLC 시스템(Waters Alliance, Waters Corporation, Milford, MA, USA)을 사용하였다. 이 때 컬럼은 Eclipse XDB-C18 (5 μm, 150×4.6 mm), 컬럼 온도는 35°C, 이동상은 0.3% 초산수용액-메탄올(7:3) 혼합 액, 유속은 0.8 mL/min, detector는 274 nm, 투입 부피는 10 μL로 분석하였다. 카페인 함량은 3,7-dihydro-1,3,7- trimethyl-1H-purine-2,6-dione (caffeine)을 표준물질로 사용 하여 계산하였다.
커피 추출물의 갈색도는 Whatmann No.2 여과지로 여과 한 커피 추출액을 증류수에 100배 희석한 후 분광광도계 (UV-1201, Shimadzu Corporation, Kyoto, Japan)를 사용하 여 420 nm의 흡광도로 나타내었다. 커피 추출물의 총 페 놀화합물 함량 측정은 변형된 Folin-Ciocalteu 방법을 이용 하였다(Folin & Denis, 1912). 커피 추출물을 증류수에 50배 희석한 시료 1 mL과 10% Folin-Ciocalteu 용액 1 mL 을 혼합하고 실온에서 5분간 방치한 후 1 mL의 6% Na2CO3 용액을 가하여 실온에서 1시간 반응시켜 분광광도 계(UV-1201, Shimadzu Corporation, Kyoto, Japan)로 725 nm의 흡광도를 측정하였다. 표준물질로 클로로젠산을 사용하여 총 페놀화합물 함량을 계산하였고, 추출물 mL당 μg chlorogenic acid equivalent (CAE)로 나타내었다(Kim et al., 2015). 유리라디칼 소거활성은 1,1-diphenyl-2- picrylhydrazyl (DPPH)를 사용하여 변형된 Blois 방법으로 측정하였다(Blois, 1958). 커피 추출물을 50배 희석한 시료 0.2 mL과 에탄올 2 mL을 혼합하고 0.2 mM DPPH 용액 0.8 mL을 넣은 후 실온에서 30분간 반응시켜 분광광도계 (UV-1201, Shimadzu Corporation, Kyoto, Japan)로 517 nm 의 흡광도를 측정하였다. 대조구는 시료 대신에 증류수를 가하였고, 유리라디칼 소거능(%)은 (1−시료의 흡광도/대조 구의 흡광도)×100에 의해 계산하였다.
결과 및 고찰
중배전과 강배전된 커피 분말을 열수로 추출하여 시간에 따른 고형분 및 카페인 함량을 측정하였다. 생두는 열풍식 로스트기로 185°C에서 시작하여 시간을 증가시키면서 배전 하였는데 배전 정도는 Specialty Coffee Association of America (SCAA)의 분류기준인 Agtron Roast Color Classification System에 따라 원두의 색으로 확인하였다 (Farah, 2012).
Fig. 1A에서 보듯이 중배전과 강배전된 커피를 열수 추 출하였을 경우, 중배전된 커피는 15분까지, 강배전된 커피 는 20분까지 고형분이 급격히 증가하였으나 그 이후부터는 소폭의 상승만 보여주었다. 90°C의 물에서 30분 동안 충분 히 추출하였을 경우, 중배전은 고형분 함량이 1.60±0.100% 이었고, 강배전은 1.56±0.230%로 유의적인 차이를 나타내 지 않았다. 고온에서 단시간 배전한 커피가 저온에서 장시 간 배전한 커피에 비해 수용성 고형분과 휘발성 물질이 더 많이 생성된다고 보고(Toci & Farah, 2008)되었지만, 본 연구에서의 강배전(185°C→252°C, 6분)은 열풍식 로스터기 를 사용하여 중배전(185°C→245°C, 5.17분)과 같은 온도에 서 시작하여 배전 시간을 늘린 것이기 때문에 고형분 추출 에 유의미한 차이는 나타나지 않았다.
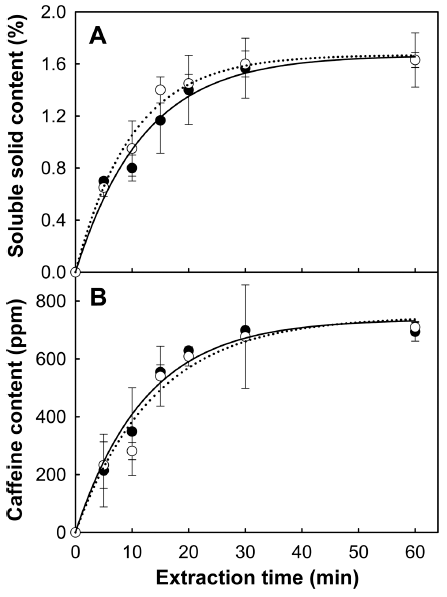
Fig. 1B에서 보듯이 중배전과 강배전된 커피를 열수 추 출하였을 경우, 둘다 15분까지는 카페인 함량이 급격히 증 가하였으나 그 이후부터는 소폭의 상승만 보여주었다. 90°C의 물에서 30분 동안 충분히 추출 시 중배전은 카페 인 함량이 676.8±179.02 ppm이었고, 강배전은 698.6±6.56 ppm으로 유의적인 차이가 없었다. 이러한 결과는 커피를 매우 높은 온도에서 배전하지 않은 한 카페인의 손실이 매 우 적으며 배전 강도에 따라 거의 변화를 보이지 않는다는 보고와 일치하였다(Kim & Park, 2006). 카페인은 세포 내 부로부터의 확산에 의해서 추출이 이루어지고, 뜨거운 물 에 대한 용해도가 높기 때문에 배전 정도에 크게 상관없이 90°C의 물에 잘 용출된 것으로 보인다(Kim et al., 2007).
중배전과 강배전한 커피 분말의 추출 시간에 따른 갈색 물질의 함량을 420 nm에서 흡광도를 측정하여 갈색도로 나타내었다. Fig. 2A에서 보듯이 중배전된 커피는 열수 추 출에서 15분까지는 갈색도가 급격히 증가하였으나 그 이후 부터는 거의 증가하지 않았다. 반면에 강배전된 커피는 20 분까지 갈색도가 크게 증가하였다. 90°C의 물에서 30분 동 안 충분히 추출하였을 경우, 중배전된 커피의 갈색도는 0.60±0.034이었고, 강배전된 커피는 0.84±0.071로 나타나 강배전 커피의 갈색도가 40% 정도 높았다. 강배전된 커피 는 볶음 강도가 세고 열처리 시간이 상대적으로 길기 때문 에 갈색 물질이 많이 생성됨으로써 열수 추출 시 중배전된 커피보다 갈색도가 유의적으로 높게 나타났다(p<0.05). 커 피의 갈색 물질은 원두에 함유되어 있는 설탕의 카라멜 반 응, 아미노기를 가진 물질과 환원당 사이의 amino-carbonyl 반응에 의해 생성되는 물질, 클로로젠산의 분해산물 및 trigonelline 반응에 의해 생성된다(Lee et al., 2013;Eun et al., 2014;Liang & Kitts, 2014). 배전 과정에서 aminocarbonyl 반응에 의해 생성되는 커피 멜라노이딘은 갈색의 고분자 화합물로서 항산화 활성을 가진다(Borrelli et al., 2002). 또한, 볶은 커피의 갈색 물질 중에는 설탕이 열분해 되면서 클로로젠산과 반응하여 생성된 glycealdehyde 및 glycolaldehyde 등의 갈색 물질이 항산화 활성과 상관관계 가 있다(Rhi & Shin, 1993).
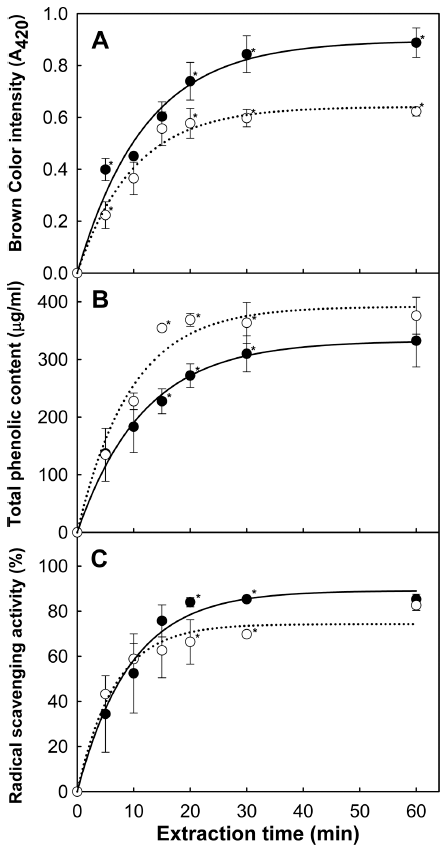
중배전과 강배전한 커피 분말의 추출 시간에 따른 총 페 놀화합물 함량을 측정하여 Fig. 2B에 나타내었다. 중배전 된 커피는 열수 추출에서 15분까지는 총 페놀화합물 함량 이 급격히 증가하였으나 그 이후부터는 거의 증가하지 않 았다. 반면에 강배전된 커피는 20분까지 총 페놀화합물 함 량이 서서히 증가하였다. 90°C의 물에서 30분 동안 충분히 추출하였을 경우, 중배전된 커피의 총 페놀화합물 함량은 363.4±35.56 μg CAE/mL이었고, 강배전된 커피는 309.8± 31.41 μg CAE/mL로 나타나 중배전 커피의 총 페놀화합물 함량이 17.3% 높았다. 즉, 갈색도와는 반대로 중배전된 커 피의 충 페놀화합물 함량이 강배전된 커피보다 유의적으로 높게 나타났다(p<0.05). 이는 커피의 페놀성 화합물의 열분 해에 기인한 것이다. 커피의 페놀성 화합물은 열에 의해 분해되기 때문에 배전 강도가 셀수록 시간이 길수록 그 함 량이 감소한다고 일반적으로 알려져 있다(Kim & Han, 2009). 특히 클로로젠산은 배전 과정 중에 열에 의해 쉽게 분해되어 총 페놀화합물 함량 감소에 크게 기여한다(Farah & Donangelo, 2006). 또한 커피의 주요 phenolic acid인 caffeoylquinic acids, p-coumaroylquinic acids, feruloylquinic acids 등도 배전 과정에서 쉽게 분해된다(Farah et al., 2005).
중배전과 강배전한 커피 분말의 추출 시간에 따른 유리 라디칼 소거능을 측정하여 Fig. 2C에 나타내었다. 중배전 된 커피는 열수 추출에서 10분까지는 유리라디칼 소거활성 이 급격히 증가하였으나 그 이후부터는 거의 변화가 없었 다. 강배전된 커피는 20분까지 유리라디칼 소거활성이 크 게 증가하였으나 그 이후에는 거의 변화가 없었다. 90°C의 물에서 30분 동안 충분히 추출하였을 경우, 중배전된 커피 추출물은 DPPH 유리라디칼을 69.8±1.26% 소거하였고, 강 배전된 커피는 85.3±1.21% 소거하였다. 갈색도의 경우와 마찬가지로 강배전된 커피의 유리라디칼 소거활성이 중배 전된 커피보다 유의적으로 높게 나타났다(p<0.05). 배전된 커피의 항산화 활성은 커피에 들어있는 클로로젠산 등의 폴리페놀 성분과 배전 과정 중 amino-carbonyl 반응에 의 해 생성되는 갈색 물질에 의한 것으로 보고된 바 있다(Lee et al., 2013;Eun et al., 2014;Liang & Kitts, 2014). 특히 amino-carbonyl 반응의 갈색 생성물인 멜라노이딘이 강한 항산화 능력을 보유하고 있고(Borrelli et al., 2002), 멜라노 이딘의 항산화 효과는 라디칼에 전자공여에 의한 환원작용 과 금속 킬레이트 작용에 기인하는 것으로 알려져 있다 (Morales & Jimenez-Perez, 2004;Morales et al., 2005).
중배전과 강배전한 커피 추출물의 관능 평가 결과(데이 터 생략), 중배전과 강배전 모두에서 추출 시간이 길수록 향, 쓴맛, 신맛, 양질감은 강하게 느껴졌으며, 단맛은 감소 하였다. 중배전과 강배전한 커피 모두 90°C의 물에서 15분 추출 시 선호도가 높았고, 두 커피간의 유의적인 차이는 없었다. 일반적으로 배전 강도가 셀수록 쓴맛과 탄맛이 강 해지고 단맛과 신맛은 감소하는 반면에 입안에 커피를 머 금었을 때 느껴지는 양질감은 강배전한 커피가 우수한 것 으로 보고된 바 있다(Lee et al., 2007;Lee et al., 2013).
중배전과 강배전한 커피를 90°C의 물에서 15분 동안 추 출하여 얻어진 갈색도, 총 페놀성 화합물 함량 및 유리라 디칼 소거능을 Table 1에 나타내었다. 중배전한 커피는 상 대적으로 낮은 열처리로 인해 폴리페놀의 성분의 파괴는 적은 반면 항산화력을 갖는 갈색 물질은 적게 생성되었다 (p<0.05). 강배전한 커피는 장시간의 열처리로 인해 폴리페 놀의 파괴가 일어나 그 함량이 낮아진 것에 비해 갈색 물 질이 더 많이 생성됨으로써 유리라디칼 소거능이 높게 유 지되었다. 즉, 15분 추출 시 중배전과 강배전된 커피는 갈 색 물질과 페놀성 화합물 함량의 상호 보완으로 인해 유리 라디칼 소거활성에 큰 차이가 없었다. 커피의 항산화 활성 은 커피 추출물의 페놀성 화합물뿐만 아니라 갈색 물질 함 량과 정비례한다는 알려져 있다(Suh et al., 2014). 또한 배 전 과정에서 클로로젠산의 감소로 인해 총 페놀성 화합물 함량이 감소하지만 amino-carbonyl 반응에 의한 항산화능 을 가진 화합물의 생성으로 인해 볶은 커피의 항산화 활성 은 그대로 유지되거나 오히려 증가한다고 보고된 바 있어 본 연구의 결과와 일치하였다(Nicoli et al., 1997).
| Roasting intensity | Total phenolics (μg CAE/mL) | Brown color intensity (A420) | Radical scavenging activity (%) | |
|---|---|---|---|---|
|
|
||||
| Medium | 311.3±2.331),* | 0.50±0.065 | * 66.5±12.09 | |
| Dark | 238.5±21.66* | 0.64±0.057* | 71.0±7.07 | |
이상의 결과에서 중배전과 강배전한 커피 모두 90°C의 물에서 20분 추출까지는 고형분, 카페인, 갈색물질 및 페 놀성 화합물 함량이 급격하게 증가하였으나 그 이후에는 증가세가 미미하였다. 중배전한 커피는 페놀성 화합물의 함량이 상대적으로 높은 반면에 갈색 물질의 생성 정도는 낮았다. 강배전한 커피는 장시간의 열처리로 인해 폴리페 놀의 파괴가 일어나 페놀성 화합물의 함량이 낮게 나타났 지만 갈색 물질이 많이 생성됨으로써 항산화 활성이 높게 유지되었다. 본 연구에서 페놀성 화합물과 갈색 물질의 함 량은 커피의 배전 강도에 따라 상호보완적으로 변화하여 항산화 활성에 영향을 주었다.
요 약
커피 원두의 배전 강도와 추출 시간이 커피 추출물의 고 형분, 카페인 및 페놀성 화합물 함량과 갈색 물질 생성, 유리라디칼 소거활성에 미치는 영향을 확인하였다. 커피 생두는 열풍식 로스터기를 이용하여 중배전(185°C→245°C, 5.17분)과 강배전(185°C→252°C, 6분)하였고, 90°C의 물로 시간에 따라 추출하였다. 중배전과 강배전한 커피 모두 20분 추출까지는 고형분, 카페인, 갈색물질 및 페놀성 화합 물 함량이 급격하게 증가하였으나 그 이후에는 증가세가 미미하였다. 중배전과 강배전한 커피에서 고형분과 카페인 함량은 거의 차이가 없었다. 중배전한 커피는 낮은 열처리 로 인해 폴리페놀의 성분의 파괴는 적은 반면 항산화력을 갖는 갈색 물질은 적게 생성되었다. 강배전한 커피는 폴리 페놀의 열분해가 일어나 함량이 낮아진 것에 비해 열에 의 해 갈색 물질이 더 많이 생성됨으로써 유리라디칼 소거능 이 높게 유지되었다. 커피의 유리라디칼 소거활성은 페놀 성 화합물 함량뿐만 아니라 갈색 물질의 함량에도 상관 관 계를 가진다는 것을 보여주었다.







