Research Note
홍삼정과 제조 부산물 이용에 관한 연구: 반응표면분석을 이용한 총 진세노사이드 추출조건의 최적화
이의석, 류관모, 김선형, 이가순1, 박수진2, 전병선3, 박종태, 홍순택*
A Study on the Utilization of By-products from Honeyed Red Ginseng: Optimization of Total Ginsenoside Extraction Using Response Surface Methodology
Eui-Seok Lee, Kwan-Mo You, Sun-Young Kim, Ka-Soon Lee1, Soo-Jin Park2, Byeong-Seon Jeon3, Jong-Tae Park, Soon-Taek Hong*
Dept. of Food Science and Technology, College of Agriculture and Life Science Chungnam National University
1Ginseng and Medicinal Plant Research Institute, CNARES
2Dept. of Oriental Medical Food and Nutrition, Semyung University
3R&D Reasearch Center, Daedong Korea Ginseng Co. Ltd.
*Corresponding author: Soon-Taek Hong, Dept. of Food Science and Technology, College of Agriculture and Life Science Chungnam National University, Daejeon 34134, Korea +82-42-821-6727; +82-42-821-8900
hongst@cnu.ac.kr
© Korean Society for Food Engineering. All rights reserved.
Received: Oct 3, 2016; Revised: Nov 14, 2016; Accepted: Dec 7, 2016
Abstract
This study was carried out to extract ginsenosides in by-products from honeyed red ginseng. Response surface methodology (RSM) was used to optimize the extraction conditions. Based on D-optimal design, independent variables were ethanol (extraction solvent) concentration (30-90%, v/v), extraction temperature (25-70°C), and extraction time (5-11 h). Extraction yield (Y1) and total ginsenosides (Y2) in the extract were analyzed as dependent variables. Results found that extraction yield increased with increasing extraction temperature and time, whereas it was decreased with increasing ethanol concentration. Similar trends were found for the content of ginsenosides in the extracts, except for ethanol concentration, which was increased with increasing ethanol concentration. Regression equations derived from RSM were suggested to coincide well with the results from the experiments. The optimal extraction conditions for extraction yield and total ginsenosides were an extraction temperature of 56.94°C, ethanol concentration of 57.90%, and extraction time of 11 h. Under these conditions, extraction yield and total ginsenoside contents were predicted to be 84.52% and 9.54 mg/g, respectively.
Keywords: red ginseng concentrates; ethanol extraction; honeyed red ginseng by-products; response surface methodology
서 론
최근에 생활수준 향상과 더불어 평균 수명연장에 따라 삶 의 질에 대한 의식이 높아지면서 웰빙(Well-being), 로하스 (LOHAS, Lifestyles Of Health And Sustainability), 셀프 메디 케이션(Self-Medication: 스스로 자신의 건강을 챙기는 일) 등 과 같은 건강 지향적 사회 트랜드가 형성되고 있다. 또한 식 생활의 서구화에 따른 생활 습관병(고혈압, 당뇨병, 비만 등)의 증가로 건강기능식품에 대한 관심과 그 수요가 늘어 나고 있으며(The Foundation of Agriculture Technology Commercialization and Transfer, 2014), 이에 따라 국내 건강 기능식품 시장 규모도 꾸준한 성장을 해 오고 있다(국내 건 강기능식품 시장 생산량: 1조 3,682억원(2011년)→ 1조 8,230억원(2015년), 24.95% 증가). 이들 중 홍삼관련 제품 이 6,943억원(2015년)으로 국내 건강기능식품 생산량의 38%를 차지하고 있으며, 지속적으로 홍삼에 대한 소비자의 관심이 높아지고 있다(Ministry of Food and Drug Safety, 2016).
홍삼은 가공하지 않은 수삼을 증숙·건조과정을 거쳐 제조 된 것으로 가공과정 중 유용 성분의 변화, 즉 ginsenosides, panaxytriols, ananxadiols, 산성다당체 및 maltol 등이 증가하 여 면역기능조절작용(Jang et al., 1994), 항산화능(Choi et al., 2004), 항돌연변이원 및 아질산 소거 작용(Lee et al., 2001), 항스트레스 및 항피로 작용(Kaku et al., 1975; Satio & Bao, 1984), 항당뇨(Cho et al., 2006), 항위궤양 및 항염증 작용 (Matsuda et al., 1990), 간기능 항진효능(Park et al., 1996) 등 유용한 생리기능성을 나타내는 것으로 보고되고 있다. 상기 유효성분 중 진세노사이드에 대한 연구가 활발히 진행되었 으며 이 중 홍삼의 부위별 진세노사이드 함량을 조사한 결 과에 의하면 동체, 지근, 세근 부위에서 총 진세노사이드 함 량이 각각 21.64mg/g, 62.15mg/g, 88.18mg/g으로 부위별 진 세노사이드 함량이 각각 달랐으며 세근 부위의 함량이 가장 높았다. 특히, 진세노사이드 Rb1 함량은 세근 28.12mg/g, 지 근 18.12mg/g, 동체 9.31mg/g으로 세근 부위의 함량이 가장 높았음을 보고하고 있다(Han et al., 2010).
그러나, 홍삼은 다양한 약리·병리적인 효과가 뛰어나 약 용으로만 인식되어 있어 식품으로서의 친근성이 떨어지고, 홍삼의 고유한 향 및 쓴맛으로 인해 일부 소비자층(젊은층) 들에게 거부감을 나타내고 있다. 이를 고려하여 홍삼을 통 째로 벌꿀 또는 당액에 넣어 조리거나 재워 만든 당절임(정 과)이라는 제품이 있는데, 이 제품의 소비량은 꾸준히 증가 하는 것으로 조사되었다(2006년 67톤에서 2012년 508톤). 반면, 당절임 홍삼류(예, 홍삼정과)는 제조 가공 시 다량의 부산물(당절임 잔뿌리, 절삼류, 당침액 등)이 생성되는데(당 침홍삼 연 매출액 50억 기준 부산물 생성량 약 20톤, 금산 소재 D기업 자료), 이 중 뿌리부분(지근, 세근류)은 진세노 사이드 함량이 상기에서 언급한 것과 같이 동체에 비해 2-3 배 이상 높게 함유되어 있음에도 불구하고 현재 퇴비 및 동물사료 등으로 폐기물화 되고 있는 실정이다.
이에 본 연구는 홍삼정과 제조가공시 생성되는 부산물(뿌 리부분) 중의 유용성분, 즉 진세노사이드를 추출·분리하여 산업적 효용성을 증대함에 있어서 먼저, 추출용매의 농도, 온도, 시간 등을 독립변수로 하여 D-optimal design을 통하여 실험계획하고 반응표면분석법(response surface methodolgy, RSM)을 이용하여 진세노사이드 추출 최적조건을 규명하고 자 하였으며, 최종적으로 식품산업에서 본 추출법의 적용 여부를 평가하기 위한 기초 자료를 확보하는 데 그 목적이 있다.
재료 및 방법
실험재료
본 실험에 사용된 홍삼정과 부산물은 금산소재 D사에서 공급받아 0.3 mm 간격으로 잘라 -80°C의 deep freezer (DF8514, Ilshin Bio Base, Yangju, Korea)에 보관하면서 시료 로 사용하였다. 추출용매 에탄올은 식용주정(Korea Ethanol Supplies Co., Seoul, Korea)으로 사용하였으며 ginsenoside 표준시약으로 Rg3 (Chengdu Biopurify Phytochemicals, Sichuan, China) 등 20종을 사용하였다. Acetonitrile (Merck, Darmstadt, Germany)은 HPLC 분석용으로 사용하였다.
홍삼정과 부산물로부터 진세노사이드 추출공정
홍삼정과 부산물 중 진세노사이드 추출은 Sung & Yang (1985)의 방법을 응용하여 진행하였다. 즉, 일정한 크기 (0.3 mm)로 자른 홍삼정과 부산물 100 g에 중량대비 추출용 매(X1, 에탄올 30-90%, v/v) 10배량을 가한 후 shaking bath (HB-250SW, Hanbaek Co. Ltd., Bucheon, Korea)에서 100 rpm으로 shaking하면서 추출온도(X2, 25-70°C), 추출시간(X3, 5-11 hr)동안 추출하였다. 추출이 완료된 후 여과포로 1차 여 과한 여액은 10,000 ×g에서 20분간 원심분리(Supra 2000, Hanil Scientific Inc., Seoul, Korea)시켜 침전물을 제거시킨 다음 상등액을 감압농축기(NE-1000SW, Eyela Co., Tokyo, Japan)를 이용하여 농축하여 최종 시료로 사용하였다.
추출조건 설정을 위한 실험계획
홍삼정과 부산물 중 진세노사이드 추출 최적조건을 도출 하기 위하여 반응표면분석에 적합한 D-optimal design에 따라 실험을 설계하였다(Table 1). 독립변수(Xn)로는 추출 공정에 영향을 미칠 것으로 예상되는 추출용매 농도(X1), 반응온도(X2) 및 반응시간(X3)을 설정했으며 종속변수(Yn) 는 추출수율(Y1) 및 총 진세노사이드 함량(Y2)으로 하였다. 추출수율은 다음과 같이 계산하였다.
Table 1.
Experimental combinations according to codes of experimental design at various extraction conditions of solvent concentration, reaction temperature, and time
|
Treatment |
Concentration (%) |
Temperature (°C) |
Time (hr) |
Actual parameters |
|
X1
|
X2
|
X3
|
Concentration (%) |
Temperature (°C) |
Time (hr) |
|
1 |
-1 |
-1 |
-1 |
30 |
25 |
5 |
|
2 |
1 |
-1 |
-1 |
90 |
25 |
5 |
|
3 |
0.333 |
0.333 |
-1 |
70 |
55 |
5 |
|
4 |
-1 |
1 |
-1 |
30 |
70 |
5 |
|
5 |
1 |
1 |
-1 |
90 |
70 |
5 |
|
6 |
-0.333 |
-1 |
-0.333 |
50 |
25 |
7 |
|
7 |
-1 |
-0.333 |
-0.333 |
30 |
40 |
7 |
|
8 |
1 |
0.333 |
-0.333 |
90 |
55 |
7 |
|
9 |
1 |
-0.333 |
0.333 |
90 |
40 |
9 |
|
10 |
0.333 |
1 |
0.333 |
70 |
70 |
9 |
|
11 |
-1 |
-1 |
1 |
30 |
25 |
11 |
|
12 |
1 |
-1 |
1 |
90 |
25 |
11 |
|
13 |
0.333 |
-0.333 |
1 |
70 |
40 |
11 |
|
14 |
-0.333 |
0.333 |
1 |
50 |
55 |
11 |
|
15 |
-1 |
1 |
1 |
30 |
70 |
11 |
|
16 |
1 |
1 |
1 |
90 |
70 |
11 |
|
17 |
1 |
1 |
1 |
90 |
70 |
11 |
|
18 |
1 |
1 |
1 |
90 |
70 |
11 |
Download Excel Table
추출 최적조건의 도출을 위해 설계된 18개의 실험구간에 대한 종속변수 및 독립변수 상호작용은 Modde 프로그램 (Ver. 5.0, Umetrics, Umea, Sweden)을 사용하여 분석하였다.
가용성 고형분 함량 측정
가용성 고형분 함량은 식품공전에 준하여 측정하였다. 즉, 시료 50 mL를 항량을 구한 수기에 취하여 105°C에서 증발 건조시켜 무게를 측정하여 수분의 함량을 측정하였다. 그리 고 100 에서 수분함량을 빼어 고형분 함량을 구하였다.
총 진세노사이드 조성 및 함량 분석
총 진세노사이드 조성 및 함량은 Table 1의 추출조건으 로 추출된 시료를 HPLC용 메탄올에 용해한 후 이를 membrane filter (0.2 μm pore size, Whatman Co., Kent, England)로 여과, HPLC (Agilent 1200, Agilent technologies, Santa Clara, CA, USA)에 10 μL씩 주입하여 분석하였으며, 검출기는 YMC Pro C18 RS (YMC Co., Ltd, Kyoto, Japan) 을 장착한 HPLC system (Agilent 1200 series system with DAD detector at 203 nm)을 이용하여 분석하였다. 분석조 건은 이동상으로 용매 A (water)와 용매 B (acetonitrile)를 사용하여 gradient 조건으로 용매 B의 비율을 초기 20%로 흘려주고 25분까지 24%, 30분까지 33%, 42분까지 37%, 57분까지 80%, 58분까지 100%, 68분까지 60%, 70분까지 20%로 순차적으로 유속 1 mL/min로 흘려주었다(Lee et al., 2015). 진세노사이드 표준물질은 순도 99% 이상의 Rg3 (Chengdu Biopurify Phytochemicals, Sichuan, China)등 20 종의 진세노사이드를 이용하여 검량곡선으로 하여 피크면 적에 의하여 환산하여 정량하였다.
통계처리
모든 실험 결과들은 2회 반복 측정하여 평균치와 표준편 차로 나타내었으며, 각 처리별 평균치간의 유의성 검정은 SAS version 9.40 (SAS Institute Inc., Cary, NC, USA)을 이용하여 ANOVA 분석 후 p<0.05에서 Duncan’s multiple range test를 이용하여 유의성 검증을 하였다.
결과 및 고찰
추출조건에 따른 수율의 변화
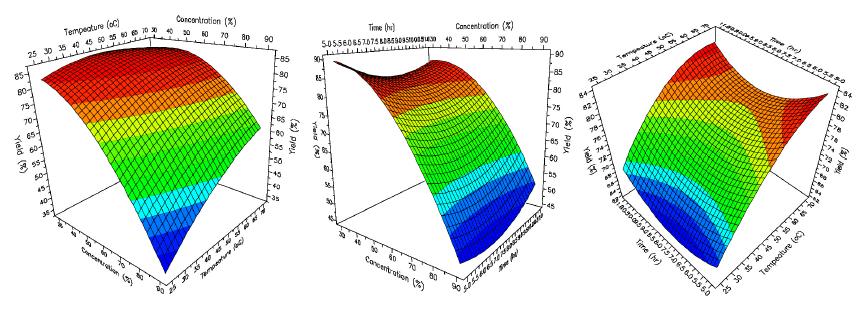
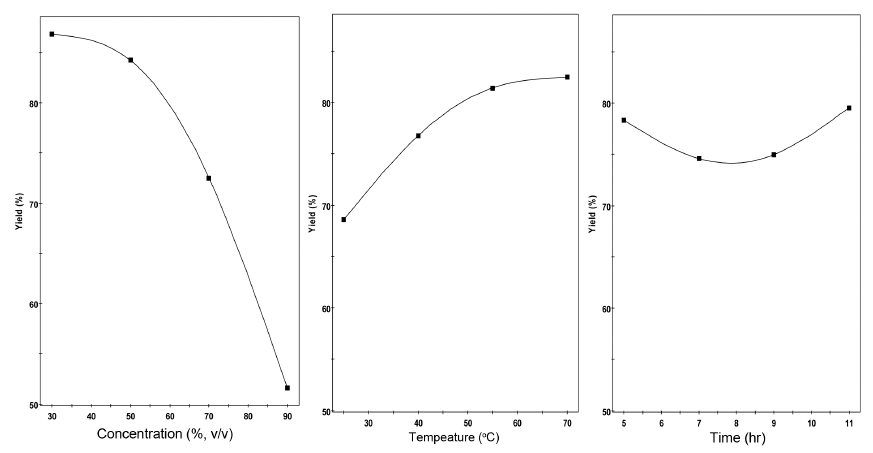
홍삼정과 부산물로 각 추출조건에 따른 수율 및 총사포닌 함량을 Table 2에 나타내었다. 추출용매 농도, 추출온도, 추 출시간을 달리한 18개 구간에서 추출액의 추출수율은 25.79- 87.91%의 범위로 추출용매 농도 30%, 추출온도 70°C, 추출 시간 11시간 조건(No. 15 실험구)에서 가장 높았으며, 추 출용매 농도 90%, 추출온도 25°C, 추출시간 5시간 조건 (No. 2 실험구)에서 가장 낮은 추출수율을 나타냈다. 각 독 립변수 값의 변화에 따른 반응변수의 값을 등고선으로 표 현한 후 추출수율의 변화를 분석한 결과(Fig. 1), 각 독립 변수인 추출온도와 추출시간이 증가할수록 추출수율은 증 가하는 것으로 나타났고, 반면, 추출용매 농도가 증가할수 록 추출수율은 감소하는 것으로 나타났다. 최대 수율을 유 도한 조건(No. 15 실험구)을 기본으로 하여 각 독립변수 값의 변화에 따른 추출수율에 prediction plot을 Fig. 2에 나타내었다. Fig. 2에 의하면 추출용매 30% (v/v)에서 추 출수율 83.5%, 50%에서 79.8%, 70%에서 66.3%, 90%에 서 44.1%로 추출용매 중 에탄올 농도가 증가함에 따라 수 율은 약 1.89배 감소할 것으로 예측되었다. 이는 고농도의 에탄올을 추출용매로 사용할 경우 홍삼정과 부산물에 함유 된 다량의 전분(26.2-36.6%), 다당류, 펙틴, 단백질 등의 수 용성 고분자 물질들이 거의 용출되지 않고 또한, 조직의 팽 윤이 저해되어 초래된 결과로 추정되었다(Sung, 1983; Sung & Kim, 1986; Ko et al., 1992).
Table 2.
Extraction yield and total ginsenoside contents data according to the extraction conditions for response surface analysis
|
Treatment |
Extraction conditions |
Responses |
|
|
|
Concentration (%) |
Temperature (°C) |
Time (hr) |
Yield (%) |
Total ginsenoside contents (mg/g) |
|
1 |
30 |
25 |
5 |
80.59±1.49ab
|
3.56±1.061)cd2) |
|
2 |
90 |
25 |
5 |
25.79±1.70i
|
1.89±0.33d
|
|
3 |
70 |
55 |
5 |
74.43±5.24bc
|
7.42±1.24abc
|
|
4 |
30 |
70 |
5 |
81.14±2.66ab
|
6.21±0.12abcd
|
|
5 |
90 |
70 |
5 |
56.46±0.44ef
|
5.40±2.64ab
|
|
6 |
50 |
25 |
7 |
76.56±0.45bc
|
7.15±0.24abcd
|
|
7 |
30 |
40 |
7 |
82.74±5.62ab
|
5.88±0.59abcd
|
|
8 |
90 |
55 |
7 |
47.89±2.54fg
|
8.95±0.38ab
|
|
9 |
90 |
40 |
9 |
40.99±11.31gh
|
6.21±1.42abcd
|
|
10 |
70 |
70 |
9 |
70.17±12.53dc
|
9.62±0.94a
|
|
11 |
30 |
25 |
11 |
87.58±1.66a
|
3.65±0.53bcd
|
|
12 |
90 |
25 |
11 |
32.03±7.66hi
|
8.96±2.23ab
|
|
13 |
70 |
40 |
11 |
75.04±5.68bc
|
10.07±0.24a
|
|
14 |
50 |
55 |
11 |
81.76±1.84ab
|
8.35±1.53abc
|
|
15 |
30 |
70 |
11 |
87.91±4.18a
|
6.16±0.36abcd
|
|
16 |
90 |
70 |
11 |
62.67±1.05de
|
6.97±0.68abcd
|
|
17 |
90 |
70 |
11 |
59.93±6.46e
|
9.29±1.71a
|
|
18 |
90 |
70 |
11 |
60.34±5.94de
|
9.72±1.25a
|
Download Excel Table
Fig. 1.
Contour plots for yield of extraction saponins with respect to the extraction condition.
Download Original Figure
Fig. 2.
Response prediction plot for the effect of ethanol concentration, temperature, and time on the extraction yield.
Download Original Figure
또한, 추출온도의 변화에 따른 추출수율의 변화는 최소 추출온도인 25°C에서 62.1%, 최대 추출온도인 70°C에서 78.3%로 온도가 상승함에 따라 추출수율이 증가하는 경향 을 보였으며, 이는 에탄올 농도가 낮고 추출온도가 증가할 수록 고분자 물질(전분, 펙틴, 단백질 등)이 조직 내에서 추출이 원활해져서 추출수율이 증가하였음을 보고한 Sung & Kim (1986)의 결과와 유사한 것으로 사료되었다.
추출시간의 변화에 따른 추출수율은 5시간 78.4%, 7시간 74.7%, 11시간에서 79.6%로 추출시간 7시간에서 다소 감 소하다 증가하였으나 유의적 차이는 없었다(p > 0.05).
따라서, 추출용매 농도 및 추출온도의 변화에 따른 추출 수율의 변화와 비교하였을 때 약 1.06배 더 낮은 것으로 예측되어, 추출용매 농도에 가장 큰 영향을 미치는 것으로 나타났다.
추출조건에 따른 총 진세노사이드 함량변화
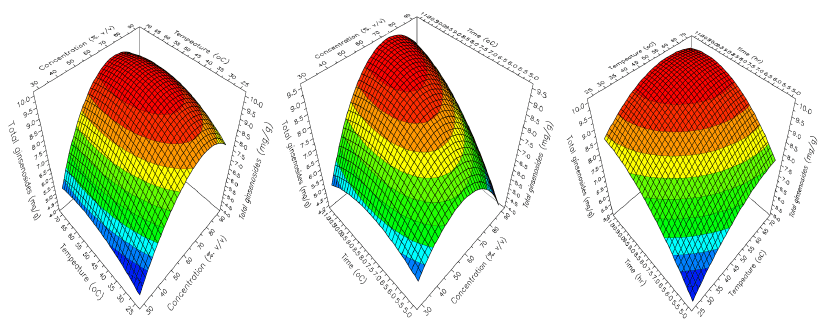
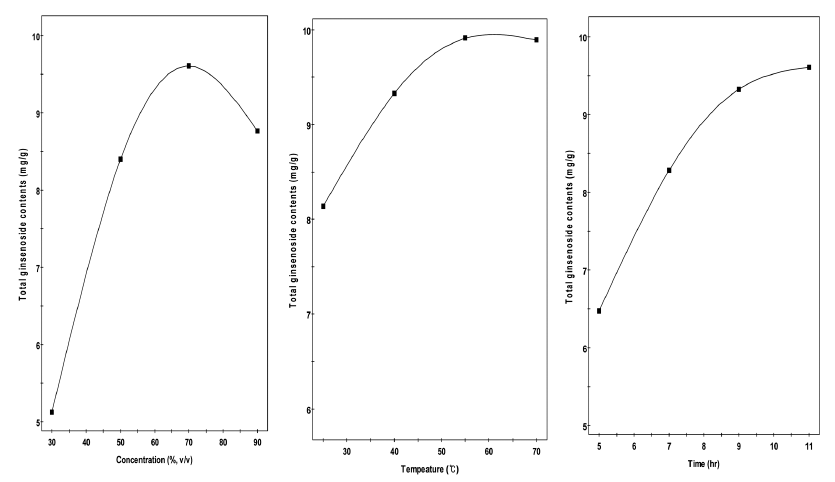
각 추출조건에 따른 총 진세노사이드 함량을 분석한 결 과는 Table 2-4에 나타냈다. 추출용매 농도, 추출온도, 추 출시간을 달리한 18개 구간에서 추출액의 총 진세노사이드 함량은 1.89-10.07 mg/g의 범위로 에탄올 농도 70%, 추출 온도 40°C, 추출시간 11시간 조건(No. 13 실험구)에서 가 장 높았으며, 에탄올 농도 90%, 추출온도 25°C, 추출시간 5시간 조건(No. 2 실험구)에서 가장 낮은 총 진세노사이드 함량을 나타냈다(Table 2). 각 독립변수 값의 변화에 따른 반응변수의 값을 등고선으로 표현한 후 총 진세노사이드 함량 변화를 분석한 결과(Fig. 3), 추출온도와 추출시간이 증가할수록 총 진세노사이드 함량은 증가하는 경향을 나타 냈고 반면, 추출용매 농도는 추출용매 농도 70%까지 총 진세노사이드 함량은 최대로 증가하다 이후 감소하는 것으 로 나타났다. 최대 총 진세노사이드 함량을 유도한 조건 (No. 13 실험구)을 기본으로 하여 각 독립변수 값의 변화에 따른 추출액의 총 진세노사이드 함량의 prediction plot을 Fig. 4에 나타냈는데, 추출용매 농도에 따른 총 진세노사이 드 함량의 변화는 30% 5.15 mg/g, 50% 8.40 mg/g, 70% 9.63 mg/g, 90% 8.78 mg/g로 추출용매 농도 70%까지 증가 하다 90%에서 약 1.38배 정도 감소되는 것으로 예측되었 다. 이는 Sung & Yang (1985)의 연구 결과와 유사한 경향 으로 높은 에탄올 농도(예, 90%)에서 프로토파낙사트리올 (protopanaxadiol, PPD)계 -Rb2, -Rb1 등 일부 구성성분들의 추출이 감소하여 추출물 중 총 진세노사이드 함량이 감소하 며, 이는 용매의 극성 차이가 진세노사이드를 구성하는 성 분들의 용해도를 다르게 하여 진세노사이드 추출에 영향을 미친다고 하였다. Table 3
Table 3.
Total ginsenoside contents according to the extraction conditions for response surface analysis
|
Treatment |
Extraction conditions |
Ginsenoside contents (mg/g) |
|
|
|
Conc. (%) |
Temp. (°C) |
Time (hr) |
Rg1 |
Re |
Rf |
Rb1 |
Rc |
Rg2 |
Rh1 |
Rb2 |
Rb3 |
Rd |
|
1 |
30 |
25 |
5 |
0.013±0.000a
|
0.013±0.000a
|
0.057±0.016d
|
0.174±0.042d
|
0.089±0.019b
|
0.069±0.020b
|
0.121±0.031cde
|
0.062±0.014b
|
0.133±0.030cd
|
0.038±0.000de
|
|
2 |
90 |
25 |
5 |
0.014±0.000a
|
0.021±0.000a
|
0.030±0.006d
|
0.240±0.001abcd
|
0.156±0.007ab
|
0.027±0.007b
|
0.049±0.013de
|
0.102±0.006ab
|
0.069±0.016cd
|
0.038±0.000cde
|
|
3 |
70 |
55 |
5 |
0.023±0.000a
|
0.021±0.000a
|
0.099±0.005abcd
|
0.409±0.104abcd
|
0.232±0.084ab
|
0.108±0.004b
|
0.184±0.013abcde
|
0.170±0.070ab
|
0.209±0.015abc
|
0.041±0.000bcde
|
|
4 |
30 |
70 |
5 |
0.022±0.000a
|
0.022±0.000a
|
0.105±0.002d
|
0.422±0.022cd
|
0.266±0.028ab
|
0.122±0.003b
|
0.195±0.007cde
|
0.162±0.013b
|
0.201±0.006cd
|
0.052±0.000de
|
|
5 |
90 |
70 |
5 |
0.018±0.000a
|
0.018±0.000a
|
0.070±0.044abcd
|
0.317±0.096abcd
|
0.182±0.034ab
|
0.082±0.058b
|
0.138±0.097abcde
|
0.112±0.031ab
|
0.156±0.102abcd
|
0.075±0.040cde
|
|
6 |
50 |
25 |
7 |
0.017±0.000a
|
0.016±0.000a
|
0.097±0.001cd
|
0.346±0.018bcd
|
0.190±0.014ab
|
0.109±0.003b
|
0.189±0.004cde
|
0.127±0.009b
|
0.199±0.003cd
|
0.074±0.007cde
|
|
7 |
30 |
40 |
7 |
0.026±0.000a
|
0.027±0.000a
|
0.107±0.027abcd
|
0.438±0.103abcd
|
0.252±0.055ab
|
0.117±0.034b
|
0.191±0.052abcde
|
0.169±0.031ab
|
0.194±0.055bcd
|
0.128±0.031abcd
|
|
8 |
90 |
55 |
7 |
0.050±0.007a
|
0.069±0.030a
|
0.121±0.009abc
|
0.543±0.188ab
|
0.092±0.000ab
|
0.246±0.119a
|
0.166±0.064abcde
|
0.280±0.153a
|
0.233±0.019a
|
0.161±0.070a
|
|
9 |
90 |
40 |
9 |
0.022±0.000a
|
0.021±0.000a
|
0.089±0.035abcd
|
0.360±0.062abcd
|
0.194±0.022ab
|
0.094±0.046b
|
0.162±0.073abcde
|
0.133±0.017ab
|
0.172±0.082abc
|
0.086±0.015abc
|
|
10 |
70 |
70 |
9 |
0.038±0.000a
|
0.033±0.000a
|
0.124±0.028abc
|
0.520±0.046abc
|
0.306±0.033ab
|
0.138±0.041ab
|
0.230±0.063ab
|
0.190±0.001ab
|
0.244±0.058a
|
0.146±0.002ab
|
|
11 |
30 |
25 |
11 |
0.023±0.000a
|
0.019±0.000a
|
0.073±0.026cd
|
0.256±0.072bcd
|
0.150±0.030ab
|
0.145±0.087ab
|
0.074±0.002e
|
0.141±0.068ab
|
0.068±0.001d
|
0.031±0.000bcde
|
|
12 |
90 |
25 |
11 |
0.052±0.015a
|
0.058±0.026a
|
0.127±0.048a
|
0.526±0.245abc
|
0.290±0.168ab
|
0.133±0.045ab
|
0.235±0.066a
|
0.194±0.110ab
|
0.244±0.045a
|
0.136±0.057abc
|
|
13 |
70 |
40 |
11 |
0.027±0.000a
|
0.027±0.000a
|
0.132±0.007abcd
|
0.525±0.050abcd
|
0.295±0.039ab
|
0.153±0.004ab
|
0.246±0.001abcd
|
0.187±0.025ab
|
0.228±0.003abc
|
0.133±0.013e
|
|
14 |
50 |
55 |
11 |
0.025±0.000a
|
0.025±0.000a
|
0.108±0.029abcd
|
0.399±0.093abcd
|
0.240±0.051ab
|
0.122±0.043ab
|
0.209±0.064abc
|
0.147±0.036ab
|
0.202±0.055abc
|
0.112±0.032abcde
|
|
15 |
30 |
70 |
11 |
0.020±0.000a
|
0.019±0.000a
|
0.086±0.019bcd
|
0.313±0.091abcd
|
0.182±0.049ab
|
0.093±0.022b
|
0.164±0.038bcde
|
0.128±0.033b
|
0.164±0.040cd
|
0.101±0.032abcde
|
|
16 |
90 |
70 |
11 |
0.023±0.000a
|
0.022±0.000a
|
0.093±0.010abcd
|
0.471±0.073abcd
|
0.234±0.027ab
|
0.118±0.031ab
|
0.165±0.014abcde
|
0.180±0.024ab
|
0.165±0.019abc
|
0.116±0.021abcde
|
|
17 |
90 |
70 |
11 |
0.036±0.000a
|
0.036±0.000a
|
0.121±0.045ab
|
0.558±0.184a
|
0.293±0.122a
|
0.148±0.038ab
|
0.220±0.081a
|
0.197±0.075ab
|
0.212±0.070abc
|
0.129±0.045abcd
|
|
18 |
90 |
70 |
11 |
0.046±0.000a
|
0.054±0.000a
|
0.131±0.045a
|
0.565±0.251a
|
0.309±0.175a
|
0.155±0.032ab
|
0.230±0.066a
|
0.214±0.097ab
|
0.226±0.060abc
|
0.150±0.062ab
|
Download Excel Table
Table 4.
Total ginsenoside contents according to the extraction conditions for response surface analysis
|
Treatment |
Extraction conditions |
Ginsenoside contents (mg/g) |
|
|
|
Conc. |
Temp. |
Time |
Rg6 |
F4 |
Rh4 |
Rg3-S |
Rg3 |
Rg3-R |
Rk1 |
Rg5 |
C-K |
Rh2 |
Total |
|
(%) |
(°C) |
(hr) |
|
1 |
30 |
25 |
5 |
0.051±0.018e
|
0.074±0.014b
|
0.736±0.120d
|
0.412±0.086f
|
0.177±0.021g
|
0.335±0.074d
|
0.158±0.027f
|
0.805±0.122a
|
N.D.2) |
0.043±0.000a
|
3.56±1.061)cd3) |
|
2 |
90 |
25 |
5 |
0.024±0.009e
|
0.025±0.010b
|
0.253±0.103d
|
0.153±0.058f
|
0.107±0.041g
|
0.146±0.056d
|
0.081±0.031f
|
0.327±0.156a
|
N.D. |
0.025±0.000a
|
1.89±0.33d
|
|
3 |
70 |
55 |
5 |
0.114±0.007abcde
|
0.119±0.008b
|
1.178±0.049abcd
|
0.827±0.039abcdef
|
0.412±0.007bcdefg
|
0.544±0.045bcd
|
0.443±0.023bcdef
|
2.255±0.091a
|
0.021±0.001ab
|
0.008±0.024a
|
7.42±1.24abc
|
|
4 |
30 |
70 |
5 |
0.122±0.002de
|
0.122±0.002b
|
1.193±0.004cd
|
0.631±0.025ef
|
0.306±0.011g
|
0.466±0.003d
|
0.285±0.012ef
|
1.517±0.049a
|
N.D. |
N.D. |
6.21±0.12abcd
|
|
5 |
90 |
70 |
5 |
0.087±0.066abcde
|
0.085±0.064b
|
0.834±0.622abcd
|
0.588±0.452abcdef
|
0.306±0.225cdefg
|
0.463±0.339abcd
|
0.318±0.246bcdef
|
1.527±1.193a
|
0.011±0.000ab
|
0.016±0.000a
|
5.40±2.64ab
|
|
6 |
50 |
25 |
7 |
0.120±0.002cde
|
0.123±0.002b
|
1.187±0.001abcd
|
0.818±0.015bcdef
|
0.392±0.011defg
|
0.569±0.009cd
|
0.430±0.009cdef
|
2.097±0.024a
|
0.053±0.005ab
|
N.D. |
7.15±0.24abcd
|
|
7 |
30 |
40 |
7 |
0.115±0.036bcde
|
0.116±0.035b
|
1.085±0.317abcd
|
0.655±0.263bcdef
|
0.257±0.097efg
|
0.479±0.175bcd
|
0.262±0.119def
|
1.227±0.495a
|
0.007±0.000ab
|
0.026±0.000a
|
5.88±0.59abcd
|
|
8 |
90 |
55 |
7 |
0.145±0.003abcd
|
0.149±0.006b
|
1.431±0.046ab
|
0.969±0.026abc
|
0.484±0.020abcd
|
0.700±0.069ab
|
0.521±0.015bc
|
2.553±0.098a
|
0.022±0.004ab
|
0.013±0.003a
|
8.95±0.38ab
|
|
9 |
90 |
40 |
9 |
0.108±0.031abcde
|
0.094±0.053b
|
0.979±0.392abcd
|
0.592±0.344abcdef
|
0.422±0.110abcd
|
0.548±0.257abcd
|
0.375±0.149bcdef
|
1.732±0.691a
|
0.008±0.000ab
|
0.018±0.001a
|
6.21±1.42abcd
|
|
10 |
70 |
70 |
9 |
0.178±0.020ab
|
0.137±0.047b
|
1.514±0.264ab
|
0.934±0.405abc
|
0.611±0.064a
|
0.702±0.194abc
|
0.587±0.147b
|
2.910±0.642a
|
0.028±0.004ab
|
0.000±0.017a
|
9.62±0.94a
|
|
11 |
30 |
25 |
11 |
0.066±0.026de
|
0.086±0.026b
|
0.766±0.255bcd
|
0.381±0.184def
|
0.198±0.043g
|
0.362±0.130d
|
0.330±0.203cdef
|
0.480±0.009a
|
N.D. |
N.D. |
3.65±0.53bcd
|
|
12 |
90 |
25 |
11 |
0.176±0.085a
|
0.313±0.179a
|
1.082±0.895abcd
|
1.011±0.273ab
|
0.551±0.076ab
|
0.850±0.190a
|
0.918±0.257a
|
2.036±1.427a
|
0.019±0.007ab
|
0.015±0.000a
|
8.96±2.23ab
|
|
13 |
70 |
40 |
11 |
0.167±0.009abcde
|
0.165±0.009b
|
1.609±0.105abcd
|
1.165±0.073abcde
|
0.519±0.006abcde
|
0.702±0.010abcd
|
0.635±0.046bcd
|
3.109±0.200a
|
0.028±0.006ab
|
0.018±0.003a
|
10.07±0.24a
|
|
14 |
50 |
55 |
11 |
0.133±0.040abcde
|
0.141±0.032b
|
1.391±0.295abcd
|
0.966±0.288abcd
|
0.436±0.137abcde
|
0.596±0.175abcd
|
0.513±0.149bcd
|
2.551±0.727a
|
0.011±0.002ab
|
0.020±0.000a
|
8.35±1.53abc
|
|
15 |
30 |
70 |
11 |
0.097±0.015cde
|
0.104±0.010b
|
1.070±0.116abcd
|
0.686±0.087cdef
|
0.357±0.062defg
|
0.451±0.050d
|
0.302±0.031def
|
1.756±0.216a
|
0.018±0.001ab
|
0.048±0.008a
|
6.16±0.36abcd
|
|
16 |
90 |
70 |
11 |
0.107±0.013abcde
|
0.112±0.019b
|
1.093±0.223abcd
|
0.761±0.096abcde
|
0.362±0.034abcdef
|
0.464±0.008abcd
|
0.413±0.066bcde
|
2.053±0.359a
|
0.015±0.014ab
|
N.D. |
6.97±0.68abcd
|
|
17 |
90 |
70 |
11 |
0.141±0.051abcd
|
0.149±0.039b
|
1.464±0.356ab
|
1.011±0.328a
|
0.508±0.181abc
|
0.686±0.311ab
|
0.561±0.188b
|
2.786±0.861a
|
0.024±0.001ab
|
0.025±0.000a
|
9.29±1.71a
|
|
18 |
90 |
70 |
11 |
0.148±0.040abc
|
0.159±0.027b
|
1.556±0.247a
|
1.058±0.247a
|
0.522±0.141abc
|
0.693±0.240ab
|
0.576±0.127b
|
2.887±0.589a
|
0.027±0.001a
|
0.024±0.000a
|
9.72±1.25a
|
Download Excel Table
Fig. 4.
Response prediction plot for the effect of ethanol concentration, temperature, and time on the total saponins.
Download Original Figure
또한, 추출온도에 따른 총 진세노사이드 함량의 변화는 최소 추출온도 25°C에서 8.38 mg/g, 최대 추출온도 70°C에 서 10.00 mg/g 으로 추출온도가 상승함에 따라 총 진세노사 이드 함량이 증가하는 경향을 나타냈다. Sung et al. (1985) 의 보고에 의하면 추출온도 100°C에서 진세노사이드 종류 에 따라 열에 대한 안정성이 낮아져서 총 진세노사이드 함 량이 감소한다고 보고하였으나 본 연구결과에서는 최대 추 출온도가 70°C로 추출액의 총 진세노사이드 함량에 영향을 미치지 않은 것으로 사료된다.
추출시간의 변화에 따른 총 진세노사이드 함량의 변화는 5 시간에서 6.49mg/g, 11시간에서 9.62mg/g으로 추출시간이 증가할수록 총 진세노사이드 함량은 증가하는 경향을 나타냈 다. 이는 Han et al. (2010)이 추출온도 75°C에서 홍삼 부위별 추출시간에 따른 총 진세노사이드 함량을 조사한 결과 동체 21시간(23.04mg/100mL), 지근 18시간(65.68mg/100mL), 세 근 12시간(295.92mg/100mL) 추출액에서 최고 함량을 나타 났다고 보고하였는데 본 연구 결과에서도 유사한 경향을 나 타냈다.
총 진세노사이드 추출조건의 최적화
홍삼정과 부산물로부터 총 진세노사이드 추출 최적조건을 도출하기 위하여 추출용매 농도(X1), 추출온도(X2) 및 추출 시간(X3)을 독립변수(Xn)로 설정한 후 D-optimal design에 의한 반응표면분석을 실시하여 최적화 조건을 도출하였다. 즉, 반응변수(Yn)인 추출수율(Y1) 및 총 진세노사이드 함량 (Y2)의 변화를 회귀분석하여 독립변수의 일차항. 이차항, 교 호항을 통해 얻은 반응변수에 대한 반응표면회귀식과 유의 성을 Table 5에 나타냈다. ANOVA 분석에서 모델의 적합성 평가를 위한 lack of fit의 p-value는 0.05 이상이어야만 적합 한 모형이라 판단하며, R2 (coefficient of determination)은 회 귀모델이 데이터를 얼마나 근접하게 예측하고 있는가를 나 타내는 척도가 되고, 그 수치가 1에 가까울수록 실험식이 실제 실험값과 일치하는 좋은 모형임을 나타낸다. 추출수 율과 총 진세노사이드 함량에 대한 lack of fit의 p-value는 각각 0.072 및 0.664로 본 실험의 수행을 위하여 가정된 모델(Table 1)은 적합한 것으로 판단되었고 추출수율과 총 진세노사이드 함량의 R2 값은 0.971 및 0.846로 나타났다. 추출공정의 최적조건을 찾기 위한 회귀분석결과, 추출용매 농도 57.90%, 추출온도 56.94°C, 추출시간 11시간일 때 추 출수율은 84.52%, 총 진세노사이드 함량은 9.54 mg/g로 예 측되었다.
Table 5.
Second order polynomial equation calculated by response surface methodology program on yield and total ginsenosides
|
Responses |
Polynomial equation |
R2
|
Significance |
Lack of fit |
|
Yield (%, Y1) |
Y1 = 71.5013 - 19.5166X1 + 7.12453X2 + 1.96518X3 - 7.85676X12 + 5.20266X1X2
|
0.971 |
0.000 |
0.072 |
|
-2.93469X22 + 1.53743X1X3 - 0.865563X2X3 + 3.62642X32
|
|
Total ginsenosides |
Y2=9.6602-0.0236685X1 + 0.688243X2 + 0.84433X3 - 1.75861X12
|
0.846 |
0.018 |
0.664 |
|
(mg/g, Y2) |
- 0.00852562X1X2 - 0.498489X22 + 0.889431X1X3 - 0.30844X2X3 - 0.30844X32
|
Download Excel Table
이는 홍삼정과 제조시 당침액(올리고당, 설탕 등)이 홍삼 내로 침투하여 홍삼 중 총 진세노사이드 함량이 상대적으 로 감소하고 또한 제조 공정 중 고온 장시간 열처리가 추 가적으로 진세노사이드 함량의 감소를 초래하는 것으로 사 료된다. Song et al. (2010)의 보고에서도 인삼정과 제조 후 총 진세노사이드 함량이 4.12-10 mg/g으로 분석되어 본 연구와 유사한 결과를 나타냈다.
요 약
본 연구는 홍삼정과 부산물의 산업적 이용성 증대를 위 하여 중 반응표면분석법을 이용한 추출수율 및 총 진세노 사이드 함량 추출 최적조건을 찾는데 목적이 있다. 추출용 매 농도(에탄올, 30-70%, v/v), 추출온도(25-70°C), 추출시 간(5-11 hr) 등의 독립변수를 D-optimal design을 통하여 실 험계획하고, 얻어진 실험결과를 반응표면분석하여 추출수 율, 총 진세노사이드 함량 등의 반응변수에 대한 최적 추 출조건을 검토하였다. 그 결과, 독립변수인 추출온도와 시 간이 증가함에 따라 수율 및 총 진세노사이드 함량은 증가 하였으나, 추출용매(에탄올)의 경우 고농도에서 수율은 감 소한 반면, 추출물 중 총 진세노사이드 함량은 증가하였다. 독립변수 중 추출용매의 농도가 각 반응변수에 가장 큰 영 향을 주는 것으로 나타났다. 본 연구를 통해서 유도된 회 귀식 모형은 실험을 통해 얻은 결과와 잘 일치하였고, 추 출수율과 총 진세노사이드 함량을 최대로 하는 최적 조건 은 추출용매농도 57.90% (v/v), 추출온도 56.94°C, 추출시 간 11시간으로 이 경우 추출수율은 84.52%, 총 진세노사 이드 함량은 9.54 mg/g으로 예측하였다.
감사의 글
본 결과물은 농림축산식품부의 재원으로 농림수산식품기 술기획평가원의 수출전략기술개발사업의 자원을 받아 연구 되었음(과제번호: 115070).
References
Cho WC, Chung WS, Lee SK, Leng AW, Cheng CH, Yue KK. Ginsenoside Re of Panax ginseng possesses significant antioxidant and antihyperlipidemic efficacies in streptozotocininduced diabetic rats . Eur. J. Pharmacol. 2006; 550:173-179.

Choi JH, Kim YS, Lee KM, Kim HJ. The effects of red ginseng intaking on free radical produced during aerobic exercise in the elderly. J. Ginseng Res. 2004; 28:27-32.

Han JS, Kang SJ, Nam KY, Choi JE. Difference of ginsenoside yields in red ginseng parts according to extraction time at low temperature. Korean. J. Crop. Sci. 2010; 55:299-305.

Jang SK, Chung YS, Ahn DC, Kang MJ, Lee DG, Kim SH. An experimental study on the effect of immunopotential and the anitcancer effect of red ginseng extact. Korean. J. Ginseng Sci. 1994; 18:151-159.

Kaku T, Miyata T, Uruno T, Sako I, Kinoshita A. Chemicopharmacological studies on saponins of Panax ginseng C. A. Meyer. II. Pharmacological part. Arznei-Forschung. 1975; 25:539-547.

Ko SR, Kim SC, Choi KJ. Extract yields and saponin contents of red ginseng extracts prepared with various concentration of ethanol. Kor. J. Pharmacogn. 1992; 23:24-28.

Lee JW, Bae YI, Shim KH. Biofunctional characteristics of the water soluble browning reaction products isolated from Korean red ginseng study on the antimutagenic and nitrite scavenging activities. J. Ginseng Res. 2001; 25:118-121.

Lee KS, Seong BJ, Kim SI, Han SH, Kim HH, Won JY, Kim GH. Change of fatty acids, minerals and ginsenosides on ginseng seeds during stratifying treatment. Korean. J. Medicinal Crop. Sci. 2015; 23:406-413.

Lee SH, Kang JI, Lee SY. Saponin composition and physicochemical properties of Korean red ginseng extract as affected by extracting conditions. J. Korean Soc. Food Sci. Nutr. 2008; 37:256-260.

Matsuda H, Samukawa K, Kubo M. Anti-inflammatory activity of ginsenoside ro. Planta. Med. 1990; 56:19-23.

Ministry of Food and Drug Safety. The statistics of mortality and the cause. 2016Available from http://www.mfds.go.kr Accessed Sep. 24. 2016
Park HJ, Park KM, Rhee MH, Song YB, Choi KJ, Lee JH, Kim SC, Park KH. Effect of ginsenoside Rb1 on rat liver phosphoproteins induced by carbon tetrachloride. Biol. Pharm. Bull. 1996; 19:834-838.

Satio H, Bao TT. Effect of red ginseng on mice exposed to various stresses. Proceeding of the 4th International Ginseng Symposium. 1984; ; September 1, Seoul, Korea p. 97-105.

Seong HS. Studies on the effect of extracting conditions on the physicochemical properties of Korean Ginseng extract. Ph.D. Thesis. 1983Hanyang Univ. Seoul: .

Song MR, Kim MR, Kim HH, Chu S, Lee KS. Quality characteristics of ginseng Jung Kwa obtained by different sugar treatments. J. Korean Soc. Food Sci. Nutr. 2010; 39:999-1004.

Sung HS, Yang CB. Effect of ethanol concentration on saponin composition of red ginseng extract. Korean. J. Food Sci. Technol. 1985; 17:227-231.

Sung HS, Yang CB, Kim WJ. Effect of extraction temperature and time on saponin composition of red ginseng extract. Korean. J. Food Sci. Technol. 1985; 17:265-270.

Sung HS, Kim WJ. Effect of extracting conditions on the soluble solid's yield of Korean red ginseng. Korean. J. Food Sci. Technol. 1986; 18:168-171.

The Foundation of Agriculture Technology Commercialization and Transfer. Industry trends of agriculture and food. Available from http://www.fact.or.kr Accessed Sep. 25. 2016. 2014