서 론
현대인들의 식생활과 관련된 당뇨병은 만성 대사질환으로, 그 유병률은 최근 들어 급격히 증가되는 추세이며, 암 및 순환기계 질환과 더불어 3대 질병으로 지목됨에 따라 그 예방과 치료에 대한 관심이 집중되고 있다(Kim et al., 2009). 당뇨병은 췌장 베타-세포에서 분비되는 인슐린의 분비장애와 말초조직에 대한 인슐린 저항으로 야기된 고혈당증(hyperglycemia)으로 당 대사는 물론 단백질, 지질 및 전해질 대사 등과 관련된 대사성 질환이다(Lee et al., 2010). 당뇨병은 발생기전에 따라 췌장 베타-세포의 파괴성 병변에 의해 인슐린이 결핍되어 생기는 제1형 당뇨병과 인슐린 분비 저하와 인슐린 저항성으로 인해 생기는 제2형 당뇨병으로 분류한다(Kim et al., 2013). 3T3-L1 세포는 지방세포의 대사 기능과 유사하며, 인슐린 신호전달 경로를 통해 혈당 조절에 중요한 역할을 한다. 이러한 지방세포의 비정상적인 분화 및 기능 저하가 인슐린 저항성에 따른 제2형 당뇨병 및 비만의 발병과 밀접한 관련이 있다(Rosen et al., 2002). 혈당 조절능력이 저하된 사람에게 과량의 포도당이 흡수되면 이를 제대로 조절하지 못해 고혈당상태를 유지하게 된다. 따라서 소장의 α-glucosidase의 활성을 억제하는 것은 혈당의 상승을 늦춰 혈당 조절은 돕는 하나의 방안이 될 수 있다(Seo et al., 2015). 당뇨병의 증세를 개선하기 위한 약물요법 가운데 현재 경구용 혈당 강하제로는 설포닐요소제, 메트포르민, α-glucosidase 저해제 등이 사용되고 있으나, 이러한 약물들은 저혈당, 간 독성, 체중 증가, 복부 팽만감, 젖산증 등의 부작용을 유발함으로 이들 약해를 최소화한 새로운 타입의 혈당 강하 소재의 발굴이 필요하다(Hwang et al., 2008). 곰보배추(Salvia plebeia Herb.)는 꿀풀과(Labiatae)의 두해살이풀로 주로 배암차즈기라고 불리우며, 잎의 모양이 곰보 같다고 하여 곰보배추, 뱀비늘처럼 생겼다고 뱀배추 등으로 불린다(Jeong et al., 2014). 곰보배추의 2차 대사산물로 유용한 약리 효과를 나타내는 성분들은 homoplantaginic, rosmarinic acid, luteolin, nepetin, nepetin-7-glucoside, hispidulin, luteolin-7-glucoside, caffeic acid, coniferyl aldehyde 등이 알려져 있다(Ren et al., 2014; Jin et al., 2008). 당뇨쥐의 혈당을 감소시키고, 혈액의 triglyceride와 총 cholesterol의 수준을 감소시키는 지방 저하 효과를 가지는 주성분으로는 cynaroside (luteoline 7-O-β-D-glucoside)가 보고된 바 있다(Park, 2014). 최근 보고된 곰보배추의 연구로는 메탄올 추출물의 항산화 활성, lipopolysaccharide 자극으로 활성화된 RAW264.7 대식세포에서 nitric oxide와 prostaglandin E2을 농도 의존적으로 억제하여 항염증 및 항알레르기 효과를 보고하였으며, 마우스 백혈병 세포 및 murine leukemia cell에 대한 세포독성 및 항균 효과, 항바이러스 작용 유도로 인한 항암 작용, 인체 유래 위암세포주인 AGS에 물과 60% 에탄올추출물 처리 시 농도 의존적인 세포 밀도 감소 효과와 관련된 다양한 연구와 약리효능 연구가 보고되었다(Kim et al., 2014). 그러나 아직 곰보배추의 혈당 강하 효과를 나타내는 관련된 연구는 미비한 실정이다. 본 연구는 곰보배추 열수 추출물과 곰보배추 에탄올 추출물의 혈당 강하 효과를 확인함과 동시에 항산화 활성에 대한 기능성을 확인하고자 하였다.
재료 및 방법
본 실험에 사용되어진 재료는 충청남도 천안에서 6월에 수확한 곰보배추(S. plebeia Herb.)를 3일간 자연건조 후 완전히 분쇄한 분말(60 g)을 10배(v/w)에 해당하는 600 mL의 70% 에탄올과 증류수를 이용하여 2시간 30분 동안 환류 냉각 추출하였다. 추출 후 그 여액을 필터 페이퍼(150 mm, Whatman)를 이용하여 필터 후 용액을 24시간동안 –20℃에서 동결시켰다. 동결된 시료를 동결건조기(lyophilizer, Il-Shin Co., Seoul, Korea)에서 48시간 동결건조시킨 곰보배추 에탄올 추출물(S. plebeia Herb. 70% ethanol extract, SPEE)과 곰보배추 물 추출물(S. plebeia Herb. water extract, SPWE) 각각의 분말을 4℃의 냉장고에 보관하면서 실험에 사용하였다.
3T3-L1 세포(American Type Culture Collection, ATCC)를 10% fetal bovine serum (FBS)가 포함된 Dulbecco's Modified Eagle Medium (DMEM) 배지에 37℃, 5% CO2 조건에서 배양하였다. 세포는 70% 정도 배양한 후 주기적으로 계대하여 실험에 사용하였다. 분화시키기 위하여 세포가 confluence 상태가 될 때까지 배양하였다. Confluence (day 0) 상태가 된 지 2일 후 MDI (25 mM glucose, 0.5 mM 3-isobutyl-1-methylxanthine, 1 μM dexametasone, 1 μg/mL insulin) 첨가 후 48 시간 동안 분화 유도를 하였다. 48 시간 후 시료 농도별로 처리하여 48 시간 동안 배양하였다. 6일째 되는 날 샘플링을 하였다.
3T3-L1 세포 (5×103개)를 10% FBS가 첨가된 DMEM 배지에서 96-well plate에 24시간 동안 안정화 시켰다. 세포에 100, 200 μg/mL의 농도로 시료들을 48시간 동안 처리한 후 세포 생존률은 Cell Proliferation MTS Kit (Promega Corporation, Madison, WI, US)를 사용설명서의 방법으로 측정하였다.
세포 내 지방생성량은 Oil Red O 시약을 사용하여 측정하였다. 3T3-L1 세포를 phosphate-buffered saline (pH 7.4)로 세척 후 10% formaldehyde로 1시간 동안 고정하였다. 1시간 후 60% isopropanol로 세척하였다. 세포는 0.5% Oil Red O로 30분 동안 실온에서 30분 동안 유지시켰다. 30분 후 지방 이외에 묻어있는 Oil Red O 시약을 씻어내기 위해 증류수로 세척하였다. 염색된 세포는 현미경으로 관찰하고 사진 촬영을 하였다. 현미경 관찰 후, 100% isopropanol (3 mL/well)을 사용하여 지방에 염색된 Oil Red O 시약을 녹인 후 각 well의 100% isopropanol을 96-well plate에 옮긴 뒤 500 nm에서 흡수되는 양으로 지방생성량을 비교하였다.
총 폴리페놀 함량은 Folin-Denis 방법을 응용하여 측정하였다. 각각의 시료 0.2 mL와 증류수 1.8 mL를 혼합한 후 2 N Folin-Ciocalteau regent 0.2 mL를 가하여 6분간 정치시킨 후, 20% sodium carbonate 2 mL를 가하고 60분간 방치한 혼합액을 1시간 동안 정치한 다음 분광광도계를 사용하여 750 nm에서 흡광도를 측정하였다. 총 폴리페놀 함량은 gallic acid를 이용하여 작성한 표준 곡선으로부터 환산하였다.
DPPH 자유라디칼 소거활성은 Faller-Fialho의 방법을 이용하여 측정하였다. DPPH는 80% 메탄올에 400 μM로 용해하였고, 시료를 50 mg/mL농도로 3차 증류수에 녹여 사용하였다. 시료 0.3 mL와 400 μM DPPH 11.7 mL를 혼합한 뒤 15분간 방치하고, ELISA reader (SPECTRA max M2, Molecular Devices Co, Sunnyvale, CA, US)를 이용하여 517 nm에서 흡광도를 측정하여 계산식을 이용해 소거 활성을 계산하였다. 양성 대조군으로는 0.5 M L-아스코르브산을 희석하여 사용하였으며, 시료 첨가군과 비첨가군의 흡광도 차이를 백분율(%)로 환산하여 나타내었다.
α-Glucosidase 억제 활성 측정은 Zhang 등(2011)의 방법에 의하여 측정하였다. 120 μL의 0.1 M phosphate buffer(pH 6.9)와 20 μL의 α-glucosidase (0.5 unit/mL)를 섞은 혼합액에 SPEE와 SPWE (1 mg/mL) 10 μL를 같이 혼합한 후 혼합액을 96 well plate에 넣어 37℃에서 15분간 반응시켰다. 반응 후 5 mM p-nitrophenyl-α-D-glucopyranoside 용액을 20 μL 추가한 후 15분 추가로 반응시켰다. 0.2 M sodium carbonate 80 μL를 추가하여 반응을 정지시킨 후 microplate reader를 사용하여 405 nm에서 흡광도를 측정하였다.
본 실험에서 사용한 실험동물은 4주령 수컷 C57BL/6 마우스를 샘타코(Osan, Korea)에서 구입하여 일주일 간 순화기간을 거친 다음 사용하였다. 실험동물 사육실은 12시간 간격으로 명암을 조절하였고, 온도는 23±2℃, 습도는 50±10%를 유지하였다. 본 동물실험은 원광대학교 동물실험가이드 (Guide for Animal Experimentation)를 준수하여 시행되었으며, 원광대학교 동물실험윤리위원회의 승인을 받아 시행하였다 (Approval NO. WKU22-133). 실험군은 대조군인 CON (D.W + Glucose)군, 약물대조군인 MET (metformin + Glucose)군, 시료투여군인 SPEE (S. plebeia Herb. ethanol extract 300 mg/kg + Glucose)군, SPWE (S. plebeia Herb. water extract 300 mg/kg + Glucose)군으로 분리하였다.
실험동물에게 0.1 M citrate buffer (pH 4.5)에 용해시킨 streptozotocin (Sigma Aldrich, St. Louis, MO, US) 120 mg/kg을 복강에 1회 주사하여 당뇨를 유발시켰다. STZ (streptozotocin)를 투여하고 2주 후 공복상태의 동물의 꼬리정맥으로부터 채혈하여 간이혈당계(Glucotrend, Roche Diagnostics, Mannheim, Germany)로 측정한 혈당이 200 mg/dL 이하인 동물은 제외하였다. 1 주일 후 혈당을 재 측정하여 혈당 200 mg/dL 이상 유지된 동물을 선별하여 사용하였다. 각 시료의 농도는 Table 1과 같다.
| Sample | Total polyphenol (mg GAE/g) |
|---|---|
| SPEE | 152.03±5.96 |
| SPWE | 81.12±0.30 |
결과 및 고찰
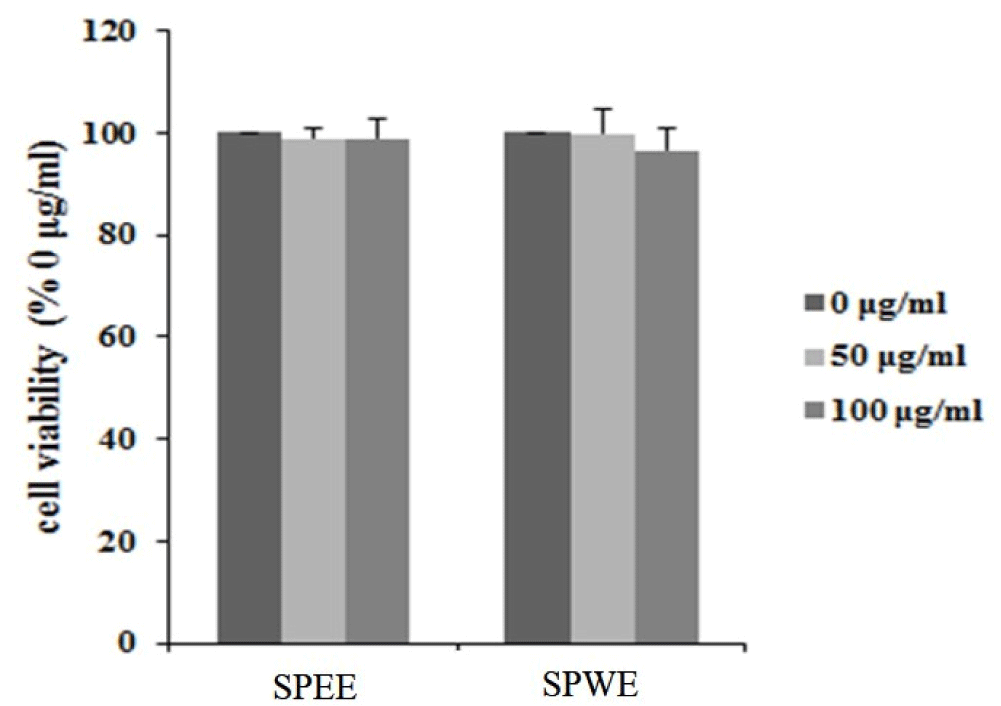
SPEE와 SPWE의 세포 생존율에 대한 영향을 알아보기 위하여 3T3-L1 세포에 시료들을 0, 50, 100 μg/mL 농도로 48시간 처리한 후, MTS assay를 이용하여 측정한 세포 생존율 결과는 다음과 같다(Fig. 1). 측정 결과, SPEE와 SPWE 모두 0, 50, 100 μg/mL에서는 세포 생존율에 큰 영향을 끼치지 않았다.
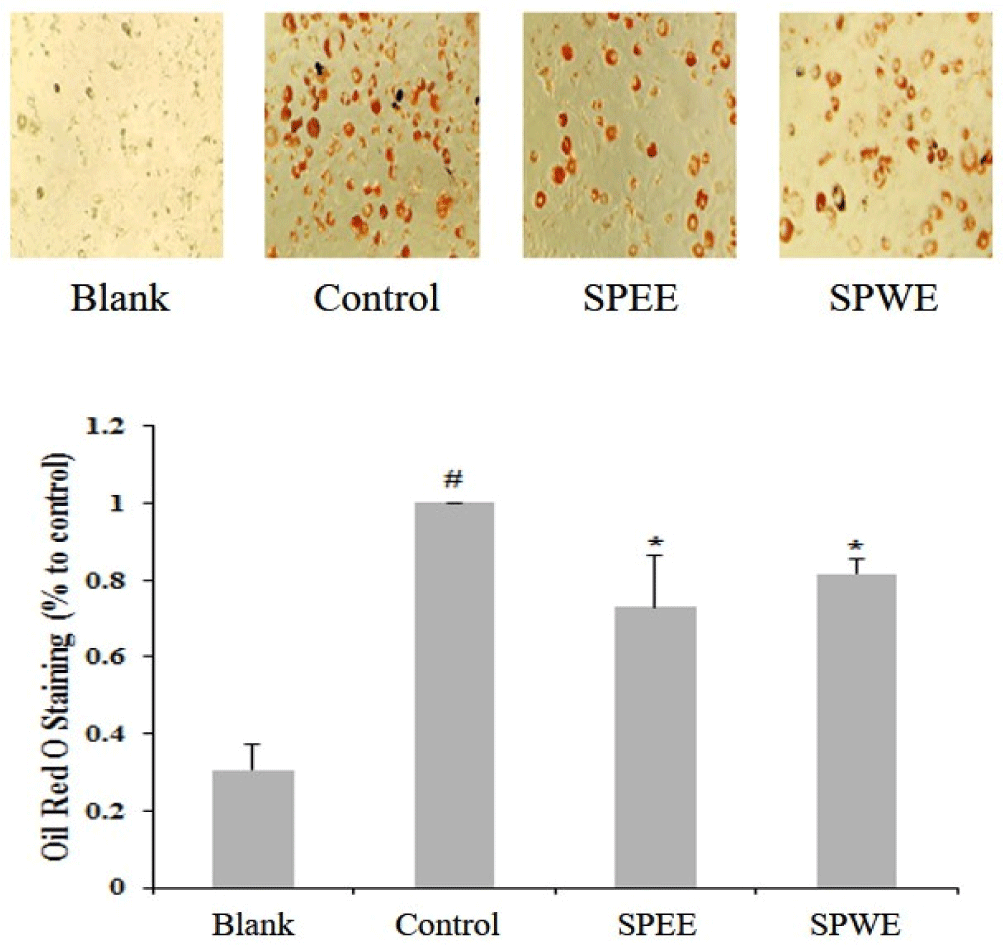
SPEE와 SPWE의 지방세포 분화 억제능을 확인하기 위해 3T3-L1 세포를 adipocyte로 분화시키면서 SPEE와 SPWE를 세포에 처리한 후 Oil red O 염색법을 통하여 지방축적을 비교해 본 결과, MDI 분화 유도제만 처리한 세포에서는 4일째부터 지방구 형성이 관찰되었으며, Oil red O 염색에 의해 adipocyte에서 선명한 붉은색을 나타내어 세포의 분화가 정상적으로 일어나 충분한 지방이 축적된 것을 확인할 수 있었다. Control 대비 SPEE와 SPWE 처리군에서 지방축적이 현저히 감소되었으며, SPEE 처리군이 SPWE 처리군보다 더 감소하였다. 이를 통해 SPEE와 SPWE의 세포 지방축적 억제를 확인하였다(Fig. 2).
페놀성 화합물은 식물계에 널리 분포되어 있는 2차 대사산물로서, 이는 항산화 활성 등 생리활성물질로 잘 알려져 있다(Lee et al., 2011). 총 폴리페놀 함량은 gallic acid를 이용하여 작성한 표준 곡선으로부터 환산하였다. 실험 재료인 SPEE와 SPWE의 총 폴리페놀 함량을 측정한 결과, SPEE는 152.03±5.96 mg gallic acid equivalent (GAE)/g, SPWE는 SPEE의 50% 수준인 81.12±0.30 mg GAE/g으로 SPEE가 더 높은 함량을 가지고 있는 것으로 나타났다(Table 2). 에탄올 추출은 플라보노이드 및 페놀성 화합물과 같은 비극성, 반극성 화합물의 추출 효율을 높이는 것으로 알려져 있다(Dai & Mumper, 2010). Lim 등(2007)의 연구에서 측정된 곰보배추 메탄올 추출물의 총 폴리페놀 함량은 202.35±1.26 mg GAE/g으로 나타났으며, 본 실험에 사용되어진 에탄올추출물 보다 약 25%, 물 추출물은 약 60% 높은 함량을 나타내었다.
| Group | Material | Dose | Material | Dose | n | |
|---|---|---|---|---|---|---|
| 1 | CON | D.W. | - | Glucose | 2 g/kg | 6 |
| 2 | MET | Metformin | 10 mg/kg | Glucose | 2 g/kg | 6 |
| 3 | SPEE | SPEE | 300 mg/kg | Glucose | 2 g/kg | 6 |
| 4 | SPWE | SPWE | 300 mg/kg | Glucose | 2 g/kg | 6 |
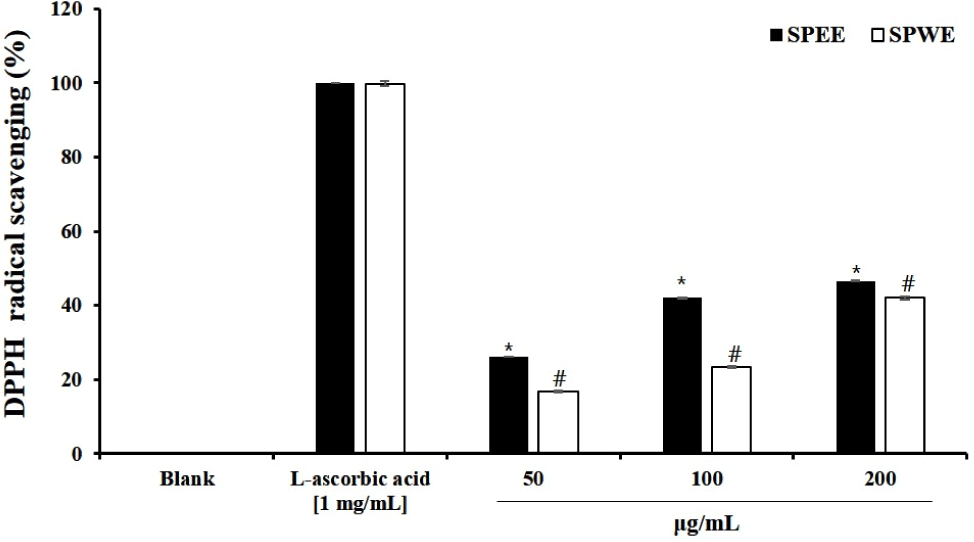
DPPH는 항산화물질과 반응하여 음이온 라디칼이 소거되면서 보라색에서 노란색으로 탈색되는 원리로 항산화 활성을 측정하는데 사용된다(Nam et al., 2015). SPEE와 SPWE의 50, 100, 200 μg/mL 농도에서 DPPH 라디컬 소거 활성을 측정한 결과, 각각 SPEE는 26.17±0.01, 41.96±0.01, 46.64±0.91%로 농도 의존적으로 증가하였다. SPWE 또한 16.67±0.01, 23.96±0.01, 41.96±0.91% 농도 의존적으로 증가하였으며, SPWE보다 SPEE가 더 높은 활성을 나타냈다(Fig. 3). Choi 등(2014)의 연구에서 배암차즈기(곰보배추)잎 에탄올추출물의 DPPH radical 소거능은 250, 500, 1,000 μg/mL 농도에서 각각 24.9±2.5, 40.5±1.1, 57.9±5.8%를 나타내었으며, 농도가 증가함에 따라 유의적인 DPPH radical 소거능을 보인 결과와 유사하였으며, 본 실험에 사용되어진 SPEE보다 낮은 활성을 나타냈다. 플라보노이드는 라디컬 소거 작용을 통해 세포 손상을 예방하며, 이는 산화스트레스와 관련된 만성 질환의 예방에 기여할 수 있다(Heim et al., 2002).
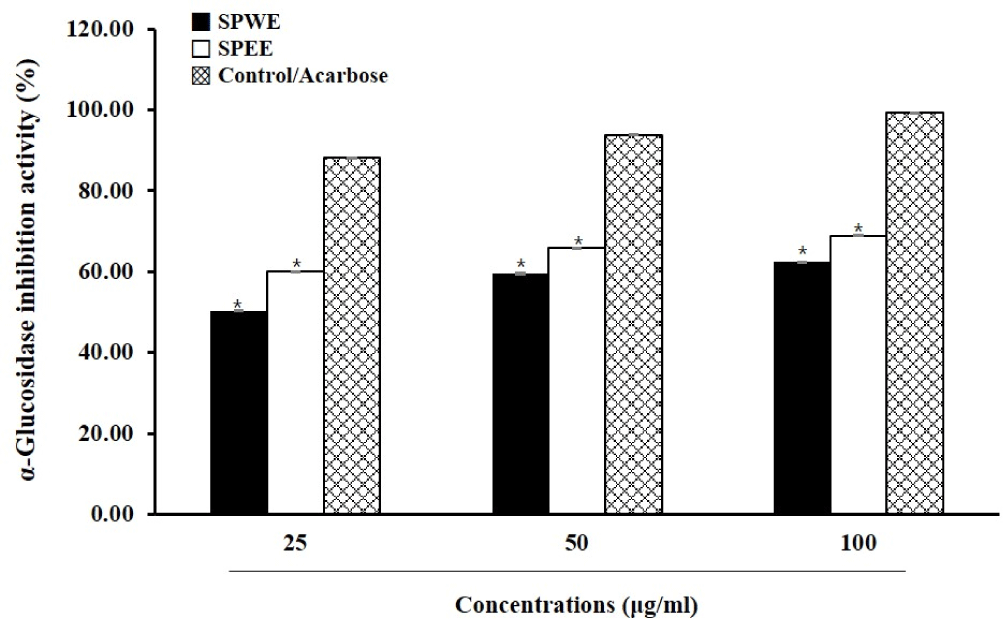
α-Glucosidase는 소장에서 탄수화물 분해를 통해 포도당 흡수를 촉진하는 효소로(Kim, 2000), α-glucosidase에 의한 단당류 생성을 저해함으로써 식사 후 혈당이 급격히 상승하는 증상을 효과적으로 저해할 수 있음을 확인할 수 있다(Park et al., 2012). SPEE와 SPWE의 α-glucosidase의 활성 저해능을 각각 측정한 결과는 다음과 같았다(Fig. 4). SPEE의 경우, 50, 100, 200 μg/mL의 농도에서 활성을 각각 측정한 결과, SPEE는 각각 60.11±0.10, 65.80±0.07, 68.95±0.05% 저해시켰으며, SPWE는 50.37±0.12, 59.57±0.15, 62.50±0.10% 저해하여 농도 의존적으로 감소하였으며, SPWE보다 SPEE 저해 활성이 높게 나타났다. Control인 acarbose를 농도별 처리하였으며, α-glucosidase 저해 활성을 보였다. SPEE가 SPWE에 비해 높은 항산화 활성을 나타낸 것은 플라보노이드와 폴리페놀 함량이 높기 때문인것으로 해석되며, 이는 α-glucosidase 저해 활성과 상관관계가 있는 것으로 사료된다.
C57BL/6 정상 마우스와 streptozotocin으로 당뇨병이 유발된 C57BL/6 마우스에서 SPEE와 SPWE의 당 분해 및 당 흡수를 확인하기 위하여 경구당부검사를 시행한 결과는 다음과 같다(Table 3). 정상모델에서 glucose 경구 투여 30분 후에 미정맥 채혈하여 혈당을 측정한 결과, CON(대조군)의 혈당은 215±10.4 mg/dL로 측정되었고, SPEE군과 SPWE군의 혈당은 각각 177±6.4 mg/dL와 195±6.4 mg/dL로 SPWE 투여군에 비해 SPEE 투여군에서 혈당증가가 감소하였다. 당뇨 모델에서 경구당부하검사 결과, glucose 경구 투여 30분 후에 미정맥 채혈하여 혈당을 측정한 결과 CON군의 혈당은 473±37.7 mg/dL로 측정되었고, SPEE군과 SPWE군의 혈당은 각각 373±14.5 mg/dL와 407±16.6 mg/dL로 SPWE 투여군에 비해 SPEE 투여군에서 더 많이 감소하였다(Fig. 5). Oh 등(2012)의 streptozotocin으로 유도된 당뇨 동물모델에서 야콘추출물에서 OGTT 실험 결과에 의하면 control군의 혈당은 473±29 mg/dL로 측정되었고, GIII군의 혈당은 330±52 mg/dL로 유의하게 감소하였으며, control군과 실험군에서의 혈당 감소 수치가 본 실험과 유사하게 나타내었다.
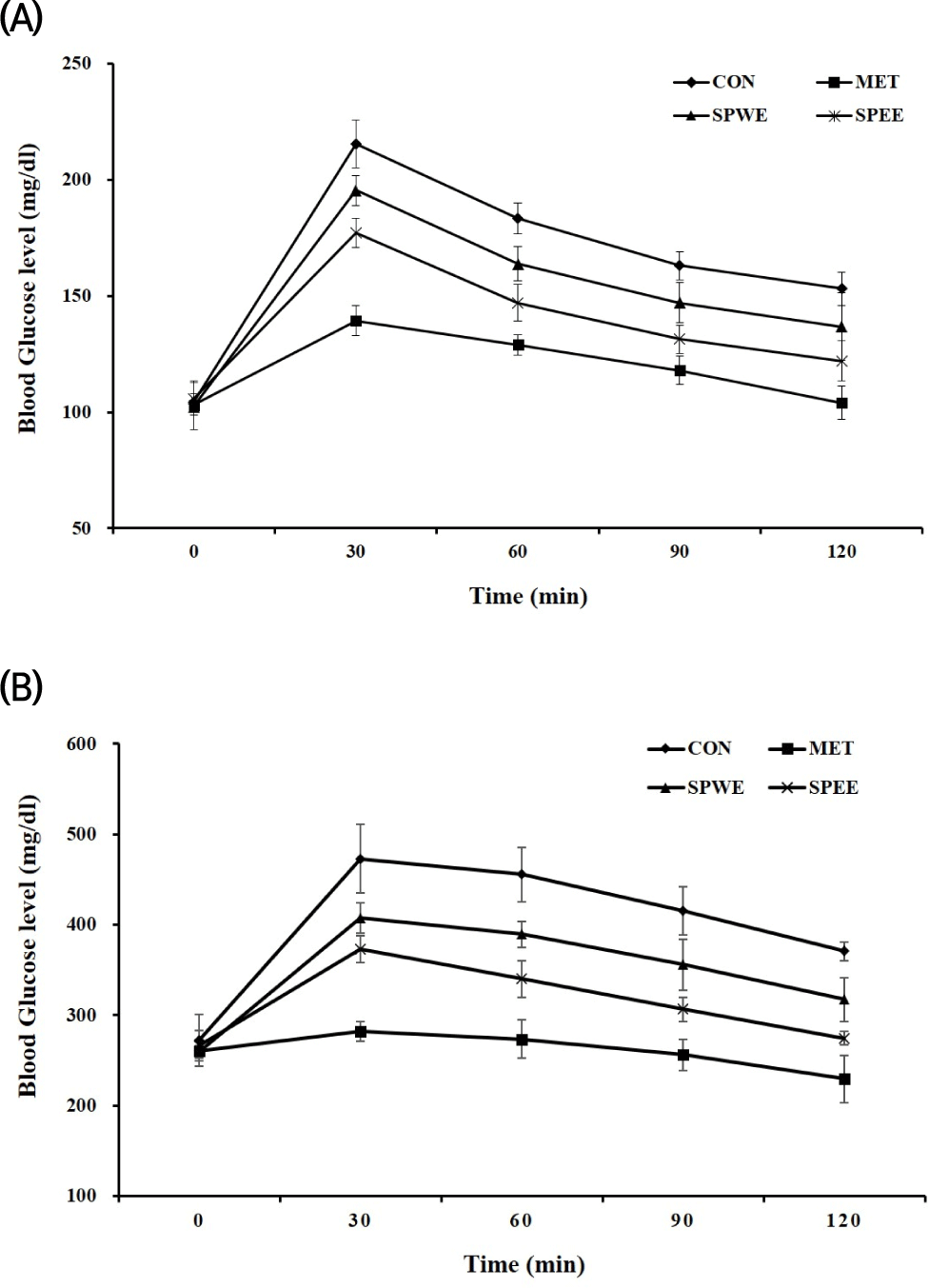
요 약
본 연구는 SPEE와 SPWE의 항산화 활성에 대한 기능성을 확인함과 동시에 혈당 강하 효과를 확인하고자 하였다. 3T3-L1 세포를 이용하여 측정 결과, SPEE와 SPWE 모두 50, 100 μg/mL에서는 세포 생존율에 큰 영향을 끼치지 않았으며, Oil Red O 시약을 사용하여 세포 내 지방생성량은 측정한 결과, 붉게 염색되는 부분이 control 군에 비해 유의적으로 감소되었음을 알 수 있었다. SPEE와 SPWE의 총 폴리페놀 함량을 측정한 결과, SPEE는 152.03±5.96 mg GAE/g, SPWE는 SPEE의 50% 수준인 81.12±0.30 mg GAE/g으로 SPEE가 더 높은 것으로 나타났다. 항산화능을 평가하는 DPPH 라디컬 소거 활성을 50, 100, 200 μg/mL 농도로 측정한 결과, SPEE는 각각 26.17±0.01, 41.96±0.01, 46.64±0.91%, SPWE는 16.67±0.01, 23.96±0.01, 41.96±0.91%로 농도 의존적으로 증가하였으며, SPWE보다 SPEE의 항산화 활성이 더 높은 것으로 나타났다. α-Glucosidase 효소 활성을 측정한 결과, 50, 100, 200 μg/mL의 농도에서 SPEE는 각각 60.11±0.10, 65.80±0.07, 68.95±0.05% 저해시켰으며, SPWE는 50.37±0.12, 59.57±0.15, 62.50±0.10% 저해하여 농도 의존적으로 감소하였으며, SPWE보다 SPEE 저해 활성이 높게 나타났다. C57BL/6 마우스를 이용하여 SPEE에 대해 경구당부하검사 (OGTT)를 한 결과, glucose 경구 투여 30분 후에 정상 마우스에서 SPEE군과 SPWE군의 혈당은 각각 177±6.4 mg/dL와 195±6.4 mg/dL로 SPWE 투여군에 비해 SPEE 투여군에서 혈당증가가 감소하였다. Streptozotocin으로 당뇨를 유발한 마우스에서 SPEE군과 SPWE군의 혈당은 각각 373±14.5 mg/dL와 407±16.6 mg/dL로 SPWE 투여군에 비해 SPEE 투여군에서 더 많이 감소하였다. 투여 후 60분 후부터 SPEE300 군에서 CON군과 비교하였을 때 유의적인 감소를 보였다. 위에 결과들을 종합하여 볼 때 SPEE는 항산화 효과와 혈당강하 효과를 나타내어 혈당 조절 및 비만 예방에 기여할 수 있을 것으로 판단되며, 추가적인 연구를 통해 건강기능식품의 원료나 고부가가치를 창출할 수 있는 식품원료로 사용할 수 있을 것으로 생각된다.
