서 론
느타리(Pleurotus ostreatus)는 느타리버섯과(Pleurotaceae) 느타리속(Pleurotus)에 속하는 버섯 중 하나로 식용 또는 약용으로 장기간 복용하여도 부작용이 거의 나타나지 않아 현재까지 널리 이용되고 있는 버섯 중 하나이다(Kim et al., 2015). 2022년 국내에서 느타리버섯은 가장 넓은 재배면적(151 ha)과 가장 높은 생산량(49,951 ton)을 기록하였다(MAFRA, 2023). 일반적으로 버섯에는 다양한 생리활성 성분들이 함유되어 있으며, 대표적으로 펩타이드와 단백질 등이 다당류에 결합된 당단백질과 다당류의 베타글루칸이 있다(Kim et al., 2019).
베타글루칸(β-glucan)은 D-glucose 단량체가 베타 글리코시드 결합으로 연결된 고분자 다당체이다(Shaheen et al., 2022). 일반적으로 베타글루칸은 식물성 곡류(예: 귀리, 보리)로부터 유래된 베타 1,3/1,4-글루칸과, 진균류(예: 버섯) 및 효모에서 얻어지는 베타 1,3/1,6-글루칸으로 구분된다(Khan et al., 2017). 이처럼 베타글루칸은 공급원에 따라 서로 다른 결합형태와 분지 방식, 분자량, 용해도를 가지게 되며 이는 건강 기능성에도 차이를 준다. 곡류 유래 베타글루칸은 혈중 콜레스테롤 감소, 비만, 당뇨, 심혈관 질환 등에 대한 건강 기능성이 보고되고 있으며, 미생물로부터 추출된 베타글루칸은 항산화, 항암, 면역증진 효과가 있는 것으로 알려져 있다(Song, 2014; Kaur et al., 2019; Kwon et al., 2023). 또한, 베타글루칸은 피부 진정, 재생 및 보습 효과가 있어 화장품 원료로도 많이 사용되고 있다(Du et al., 2014; Sousa et al., 2023).
하지만 베타글루칸의 높은 점성과 분자량은 체내 소화 및 흡수력(Niaz & Mackie, 2024)과 피부 침투력(Kozarski et al., 2023)을 낮추는 요인으로 작용하여 산업적 이용을 제한하고 있다(Lee et al., 2012). 이를 해결하기 위해 과산화수소와 고압증기멸균기를 이용한 베타글루칸의 저분자화(Innofarm, 2012), 효소처리를 통한 베타글루칸의 분자량과 점도 감소(Roubroeks et al., 2001) 등과 같은 연구들이 이어졌으나 최근에는 고분자량의 베타글루칸도 흡수가 가능하며 오히려 저분자화시킴에 따른 건강 기능성 활성의 저해 가능성이 보고되고 있다(Park & Kim, 2012). 따라서, 베타글루칸의 활용도를 높이기 위해서는 저분자화 기술뿐만 아니라 캡슐화 기술을 적용하여 소재의 안정성과 생체이용률을 높이는 방법을 함께 고려해 볼 수 있다.
리포좀은 인지질을 주성분으로 하는 구형 소포체이며, 친수성과 소수성의 기능성 물질을 모두 포집하는데 효과적인 약물 전달 시스템이다(Chun et al., 2013). 리포좀의 구조는 생체막과 유사하여 높은 생체적합성과 피부 친화도를 가진다(Yang et al., 2020). 이로 인해 리포좀은 식품, 제약 및 화장품 분야에서 널리 사용되고 있다(Lee et al., 2018).
리포좀의 제조방법으로는 크게 유기용매를 사용하는 역상 증발(reverse-phase evaporation), 박막 수화(thin-film hydration) 방법과 기계적인 힘을 가하는 균질화(homogenization), 초고압(microfluidization), 초음파 처리(sonication)로 분류된다(Akhavan et al., 2018; Assadpour & Jafari, 2019). 최근, 산업체에서는 독성의 유기용매를 사용하지 않으면서도 리포좀 대량생산공정에 적합한 초고압 및 초음파 균질법을 많이 사용하고 있다(Melchior et al., 2023). 초고압 균질은 유체에 높은 압력을 가하고 이를 좁은 틈으로 통과시킴에 따라 발생하는 전단력(shear force), 공동화(cavitation), 충격(impact)을 통해 유화 및 분산 현상을 일으킨다(Hyun & Chun, 2019). 초음파 균질은 유체에 강한 음파를 가하여 진동을 유발하고 미세 기포가 격렬하게 진동하며 용매 주위에 큰 충격파가 발생하는 추진력으로 리포좀을 생성하게 된다(Yi et al., 2024). 이처럼 서로 다른 원리를 가지고 있는 균질화 방법이나 작동 조건들은 리포좀 제형의 특성과 안정성에 많은 영향을 미치게 되므로 적절한 기계적인 힘을 가하여 안정성이 높은 제형을 개발하기 위한 연구들이 이어지고 있다(Ibišević et al., 2019; Khatib et al., 2019; Melchior et al., 2023).
본 연구에서는 베타글루칸의 열과 알코올에 대한 안정성을 높이기 위한 목적으로 리포좀 제형을 적용하였으며, 다양한 초고압 및 초음파 균질 조건에 따른 베타글루칸 리포좀을 제조하고 이에 대한 저장 안정성을 확인하여 균질화 방법과 조건에 따른 제형의 특성 변화를 관찰하고자 하였다.
재료 및 방법
본 실험에서 리포좀 제조를 위해 사용한 레시틴(LIPOID S75-3, hydrogenated phospholipids from soybean with 70% phosphatidylcholines)은 Lipoids GmbH (Ludwigshafen, Germany)에서 구입하였으며, medium chain triglycerides (MCT) oil (Palm Kernel oil 99.9%, canola oil 0.1%)은 Korea Medical Foods (Seoul, Korea)에서 구입하여 사용하였다. 이와 함께 유상으로 OLIVOIL AVENATE EMULSIFIER (Kalichem, Rezzato Brescia, Italy)와 dl- alpha-Tocopherol (DSM, Kaiseraugst, Switzerland)를 사용하였으며, 1,3-Butylene glycol (COSEEDBIOPHARM, Cheongju, Korea)은 수상으로 사용하였다.
느타리버섯 균주 배양 및 베타글루칸 추출은 Lee et al. (2013)의 방법을 일부 변형하여 사용하였다. 베타글루칸을 추출하기 위해 느타리버섯(Pleurotus ostreatus) 균주를 채집 후 배양하였다. 배양액은 탈지대두분 0.8%(w/v), 설탕 1.5%(w/v), MgSO4 0.01%(w/v), K2HPO4 0.01%(w/v)를 정제수 350 mL에 혼합하여 용해시킨 후 121℃에서 15분간 멸균 후 25℃까지 냉각시켜 실험에 사용하였다. 느타리버섯 균주 5%(w/v)를 멸균된 믹서기(BSP72368, Bamix, Switzerland)로 분쇄 후 25℃ 이하로 식힌 액체 배양액에 넣어 접종하고 배양기(SI-600R, Lab Corporation, Seoul, Korea)를 이용하여 25℃, 100 rpm으로 15일간 배양하였다. 이후 배양액을 멸균된 믹서기로 균질 후 90℃ 정제수를 배양액의 3배수만큼 넣어주고 3시간 동안 침지시켜 베타글루칸을 추출하였다. 이후 배양액을 110 mesh로 걸러낸 후 1,2-Hexanediol (COSEEDBIOPHARM, Korea) 2% (w/v)와 glycerin (COSEEDBIOPHARM, Korea) 20%(w/v)를 혼합하고 5~10℃에서 3일간 저온 침지하여 얻어진 상등액을 베타글루칸 시료로 사용하였다.
느타리버섯 균주의 액체 배양 후 베타글루칸 함량 분석은 건강기능식품공전에 고시된 베타글루칸(제1법 영지버섯자실체추출물) 시험법을 일부 변형하여 분석하였다(MFDS, 2024). 시험용액의 전처리를 위해 베타글루칸 배양액 10 mL와 증류수 10 mL를 혼합한 후 α-amylase (20,000~60,000 U/mL) 0.1 mL를 가하고 0.1 N NaOH를 이용하여 pH 6.9로 조정한 후 진탕항온수조(C-SKW1, CHANGSHIN SCIENCE, Seoul, Korea)를 이용하여 20℃에서 2시간 동안 반응시켰다. 이후, 0.1 N HCl을 이용하여 pH를 5.0으로 맞추고 cellulase (1,600 U/mL) 0.1 mL를 넣어준 후 37℃에서 2시간 동안 반응시켰다. 반응이 끝난 후, protease (600~1,300 U/mL) 0.1 mL를 넣고 0.1 N NaOH를 이용하여 pH 7.5로 맞춘 후 37℃에서 2시간 반응시켰다. 여기에 amyloglucosidase(10,000 U/mL) 0.1 mL를 넣고 0.1 N HCl로 pH를 4.8로 맞춘 후 60℃에서 2시간 동안 반응시켰다. 효소 분해물에 95% 에탄올 40 mL를 가하여 4℃에서 12시간 이상 침전시킨 후 원심분리(12,298×g, 10분)하여 시료의 침전물을 취하였다. 여기에 80% 에탄올 50 mL를 가하여 4℃에서 1시간 동안 침전시킨 후 원심분리(12,298×g, 10분)하였다. 원심분리된 침전물에 증류수 10 mL를 가한 후 침전물을 혼합하여 균질화시키고 이 용액을 증류수로 100 mL 정용한 후, 별도의 희석 없이 시험용액으로 사용하였다. 시험용액 0.2 mL와 증류수 0.8 mL 혼합 후 5% 페놀용액 1 mL를 넣었으며, 이때 D-glucose(표준용액) 1 mL와 5% 페놀용액 1 mL도 별도로 반응시켰다. 각각의 시험관을 10초간 잘 흔들어 섞은 후 황산 5 mL를 가하여 혼합하고 실온에서 20분간 반응시켰다. 이후 분광광도계로 470 nm에서 흡광도를 측정하였으며, 아래의 계산식을 이용하여 베타글루칸 함량을 구하였으며, 본 실험에 사용된 느타리버섯 균주 액체 배양액에 함유된 베타글루칸 함량은 1.31~1.42 mg/mL로 나타났다.
C: 시험용액 중의 glucose 농도 (5 μg/mL)
a: 시험용액의 전량 (100)
b: 희석배수 (1)
S: 시료 채취량 (g) (10)
5: 발색과정의 희석배수
1/1,000: 단위 환산 계수
0.9: 베타글루칸 전환계수(162/180)
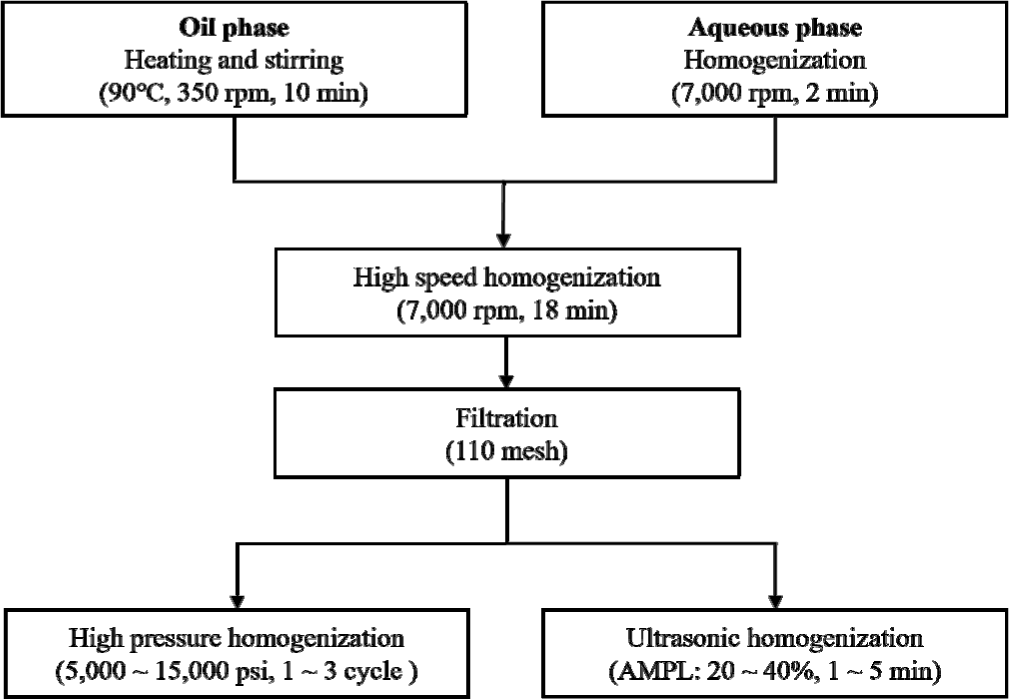
베타글루칸 리포좀의 조성은 Table 1과 같다. 유상은 MCT oil 25.0 g, 대두레시틴 2.5 g OLIVOIL AVENATE EMULSIFIER 1.3 g, dl-alpha-Tocopherol 2.0 g으로 이루어졌으며, 수상은 정제수 42.9 g, 1,3-Butylene glycol 20.0 g, 베타글루칸 6.3 g으로 구성하였다. 베타글루칸 리포좀 제조방법은 Fig. 1과 같다. 먼저, 유상의 재료들을 모두 혼합한 후 90℃에서 350 rpm으로 10분간 가열 및 교반하였다. 수상은 베타글루칸과 1,3-Butylene glycol을 먼저 혼합한 후 100℃의 정제수를 부어주고 초고속 균질기(T25D, IKA, Staufen, Germany)를 이용하여 7,000 rpm으로 2분간 균질하였다. 이후 유상을 수상에 천천히 부어주면서 7,000 rpm으로 18분간 추가로 더 균질하고 110 mesh 천을 이용하여 1회 여과하였다. 이후 초고압 균질(Picomax MN400, Micronox, Seoul, Korea) 과정에서의 압력(5,000, 10,000, 15,000 psi)과 횟수(1, 2, 3회), 초음파 균질(VCX750, Sonics & Materials, Newtown, CT, USA) 과정에서의 진폭(20, 40%)과 시간(1, 3, 5분)을 달리하여 베타글루칸 리포좀을 제조하였다. 리포좀은 상온에서 30일간 보관하며 10일 간격으로 입자크기, 입자분산도, 제타전위, 탁도를 측정하여 안정성을 확인하였다.
베타글루칸 리포좀의 입자특성을 확인하기 위하여 먼저 시료를 증류수에 200배 희석하였다. 희석액을 disposable capillary cell (DTS1070, Malvern Panalytical Ltd., Malvern, UK)에 주입 후 입도분석기 (Zetasizer Ultra, Malvern Panalytical Ltd., Malvern, UK)를 이용하여 입자특성을 확인하였다. 평균 입자크기와 다분산지수(polydispersity index, PDI)는 dynamic light scattering (DLS) 원리에 의해 측정되었으며, 제타전위는 electrophoretic light scattering (ELS) 원리에 의해 측정되었다.
결과 및 고찰
초고압 압력(5,000, 10,000, 15,000 psi)과 균질 횟수(1, 2, 3 cycle)에 따른 베타글루칸 리포좀의 평균 입자크기와 다분산지수는 Fig. 2에 나타내었다. 초고압 균질 조건을 달리한 베타글루칸 리포좀은 5,000 psi에서 1회 균질하였을 때 가장 크기가 큰 평균 입자 (198.47 nm)를 보였으며, 15,000 psi에서 3회 균질하였을 때 가장 작은 평균 입자크기(135.60 nm)를 나타내었다(Fig. 2A). 초고압 균질 압력이 높아질수록, 균질 횟수가 1회에서 2회로 증가함에 따라 리포좀의 평균 입자크기는 유의적으로 감소하는 경향을 보였으나(p<0.05), 균질 2회와 3회 간에는 유의적인 차이를 보이지 않았다(p>0.05). 반면, 초고압 균질기를 통과한 베타글루칸 리포좀의 다분산지수(polydispersity index, PDI)는 모두 0.1 미만의 작은 값을 보였다(Fig. 2B). 이는 입자 분포도에서도 피크의 너비가 좁고 뾰족한 것을 확인할 수 있으며(Fig. 2C~E), 초고압 균질을 통해 입자특성이 우수한 리포좀을 제조할 수 있음을 보여준다.
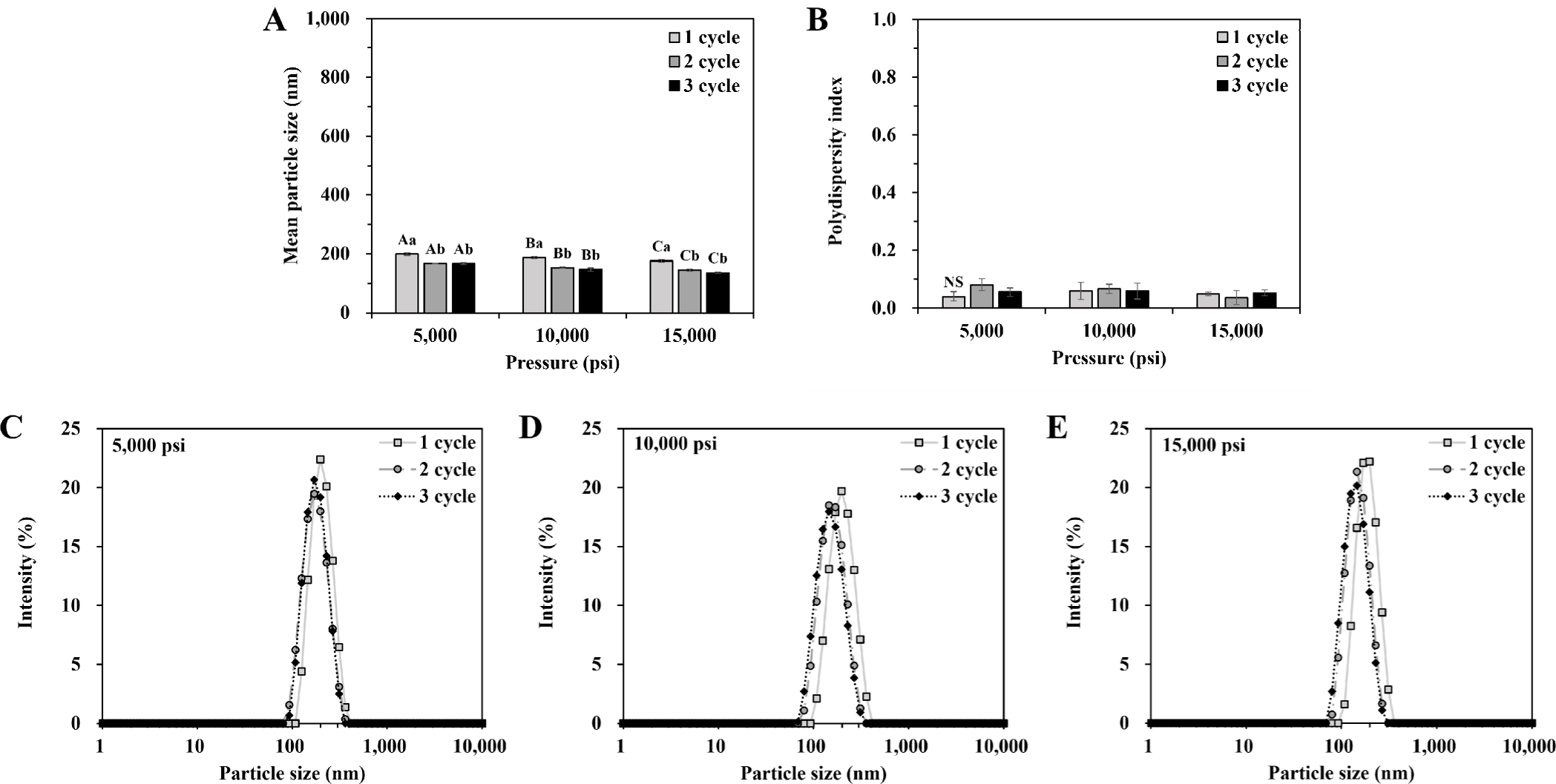
일반적으로 에멀젼 또는 리포좀을 제조할 때 초고압 균질 압력 및 횟수가 증가할수록 유화액의 입자크기는 감소하면서 분산도는 향상되는데, 이는 균질 과정 동안 생성되는 난류, 공동화 및 높은 전단력 등이 입자크기에 영향을 미치기 때문이다(Jo & Kwon, 2013; Jo et al., 2014). 하지만 필요 이상의 에너지는 오히려 제형의 안정성을 저해시키고 입자 간의 재응집을 유발할 수 있으며, 대량 생산 시에는 불필요한 원가 상승으로 이어진다(Tang et al., 2024). Ibišević et al. (2019)은 초고압 균질 횟수가 증가함에 따라 리포좀의 크기와 PDI 값은 감소하는 경향을 보였으나, 5회 이상 균질 시에는 유의미한 차이를 보이지 않았다고 하여 본 연구와 유사한 결과를 보였다.
Microfluidizer를 이용하여 콜로이드 입자의 크기를 작게 만들고 분산시키는 공정은 상대적으로 좁은 입자분포도를 가지는 나노 사이즈의 입자를 만들 수 있으며, 이때 압력과 균질 횟수는 리포좀의 입자특성과 안정성에 큰 영향을 준다(Jo et al., 2014; Tang et al., 2024). 하지만 초기 유화액의 점성이 높거나 큰 입자가 존재할 경우 높은 전단력과 공동화 현상이 발생하지 않아 입자크기의 감소 및 분산 안정성 향상 등과 같은 효과를 기대하기에는 어려움이 있다(Hyun & Chun, 2019). 본 연구에서는 초고압 균질을 진행하기에 앞서 수상과 유상 혼합 후 초고속 균질기를 이용하여 1차 균질을 진행하였고, 이를 초고압 균질기에 통과시켜 베타글루칸 리포좀을 제조함으로써 제형의 안정성이 높은 리포좀을 제조할 수 있었던 것으로 생각된다.
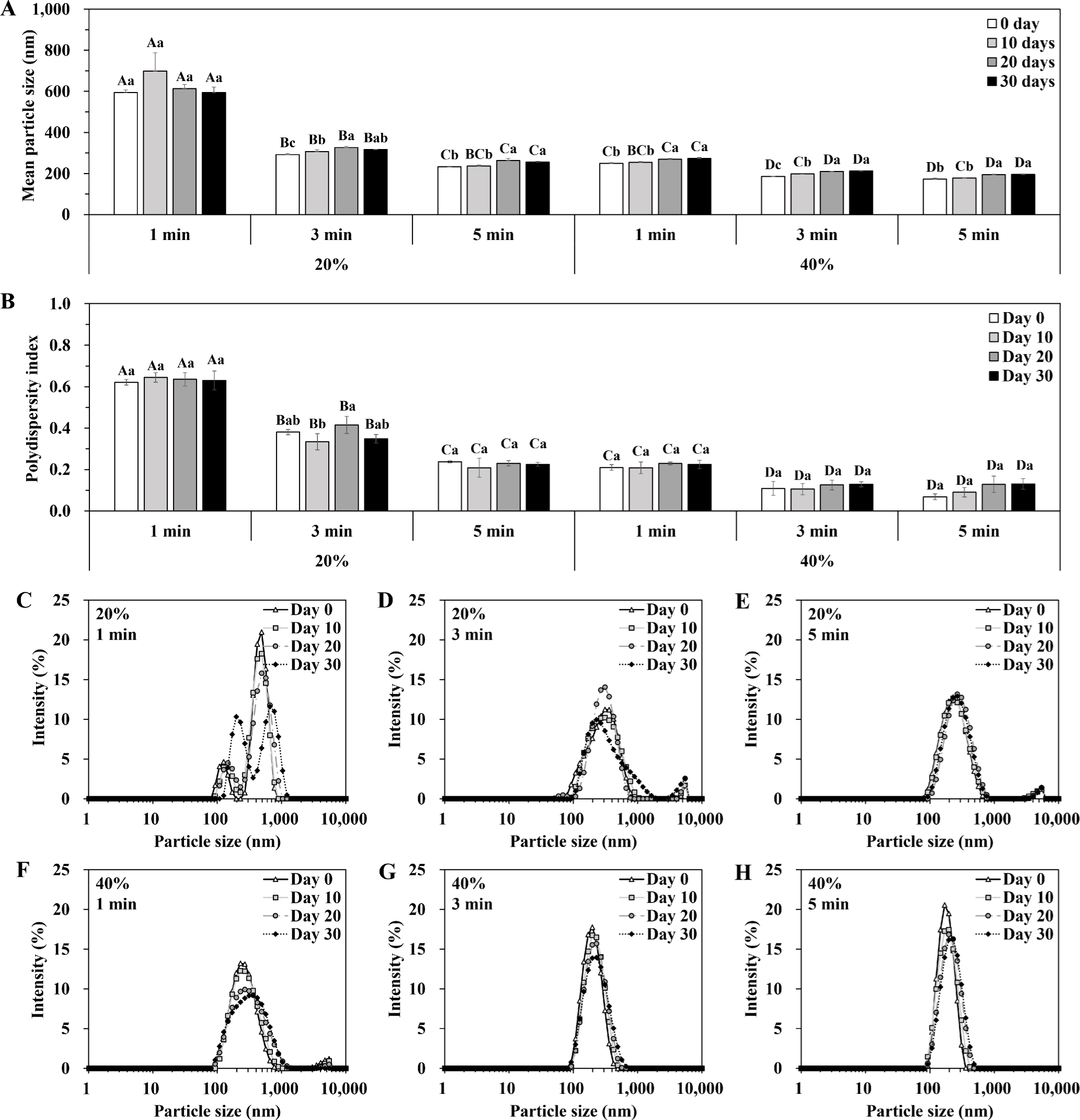
초음파 균질 진폭(amplitude, AMPL)과 시간에 따른 평균 입자크기와 다분산지수는 Fig. 3과 같다. 초음파 균질 진폭(20, 40%) 및 시간(1, 3, 5 min)에 따른 베타글루칸 리포좀의 평균 입자크기는 172.47~594.63 nm로 초고압 균질(135.60~198.47 nm)보다 큰 사이즈의 입자들이 주로 관찰되었다(Fig. 3A). 특히, 가장 낮은 진폭과 짧은 시간으로 초음파 처리(AMPL 20%, 1 min) 한 리포좀은 유의적으로 가장 큰 입자크기(594.63 nm)와 높은 PDI (0.621)를 보였으며, 입자분포도에서는 약 100 nm와 700 nm대에서 피크 2개가 확인되었다(Fig. 3). PDI는 평균 입자크기와 함께 나노 현탁액의 중요한 속성으로, 물리적-화학적 안정성, 용해도, 방출 속도, 탁도에 영향을 주는 것으로 알려져 있다(Zhang et al., 2011). 일반적으로 PDI가 0.3 이하일 때, 균일한 크기의 입자가 주로 존재하는 단분산상(monodisperse phase), 0.3에서 0.6 사이는 중분산상, 0.6 이상은 다양한 크기의 입자가 고루 존재하는 다분산상(polydisperse phase)으로 판단하며, 높은 PDI 값은 입자 간의 응집이 발생하였음을 의미하기도 한다(Chun et al., 2017; Hyun & Chun, 2019; Yi et al., 2024). 본 연구에서는 초음파 진폭 20%에서 3 min 이하로 처리한 리포좀에서 상대적으로 높은 PDI값을 가지는 것으로 나타났다. 이는 초음파 균질과 같은 고에너지 균질화법을 적용하더라도 적절한 세기의 에너지가 가해져야만 안정한 상태의 리포좀을 제조할 수 있음을 보여준다.
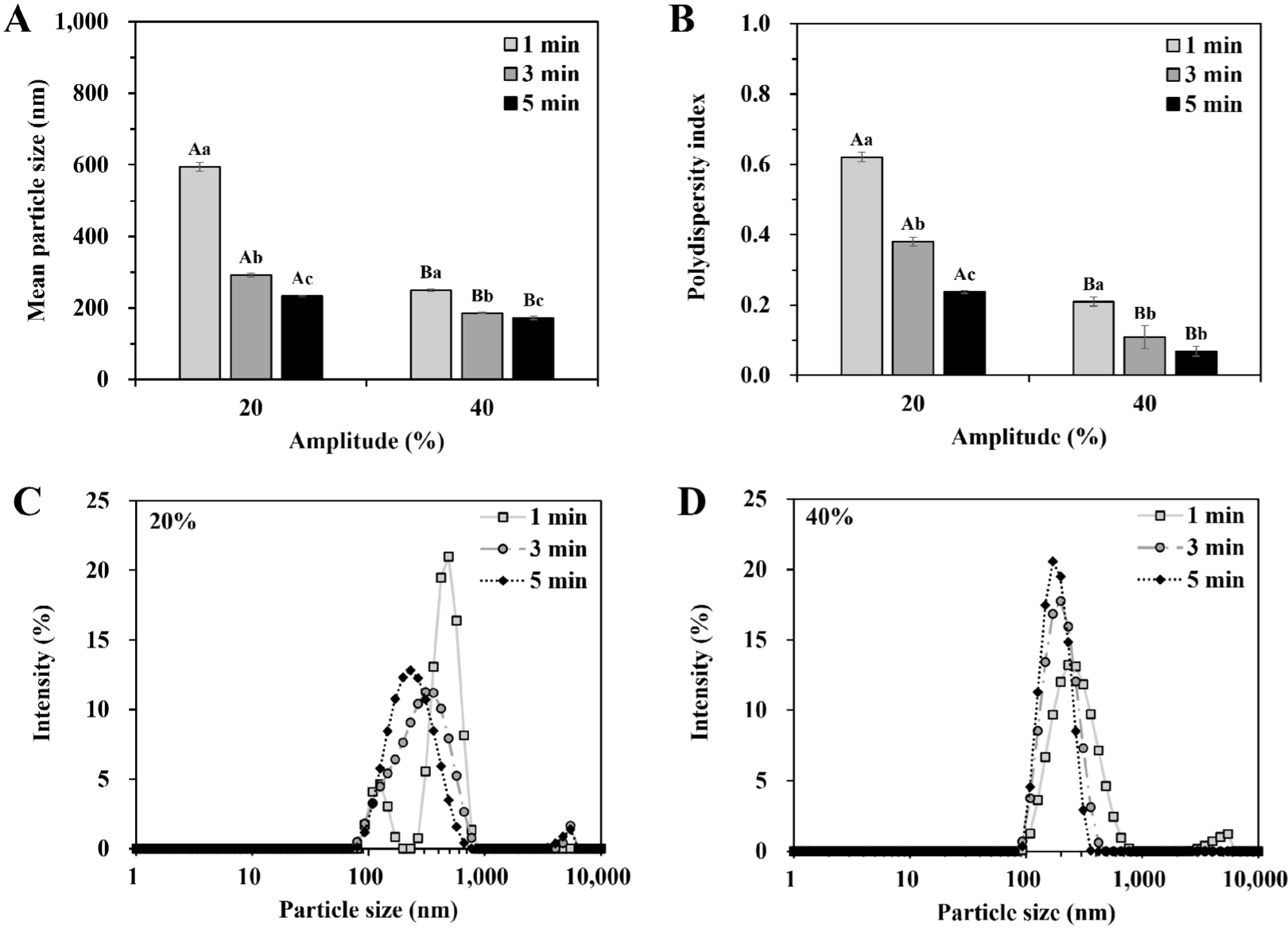
초음파 균질기는 공동화 효과로 콜로이드 시스템의 입자를 작고 균일하게 만들 수 있는 효과적인 장비 중 하나이다(Akbas et al., 2018). Probe 형태의 초음파 균질기는 균질, 분산, 유화, 세포 파괴 등의 목적으로 주로 사용되고 있으며, 일정 시간 동안 입자의 응집(aggregation)과 합일(coalescence) 현상을 억제하여 미세 입자의 안정성을 높일 수 있는 것으로 알려져 있다(Jung et al., 2022).
콜로이드 시스템에서 제타전위는 입자의 전기적 전하를 간접적으로 측정한 것이며, 절댓값이 클수록 입자 간의 반발력이 높아 장시간 안정한 상태를 유지할 수 있는 것으로 알려져 있다(Chun et al., 2017; Yang et al., 2020). 초고압 균질 베타글루칸 리포좀의 제타전위와 탁도는 Table 2와 같다. 초고압 균질 압력과 횟수를 달리한 리포좀의 제타전위값은 –58.53~–48.52 mV의 범위로 강한 음전하를 띄는 것으로 나타났으며, 압력이나 균질 횟수에 따른 뚜렷한 차이를 보이지는 않았다. 반면, 탁도의 경우 압력과 균질 횟수가 증가함에 따라 유의적으로 감소하는 결과를 보이며(p<0.05), 5,000 psi에서 1회 통과한 리포좀은 가장 높은 값(0.839)을, 15,000 psi에서 3회 통과시킨 것은 가장 낮은 값(0.243)을 나타내었다. 이러한 결과는 초고압 균질 압력과 통과 횟수가 리포좀의 탁도에 큰 영향을 주는 것으로 볼 수 있다.
Melchior et al. (2023)은 초고압 균질 압력(50~150 MPa)과 횟수를 달리한 quercetin 나노 리포좀의 탁도는 압력과 횟수가 증가함에 따라 0.720에서 0.056으로 크게 감소하였으나, 제타전위는 유의미한 차이를 보이지 않고 –20.04~–18.50 mV의 범위를 가진다고 하였다. 이처럼 초고압 균질 압력과 횟수는 리포좀의 입자크기와 분포도, 탁도에 많은 영향을 주지만 제타전위값에는 큰 영향을 주지 않는 것으로 보여진다.
베타글루칸 리포좀은 초음파 균질 시 초고압 균질(–58.53~–48.52 mV)보다 대체로 더 강한 음전하(–70.85~–54.57 mV)의 제타전위값을 나타내었으나, 초음파 진폭의 세기가 높아지고 처리시간이 길어질수록 제타전위의 절댓값은 감소하는 경향을 보였다(Table 2). Khatib et al. (2019)은 초음파 균질을 이용하여 lupulon과 xanthohumol 리포좀을 제조하였으며, 이때 초음파 세기가 증가할수록 제타전위는 점차 약한 음전하를 띄었다고 하여 본 연구와 유사한 결과를 보였다. 베타글루칸 리포좀이 음전하를 띄는 것은 레시틴 이중층의 친수성 머리에 해당하는 극성 부분(인산염)의 영향을 받았기 때문이다(Chun et al., 2013). Beltrán et al. (2020)은 균질 방법이 나노리포좀의 물리적 안정성에 미치는 영향을 확인하였는데, 초고압 균질을 통해 가장 작은 크기(100.3 nm)의 리포좀을 형성하였으나 제타전위는 초음파 균질 시 가장 강한 음전하(–55.9 mV)를 보였다고 하여 본 연구와 유사한 경향을 보였다. 이는 초고압 균질보다 상대적으로 낮은 강도의 물리적 힘으로 리포좀을 형성하는 초음파 균질의 경우 리포좀의 구조가 덜 압축되어 더 큰 입자크기를 가지며, 음전하를 띠는 인지질 성분이 표면에 고르게 노출될 가능성이 높기 때문이다.
초음파 균질 진폭이 20%일 때, 베타글루칸 리포좀은 처리시간에 따른 큰 차이를 보이지 않고 1.5 이상의 높은 탁도를 보였다. 하지만 진폭 40%의 경우 처리시간이 증가할수록 리포좀의 탁도는 유의적으로 감소하는 경향을 보여 5 min 처리 시에는 0.628로 가장 낮은 값을 보였다. Akbas et al. (2018)은 균질 방법을 달리한 캡사이신 나노 에멀젼을 제조하고 이에 대한 탁도를 확인하였으며, 초음파 균질(0.7~2.5) 시 초고압 균질(<0.5)에 비해 유의적으로 높은 값을 나타내었으며, 이는 초음파 처리 직후 큰 입자가 존재하거나 측정 과정 동안 빠른 속도로 응집이 발생하였기 때문으로 보고하였다.
초고압 또는 초음파 균질 조건을 달리하여 제조한 베타글루칸 리포좀의 저장 안정성을 확인하기 위해 상온에서 30일간 보관하면서 10일 간격으로 리포좀의 입자특성과 탁도를 확인하였다.
초고압 균질 압력과 횟수에 따른 입자크기의 특성은 Fig. 4, 초음파 균질 진폭과 시간에 따른 입자크기의 특성 변화는 Fig. 5와 같다. 초고압 균질 조건을 달리한 리포좀의 입자크기는 저장 기간이 증가할수록 조금씩 증가하는 경향을 보였으나, 유의미한 차이를 보이지는 않았으며, 135.60~209.07 nm의 범위로 작은 크기를 유지하는 것으로 나타났다. 또한, 저장 30일까지 0.2 미만의 PDI 값을 유지하며 단분산상의 모습을 유지하였다(Fig. 4B). 5,000 psi에서 1회 균질한 베타글루칸 리포좀의 경우 제조 직후에 비해 저장 10일차부터 그래프의 피크가 약간 완만해지기는 하였으나, 평균 입자크기는 198.5~209.1 nm의 범위를 가지며 급격한 변화를 보이지는 않았다(Fig. 4C). 반면, 초음파 균질을 통해 제조한 베타글루칸 리포좀의 입자분포도는 낮은 진폭(20%) 및 짧은 처리시간(1분)에서 그래프의 피크가 2개 이상 관찰되거나 피크의 너비가 넓은 다분산상의 모습을 보였다(Fig. 5C~F). 제조 직후 상대적으로 입자크기가 크거나 PDI가 높은 경우 저장 기간이 증가함에 따라 더 불안정한 입자특성을 보이는 것으로 관찰되었다. Choi et al. (2017)은 레스베라트롤 나노에멀젼의 여러 구성 요소(계면활성제, 생체고분자, 지질 등)에 의해 결정되는 초기 입자크기가 에멀젼의 저장 안정성에 영향을 줄 수 있다고 하였다. 본 연구에서도 초고압 및 초음파 조건에 따라 결정되는 리포좀의 초기 입자크기가 저장 안정성에 많은 영향을 주는 것으로 생각된다. 또한, 대두 레시틴으로 제조된 리포좀은 일정 기간동안 물리적 안정성을 유지할 수 있으며, 상온에서 보관하였다는 점에서 베타글루칸 리포좀의 입자특성이 크게 변하지 않은 것으로 보여진다(Imran et al., 2015).
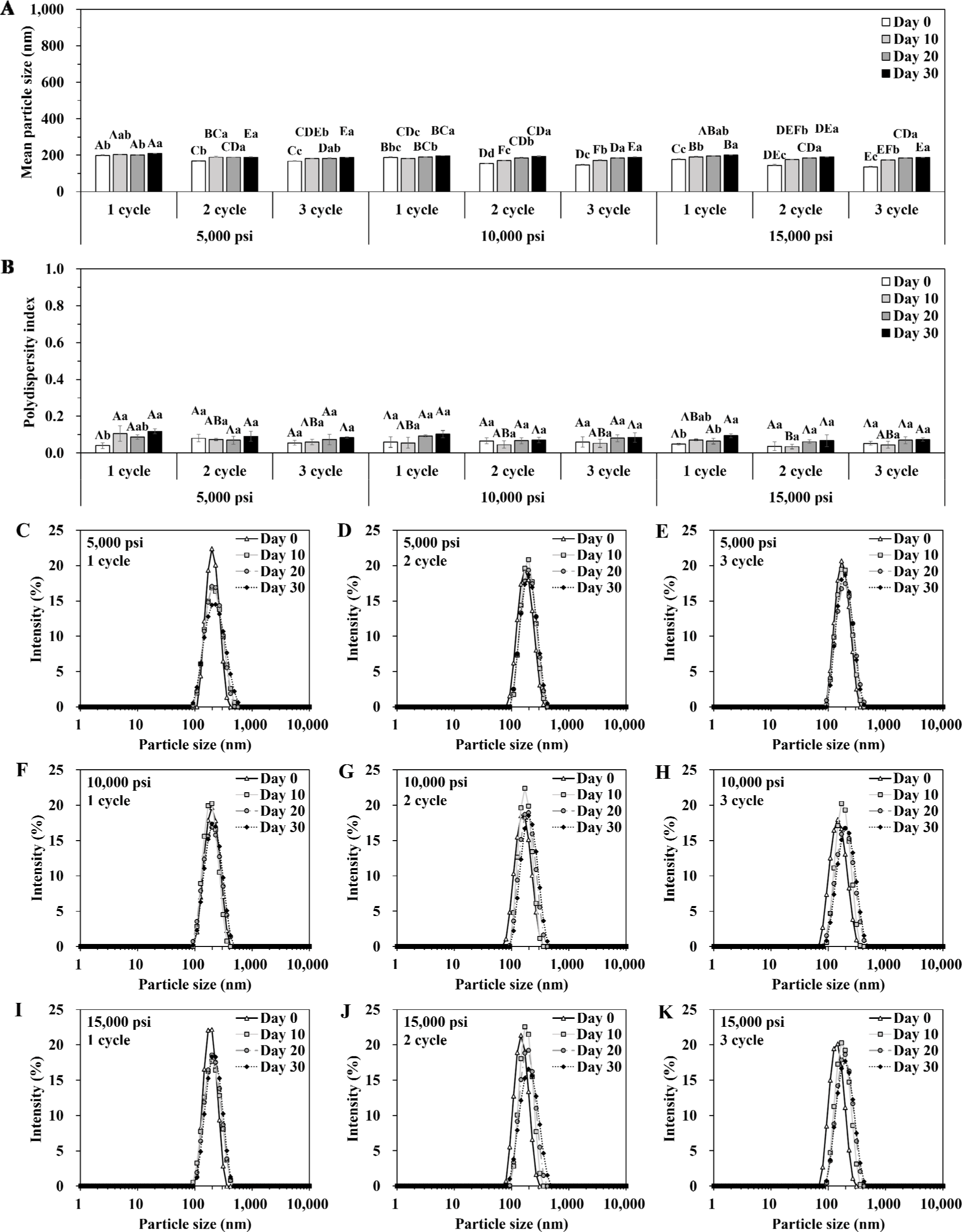
초고압 및 초음파 균질 조건을 달리한 베타글루칸 리포좀의 제타전위값은 저장 30일까지 모두 강한 음전하(–72.68~–47.26 mV)를 유지하였다(Table 3). 반면, 저장 기간이 증가함에 따라 리포좀의 탁도는 계속해서 증가하는 경향을 보였으며(Table 4), 대부분 저장 30일차에서 유의적으로 가장 높은 탁도 값을 보였다(p<0.05). 특히, 높은 진폭(40%)에서 오랜 시간(3, 5 min) 처리한 리포좀은 저장 30일까지 1.2 미만의 탁도를 유지하였으나, 그 외의 조건에서는 1.6 이상의 높은 값을 나타내었다. 탁도는 현탁액에서 입자의 빛 산란을 나타내는데 사용되는 지수이며, 리포좀막의 용해도와 입자 안정성을 확인할 수 있는 효과적인 방법으로 알려져 있다(Joy et al., 2023). Bi et al. (2023)은 리포좀의 입자크기가 증가함에 따라 탁도도 증가하였다고 하여 본 연구와 유사한 경향을 확인하였다.
요 약
본 연구에서는 베타글루칸의 식품 및 화장품으로서의 활용도를 높이기 위하여 초고압 및 초음파 균질기를 이용하여 베타글루칸을 리포좀 제형에 포집하였으며, 이에 대한 입자특성과 탁도를 확인하였다. 초고압 균질 압력(5,000, 10,000, 15,000 psi)과 횟수(1, 2, 3 cycle)를 달리하여 제조한 베타글루칸 리포좀의 평균 입자크기는 135.60~198.47 nm의 범위를 보였으며, 균질 압력과 횟수가 증가함에 따라 입자크기는 점차 작아지는 경향을 보였으나, 균질 2회 이상부터는 유의미한 차이를 보이지 않았다(p>0.05). 또한, PDI값은 모두 0.1 미만으로 단분산상의 모습을 나타내었다. 초음파 균질 진폭(20, 40%)과 시간(1, 3, 5 min)을 달리한 베타글루칸 리포좀의 평균 입자크기는 172.47~594.63 nm로 초고압 균질 리포좀보다 큰 입자들이 주로 관찰되었으며, 특히 20%에서 1 min 처리 시 높은 PDI값(0.621)을 나타내며 다양한 크기의 입자가 존재하는 것으로 나타났다. 상온에서 30일간 저장하면서 관찰한 베타글루칸 리포좀의 입자특성과 탁도 변화는 제조 직후 관찰된 특성과 밀접한 관련이 있는 것으로 나타났다. 본 연구에서는 초고압 균질을 통해 얻어진 베타글루칸 리포좀의 경우 저장 30일까지 큰 변화를 보이지 않았으나, 초음파 균질 진폭의 세기가 낮거나 처리시간이 짧은 경우 저장 기간이 증가함에 따라 평균 입자크기와 탁도가 유의적으로 증가하는 경향을 보였다(p<0.05). 결과적으로, 본 연구에서는 적절한 세기의 초고압 및 초음파 균질은 베타글루칸 리포좀의 물리적 안정성을 높일 수 있음을 확인하였다. 더 나아가, 다양한 외부환경(pH, 염 농도, 온도, 냉 · 해동 등)에 대한 리포좀의 안정성을 확인하고 생체이용률 및 경피 흡수 정도를 검토하는 후속 연구가 필요할 것으로 생각된다.