서 론
일반적으로 생체활성 펩타이드(bioactive peptide)는 식품 단백질에서 추출되며 건강증진의 목적으로 인체에 흡수되 어 질병을 예방하거나 생리활성 시스템을 조절하는 등 여 러가지 유익한효과를 가지고 있다. 생리활성 펩타이드의 서열에 따라 다양한 기능이 있으며, 대표적으로는 항산화, 항비만, 항고혈압, 항혈청, 항균 및 면역조절에 관여한다 (Hartmann & Meisel, 2007;Gómez-Guillén et al., 2011). 이러한 생리활성 펩타이드는 일반적으로 3 - 20개의 아미노 산 잔기를 포함하여, 서열이 기존 모단백질 내에 유지되는 동안 비활성 상태를 유지한다(Jo et al., 2019;Jo & van der Schaaf, 2021). 그러나, 이들은 식품 가공(특히, 가열) 동안 일부 분해되거나 섭취 후 소화과정동안 단백질 분해 효소에 의해 가수분해되면 생리활성 펩타이드로써의 긍정 적 효과를 저해시킬 수 있다.
최근 소비자들이 건강과 미용에 대한 관심이 높아지고 있는 가운데 생리활성 펩타이드 등의 기능적 특성과 관련 된 연구가 진행되고 있다. 여러 연구를 통하여 단백질 가 수 분해물로부터 얻어진 펩타이드는 주름 개선, 보습 증진 을 나타낼 수 있는 잠재적인 소재로 활용되고 있으며, 대 표적인 것이 콜라겐 가수분해물이다(Moskowit, 2000;Lee, 2007;Shigemura et al., 2009). 그러나 펩타이드와 같은 기 능성 물질들은 빛, 산소, pH, 온도 등의 외부환경으로부터 영향을 받아 가공 및 저장 보관에 따라 안정성이 저하되어 생체 내에서 활성이 감소하게 된다. 이러한 문제를 해결하 기 위한 캡슐화 기술(encapsulation)은 내부에 미립자 상태 의 기능성 물질을 피복 물질(wall material)로 감싸 유용 성분을 보호 및 보존하는 역할을 한다(Han et al., 2003;McClements, 2014).
기존 연구에서는 펩타이드와 같은 수용성 기능성 물질은 지질 미립자 운반체인 리포좀을 통해 캡슐화되었다 (Heurtault et al., 2003;Mainardes & Silva, 2004). 하지만 리포좀은 함유하고 있는 인지질이 화학적으로 불안정하여 산화적 분해가 쉽게 일어나고, 막 자체가 물리적 불안정성, 극히 낮은 포집 효율의 단점을 지니고 있다. 본 연구에서 이러한 단점을 보완하기 위하여 리포좀의 대체제로 W/O/W (water in oil in water: W/O/W) 형태의 이중 에멀젼을 통 해 수용성 물질을 캡슐화 가능하다고 예측하였다. 이중 (W/O/W) 에멀젼은 내부 수상(W)과 유상(O)으로 이루어진 단일(water in oil: W/O) 에멀젼 이 외부 수상에 분산되어 있는 형태이다(McClements et al., 2007). 이중 에멀젼은 구조적인 특성으로 인해 친수성, 지용성 유용성분을 모두 포집 가능 할 뿐만 아니라 동시 전달 가능하여 생리활성 물질 상호간의 시너지 효과를 높일 수 있다(McClements et al., 2007;Cofrades et al., 2013). 하지만, 이중 에멀젼은 유상(O)과 수상(W) 사이의 높은 계면장력을 지니고 있어 열역학적으로 불안정하며, 유상의 특성에 따라 이중 에멀 젼의 물리적 안정성에 영향을 미치게 된다.
따라서 본 연구의 목적은 서로 다른 유상(옥수수유, 팜유, MCT유, 레몬유)에 따른 펩타이드 함유 이중 에멀젼을 최 적화하고 이들의 물리적 안정성을 평가하였다. 또한 서로 다른 저장조건에서 이중 에멀젼으로부터 펩타이드 방출효 과를 확인하고자 하였다.
재료 및 방법
본 연구에서는 이중(W/O/W) 에멀젼의 유상인 옥수수유 (Corn oil (CO), Daesang, South Korea), 팜유(Palm oil (PO), Sigma-Aldrich, USA), MCT유(Medium chain triglycerides oil (MO), Medifood TM, South Korea), 레몬 유(Lemon oil (LO), Sigma-Aldrich, USA)을 사용하였다. 친유성 유화제로서 PGPR (Polyglycerol polyricinoleate 9090, PT. Muslim Mas, Indonesia)과 친수성 유화제로서 Tween 80 (Polysorbate 80, Samchun pure chemical co., Ltd, South Korea)을 사용하였으며, 포집물질로써 콜라겐 펩타이드(3 kDa, Naticol 4000, Weishardt International, France)을 준비하였다. 그 외 모든 시약은 분석용 등급을 사용하였다.
펩타이드 함유 에멀젼은 Jo & van der Shaaf (2021)의 선행논문을 일부 참고하여 제조공정을 확립하였다. 펩타이 드 함유 단일(W/O) 에멀젼을 제조하기 위하여 분산상으 로 5% (w/w) 펩타이드, 1% (w/w) NaCl, 그리고 0.02% (w/w) sodium azide를 용해시켜 준비하였다. 단일 에멀젼 에서의 연속상인 유상은 5% (w/w) PGPR을 서로 다른 오 일(옥수수유, 팜유, MCT유, 레몬유)에 용해시켰다. 분산상 (W: 내부수상)과 연속상(O)은 2:3 비율로 프로펠러 균질기 (400 rpm, Propeller stirrer, Chang shin scientific co., Ltd, South Korea)를 통해 약 3분 간 혼합한 후 초고속 균질기 (high-speed homogenizer (15,000 rpm, IKA T25 digital, Ultra-turrax, Germany)를 이용하여 추가 3분 동안 균질하 여 1차 단일 에멀젼을 제조한다. 2차 균질은 초고압균질기 (microfludizer, Picomax processor MN 400, Micronox Inc, South Korea)를 이용하여 2,000 bar에서 2회 통과시킨 후 최종적으로 펩타이드 함유 단일 에멀젼을 제조한다.
펩타이드 함유 이중(W/O/W) 에멀젼의 제조된 단일(W/O) 에멀젼과 외부 수상(W)을 1:1로 혼합한 후 균질한다. 이 때, 외부 수상은 1% (w/w) Tween 80을 포함한다. 준비된 단일 에멀젼과 외부수상은 프로펠러 균질기를 통해 약 3분 간 혼합한 후 초고속 균질기를 이용하여 추가 3분 동안 균질한다. 그 후에 초고압 균질기를 이용하여 500 bar에서 1회 통과시켜 최종 펩타이드 함유 이중 에멀젼을 제조한다.
단일 에멀젼의 입자 크기는 2% (w/w) PGPR로 200배 희석한 후 초음파 세정기(SD-250H, MUJIGAE Co. Ltd., South Korea) 40 KHz/150W에서 3분간 분산시킨 후 입도 분석기(Zeta sizer Nano ZS 90, Malvern, USA)를 이용하 여 동적 광산란(Dynamic Light Scattering) 방법으로 측정 하였다. 수상(W)의 굴절율은(Refractive Index) 1.333, 유상 (O)의 굴절율은 1.472로 설정하였다. 산출된 값은 Zaverage (nm)로 나타내었고, 입자크기 측정은 3회 반복하 였다.
이중 에멀젼의 입자 크기는 입도분석기(Master sizer Master X, Malvern, USA) 챔버에 시료를 한 방울씩 떨어 뜨려 농도의 희석 정도가 10에서 15%으로 설정한 후 입 도분석기를 이용하여 측정하였다. 이때 입자 크기는 시료 부피의 50%가 존재하는 곡선 부분 아래에서의 최대의 입 경인 D50으로 나타내었다. 이중 에멀젼의 제타전위는 증류 수로 적절히 희석한 후 입도분석기(Zeta sizer Nano ZS 90, Malvern, USA)를 이용하여 측정하였다.
제조된 에멀젼은 50mL 바이얼 공병(지름 =30mm, 높이 = 110 mm)에 담아 상온 보관하였다. 에멀젼의 크림화 수치 (CI%)는 식 eq. 1에 제시하였다.
[H: 크림화된 상층 높이, H0: 제조 직후 에멀젼 높이]
유변학적 물성을 평가하기 위해 에멀젼 점도는 modular compact rheometer (MCR 302, Anton pear, Austria)를 이 용하여 측정하였다. 점도 측정을 위한 probe의 지름은 50 mm, 기울기 2도인 C P50- 2를 사용하였다. 실험 온도는 25°C로 일정하게 유지하며 전단 속도(shear rate) 0.1부터 1000 s-1까지 변화를 주어 에멀젼의 점도를 3회 반복 측정 하였다.
유상(옥수수유, 팜유, MCT유, 레몬유)과 수상(W)간의 계 면장력은 Tensiometer (Sigma 703D, Sigma-Aldrich, USA) 를 이용하여 측정하였다. 이 때, 증류수의 표면장력은 72.15 mN으로 측정되었다. 유상은 5% (w/w) PGPR 함유 유상 및 함유하지 않은 순수한 유상으로 사용되었고, 수상 (W)은 5% 펩타이드를 포함한다. Du Nőuy Ring Method 이론을 이용하여 계면장력 값을 산출하였으며, 각각의 측 정은 3회 반복 실시하였다.
서로 다른 유상(옥수수유, 팜유, MCT유, 레몬유)에 의해 제조된 펩타이드의 포집효율은 UV/VIS Microplate Spectrophotometer (Multiskan Go, Thermo scientific, USA) 이용하여 측정하였다. 이중 에멀젼 12 g을 50 mL conical tube에 담아 15,000 rpm, 4°C에서 90분 동안 원심분리기 (Centrifuge, Labogene 1736R, GYROZEN Co. Ltd., South Korea)를 이용하여 크림화된 층과 세럼 층으로 분리하였다. 유리된 펩타이드가 포함한 세럼층은 5mL 주사기를 이용 하여 추출한 후 0.45 μm syringe filter (13 mm, BioFACT TM, South Korea)로 여과시켰다. 유리된 펩타이드의 양을 측정하기 위해 Lowry protein assay 방법을 이용하여 펩타 이드 포집 효율(EE%)을 계산하였으며, 그 산출식은 다음 과 같다(ep. 2).
[A0: 총 펩타이드 함량, A: 유리된 펩타이드 함량]
또한 에멀젼 시료의 저장은 4°C, 25°C, 37°C, 60°C 인큐베 이터에서 각각 보관한 후 7일마다 유리된 펩타이드 함량을 산출하였다. 이때 누적된 방출률(cumulative release rate %)로 나타내었다.
결과 및 토의
유상의 장쇄 지방산 대표하는 옥수수유 및 팜유, 중쇄 지방산의 대표하는 MCT유, 아로마 오일의 대표하는 레몬 유를 사용하여 단일 에멀젼의 입자 크기(A)와 에멀젼 점도 (B)의 결과를 Fig. 1에 나타내었다. 단일 에멀젼 입자크기 는 펩타이드 0%에서 옥수수유, 팜유, MCT유, 레몬유 각 각 146 nm, 266 nm, 167 nm, 417 nm 나타났고, 펩타이드 가 첨가된 경우 팜유와 MCT유에서는 입자크기가 약간 증 가하는 경향을 보였으나, 특히, 제조 직후 팜유의 경우 palmitic 지방산 함량이 높아 상온에서 고체 형태로 존재하 며 단단한 구조적인 특성에 의해 약간 큰 입자를 지닌 것 으로 사료된다. 반면, 레몬유로 제조된 단일 에멀젼인 경우 어피 펨타이드 첨가로 인해 상당히 입자크기가 감소하였다. 이는 수상에 포집되지 못한 펩타이드가 자기 조립성(selfassembling peptide) 특성으로 유상 및 과잉으로 녹여진 계 면활성제와 집합하여 micelle를 형성함으로 평균 입자크기 가 감소한 것으로 사료된다. 따라서, 유상의 포화정도, 사 슬길이, 지방 함량에 따라 에멀젼 형성에 영향을 준다는 것을 입증할 수 있었다(Nidhi & Baskaran, 2011).

단일 에멀젼의 점도 결과를 살펴보면, 펩타이드 첨가여 부와 관계없이 에멀젼의 점도는 팜유, 옥수수유, MCT유, 레몬유 순으로 높은 점도 값을 나타내었다. 이러한 단일 에멀젼의 점도 변화는 본 연구에서 사용된 오일 자체가 가 지는 점도 결과와 유사하다(Data not shown). 또한, 옥수수 유, MCT유, 레몬유는 펩타이드 첨가에 따른 유의적인 점 도 변화를 보이지 않았으나, 팜유는 급격한 점도 감소를 보였다(34 Pa∙s → 1.5 Pa∙s) (p<0.05). 그러나, 팜유의 경우 펩타이드 첨가 에멀젼이 다른 유상들에 비해 높은 점도 값 을 나타내었다. 팜유는 상온 및 낮은 온도에서는 높은 solid fat 함량을 지닌 포화지방산으로 견고한 구조를 가지 고 있어 다른 유상과 달리 높은 점도 값을 갖는 것으로 판단된다(Miskandar et al., 2002).
친유성 유화제(PGPR) 첨가에 따른 4가지 유상(O)과 펩 타이드 첨가에 따른 수상(W)사이의 계면장력 측정 결과는 Fig. 2에 제시되었다. Fig. 2A는 PGPR이 첨가되지 않은 순수한 유상 조건에서 측정한 결과이며, 펩타이드 첨가는 레몬유를 제외하고 계면장력 감소에 큰 영향 준 것으로 판 단된다. 펩타이드 첨가로 인한 계면장력 감소는 본 연구에 서 사용된 저분자 펩타이드(3 kDa)가 수상-유상 계면시스템 에서 계면활성제의 흡착을 개선하는 계면활성을 지니고 있 음을 시사한다(Jo et al., 2019). 특히, 레몬유의 경우 펩타 이드를 첨가하더라도 계면장력에 영향을 미치지 않았으며, 낮은 밀도 및 점도와 함께 비교적 물에 대한 용해성이 높 기 때문에 낮은 계면장력을 유도하였음을 보여준다(Lim et al., 2011).
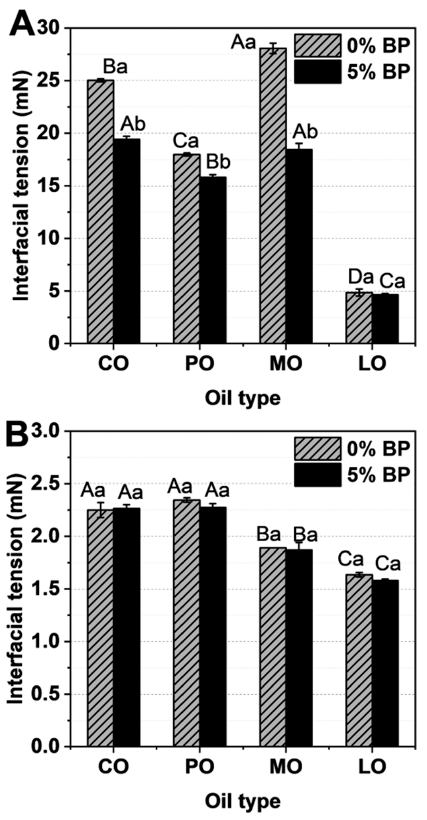
Fig. 2B는 본 연구에서 친유성 유화제로 사용한 PGPR을 각각의 유상에 포함시킨 후 펩타이드 첨가여부에 따른 수 상과의 계면장력을 측정한 결과이다. 당연하게도 순수한 유상 조건에서 측정된 계면장력(Fig. 2A)와 달리 PGPR 함 유 유상과의 계면장력 값은 2.5mN 이하로 매우 감소하였 다. 그러나, PGPR 존재 하에 펩타이드 첨가에 따른 계면 장력은 PGPR이 첨가되지 않은 계면 시스템과 달리 유의 적인 차이를 보이지 않았다(p>0.05). 친유성 유화제인 PGPR은 에멀젼 형성에 있어 높은 유화효과로 입자 형성 에너지를 낮추게 하며, 입자의 상전이 과정을 지체시키는 기능으로 해석된다. 당연하게도 PGPR에 의해 계면장력을 감소이 감소함에 따라 유화 지방구의 입자크기가 작아지기 때문에 수상-유상 계면 시스템에서 PGPR이 지배적으로 W/O 에멀젼 형성에 관여함을 증명하였다.
다양한 유상 종류에 따라 제조한 이중 에멀젼의 입자크 기(A, B)와 제타전위(C, D)는 Fig. 3에 제시하였다. Blank 이중 에멀젼(0% 펩타이드)의 입자 크기는 옥수수유, 팜유, MCT유, 레몬유의 유상 종류에 따라 제조 직후 1.37 μm, 0.98 μm, 0.89 μm, 11.2 μm로 각각 나타났고 5% 펩타이드 농도에서는 팜유를 제외한 모든 유상에서 약간씩 입자크기 가 증가하는 경향을 보였다(Fig. 3A). 또한, 옥수수유, 팜유, MCT유는 균일하고 작은 마이크로 단위의 입자 크기를 갖 는 반면 레몬유는 다소 큰 입자 형성을 보여주었다. 이는 아로마 오일 중 하나인 오렌지유과 유사한 경향성을 지닌 다. Zhang et al. (2015)에 의하면 아로마 오일은 낮은 계 면장력에 의해 액상에서 고체로 상전이가 일어나고 불안정 한 상태를 보이며, 수상(W)보다 낮은 밀도를 지니고 있어 중력에 의한 층 분리 현상이 일어난다고 알려져 있다. 게 다가, 옥수수유, 팜유, MCT유는 1개월 저장 후에도 입자 크기가 변화하지 않는 반면, 레몬유는 유의적으로 입자크 기가 감소하였으며, 이는 앞서 말한 바와 같이 낮은 계면 장력으로 인한 상전이 현상으로 에멀젼의 불안정성이 가속 화된 것으로 판단된다.
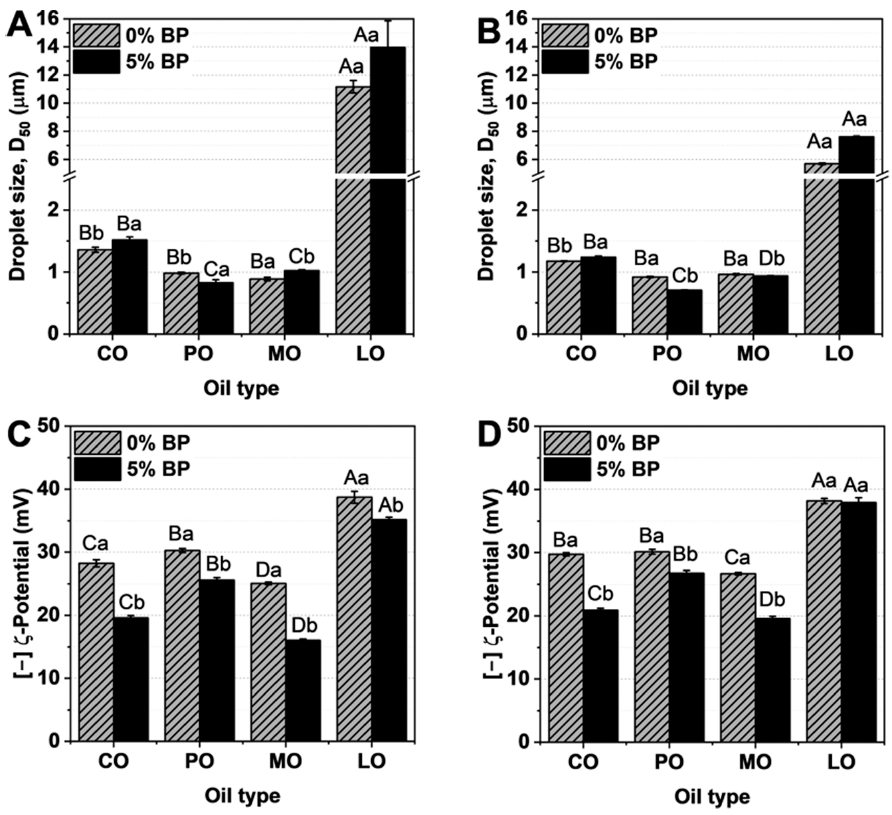
이중 에멀젼의 제타전위 결과를 살펴보면, 유상의 종류 에 관계없이 펩타이드가 첨가될 때 제타전위(절대값)이 감 소하였다. 이는 펩타이드가 전해질 역할을 하여 액적 표면 의 이온 사이 인력을 증가시키기 때문에 제타전위가 감소 하는 경향을 보여주는 것이다(Moreira de Morais et al., 2006). 일반적으로 이중 에멀젼은 Ostwald ripening을 억제 하기 위하여 내부수상에 전해질(예. NaCl)을 첨가하는데, 본 연구에서 사용된 펩타이드(저분자)또한 전해질 역할, 즉 계면활성을 가짐으로써 계면장력을 낮추고 제타전위 값을 감소시킨 것으로 판단된다. 이러한 제타전위 결과는 계면 장력 측정 결과값과 유사하게 나타났다. 이러한 경향성은 저장 1개월 이후에도 동일하게 나타났다. 유상 유형에 따 른 제타전위 비교는 오일이 가지는 유리지방산과 인지질에 의해 영향을 받는다고 알려 있다. 본 연구에서는 레몬 유 >팜유 >옥수수유 >MCT유 순서로 나타났으며, 레몬유 의 제타전위 값(>35 mV)이 다른 오일에 비해 비교적 높은 값을 나타내었다.
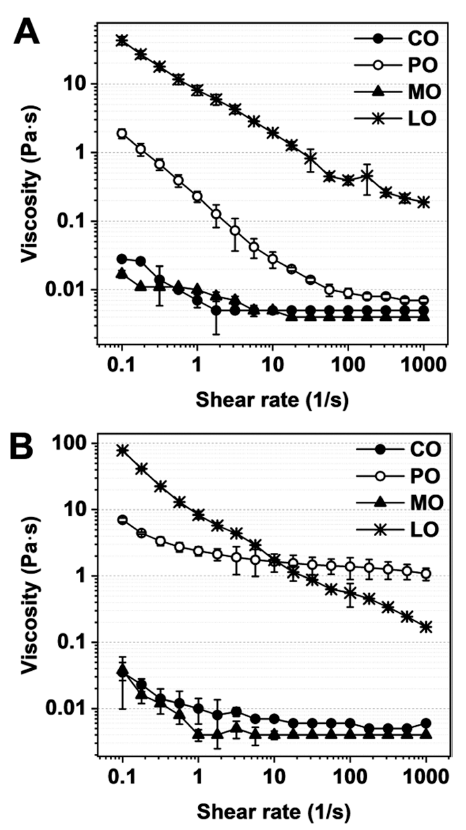
다양한 유상 종류에 따라 제조한 이중 에멀젼의 점도는 Fig. 4에 나타내었다. 모든 이중 에멀젼의 점도는 전단 속 도가 증가함에 따라 감소하는 shear thinning (전담 담화)의 유체 특성을 나타낸다. 이는 분산된 입자들이 군집을 이루 어 농축된 에멀젼의 경우, 전단 속도가 증가함에 따라 유 체역학적으로 가해지는 힘에 의하여 군집은 변형과 파괴가 일어나 점도가 저하된다고 알려져 있다(McClements, 2004). 일반적으로 이중 에멀젼의 점도는 이중 에멀젼의 연속상의 점도에 의해 결정될 수 있으며, 이들의 외부 수상은 모두 동일한 조건이기 때문에 점도의 차이는 서로 다른 유상에 직접적으로 기인할 수 있다(Bou et al., 2014). 또한 이러한 점도의 영향을 에멀젼의 안정성과 직접적으로 관련되어질 수 있다.
다양한 유상 종류에 따라 제조된 이중 에멀젼의 1개월 저장 후 외관 및 크림화 수치가 Fig. 5A에 제시되었다. 에 멀젼 각각의 유상 종류에 따른 크림화 수치로 옥수수유 10 (%), 팜유 0 (%), MCT유 46.4% 그리고 레몬유 44.5 (%) 으로 산출되었다. Dickinson & Golding (1997) 보고에 의 하면 점도가 높은 입자 일수록 층 분리 현상 및 크림화 수치가 감소한다. 낮은 크림화 수치를 나타낸 옥수수유과 팜유를 함유한 이중 에멀젼은 다른 유상보다 높은 안정성 을 보이고 있다고 사료된다. 또한 Driscoll (2001) 보고에 의하면 지방산 구성성분 중 하나인 oleic acid를 유상에 많 은 함량을 지니고 있는 에멀젼은 높은 안정성을 지닌다고 판단된다. 이와 같이 oleic acid 함량이 없는 MCT유는 높 은 크림화 수치가 나타났다고 사료된다. 레몬유는 제조 시 액상에서 고체로 변하는 상전이 현상으로 인해 외관상 입 자의 침강(sedimentation)을 보여주었다. 대부분 아로마 오 일들은 수상보다 밀도가 낮아 중력에 의한 층 분리 및 크 림화 현상으로 유사한 경향을 보여주었다.
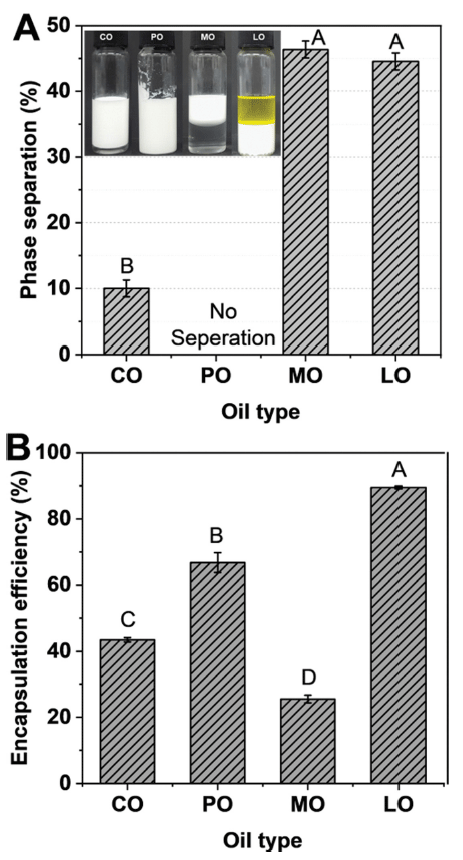
Fig. 5B는 제조 직후 이중 에멀젼에 포집된 펩타이드의 포집률을 보여주고 있다. 그 결과, 레몬유, 팜유, 옥수수유, MCT유 순서로 높은 포집효율을 나타내었다. 레몬유의 높 은 포집률은 제조 직 후 높은 점도(Fig. 4)로 인하여 펩타 이드의 포집률을 높였을 것으로 예상하며, 이러한 경향은 다른 논문과 상이한 결과를 나타내었다. Lee et al. (2023) 의 연구 결과에서는 유사 오일인 오렌지유로 제조된 이중 에멸젼이 에멀젼 제조 시 열역학적으로 불안정성을 보다 야기시켜 전해질의 포집률을 낮추었다고 설명하고 있다. 따라서, 본 연구에서는 펩타이드의 포집률 측정 결과를 보 완하기 위하여 이중 에멀젼의 물리화학적 안정성 평가를 저장 온도 및 저장 기간까지 고려한 펩타이드의 방출효과 로 확인하였다.
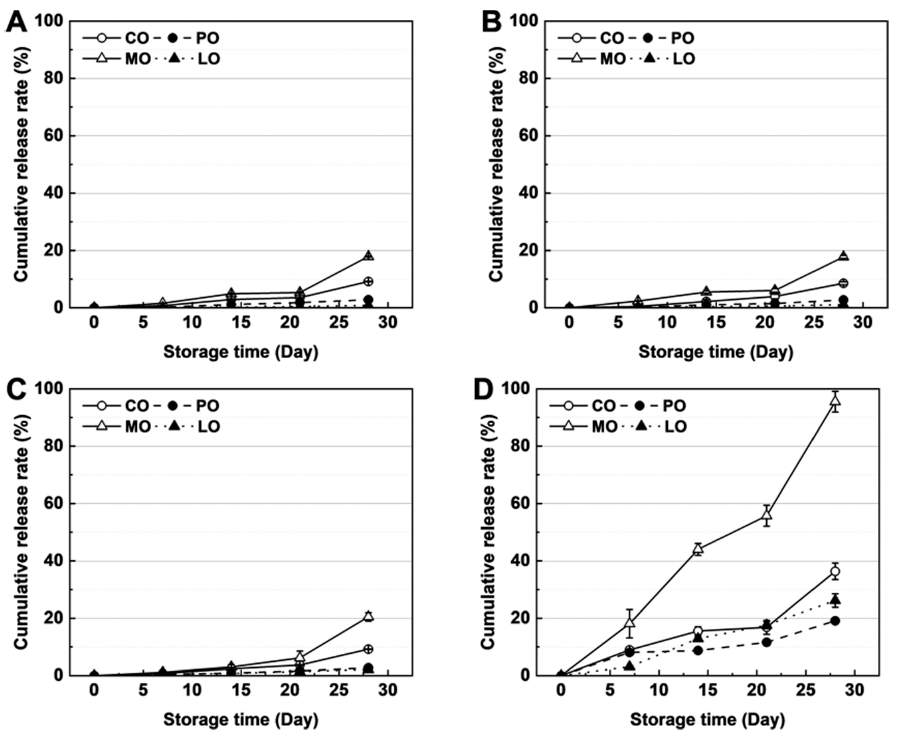
Fig. 6은 다양한 저장 온도(4, 25, 37, 60°C)에서 1개월간 저장하는 동안 방출되는 펩타이드의 함량을 누적된 펩타이 드 방출률로 제시하였다. 그 결과 4°C, 25°C, 37°C에서 온 도에 따른 펩타이드 방출효과를 보이지 않았다(p>0.05). 낮 은 펩타이드 방출률을 함유한 팜유와 레몬유는 보관 온도 에 따라 상대적으로 높은 안정성을 확인할 수 있었다. 60°C에서 유상 종류에 따라 제조된 이중 에멀젼의 펩타이 드 누적 방출률은 MCT유(95.5%), 옥수수유(36.4%), 레몬 유(26.2%), 팜유(19.1%) 순으로 높았다. 특히, 1개월 저장 후 MCT유의 내부에 포집된 펩타이드는 모두 소진하였다. Allende et al. (2008)와 Lim et al. (2011) 연구 결과에 의 하면 중쇄 지방산을 함유한 MCT유는 비교적 높은 수용해 성을 나타내어 에멀젼 시스템에서 외부 환경 온도에 취약 할 수 있기 때문에 높은 방출률을 보여주었다. 또한 지방 산의 사슬 길이가 길수록 물에 대한 용해도가 감소하여 중 쇄 지방산보다 높은 안정성을 보고되었다(Lee et al., 2023). 따라서, 본 연구에서는 긴 지방 사슬을 함유하고 있 는 옥수수유와 팜유가 MCT유에 비해 높은 온도에서도 상 대적으로 높은 포집 효율을 통해 높은 저장 안정성을 나타 내었다.
결 론
본 연구의 목적은 펩타이드가 포집된 단일 에멀젼(W/O) 과 이중 에멀젼(W/O/W)의 제형 최적화를 통해 저장 기간 에 따른 안정성 확립을 하였다. 또한 다양한 유상 종류로 옥수수유, 팜유, MCT유, 레몬유를 사용하여 서로 다른 저 장온도에서 1개월 저장동안 펩타이드의 방출효과를 확인하 였다. 이중 에멀젼 시스템에서의 입자 안정성 및 펩타이드 방출억제 효과는 팜유로 제조된 경우 가장 높았으며, 반대 로 레몬유의 경우는 가장 물리화학적 안정성이 낮게 나타 났다. 또한 모든 이중 에멀젼은 37도 이하의 저장조건에서 펩타이드가 안정적으로 포집되었으나, 60도 이상에서는 특 히 MCT유로 제조된 이중 에멀젼에 포집된 펩타이드는 대 부분 방출되어 소진된 것으로 보였다. 따라서, 추후 연구에 서는 상대적으로 고온인 60도 이상 조건에서 안정성을 보 장할 수 있는 이중 에멀젼 기반 제형 연구가 필요할 것으 로 판단된다.