Article
음이온성 나노점토를 이용한 참당귀 꽃 추출물의 나노분말화 연구
김태현, 김형준, 최애진1, 최현진1, 배영석1, 오제민*
Preparation of Nanopowder Consisting of Angelica gigas Nakai Flower Extract and Anionic Nanoclay
Tae-Hyun Kim, Hyoung-Jun Kim, Ae-Jin Choi1, Hyun-Jin Choi1, Yeoung-Seuk Bae1, Jae-Min Oh*
Department of Chemistry and Medical Chemistry, College of Science and Technology, Yonsei University
1Postharvest Research Team, National Institute of Horticultural and Herbal Science (NIHHS) of RDA
*Corresponding author: Jae-Min Oh, Department of Chemistry and Medical Chemistry, College of Science and Technology, Yonsei University, #326, Changjohall, Yonseidaegil-1, Wonju 26493, Korea Tel.: +82-33-760-2368; Fax.: +82-33-760-2182
jaemin.oh@yonsei.ac.kr
© Korean Society for Food Engineering All rights reserved. This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Received: Sep 10, 2015; Revised: Oct 1, 2015; Accepted: Oct 13, 2015
Abstract
We have hybridized Angelic gigas Nakai flower extract (AGNF) and two-dimensional layered double hydroxide (LDH) nanomaterials through reversible dehydration-hydration in order to obtain the nanopowder of natural extract. The Angelica gigas Nakai flower was treated with methanol to extract carbohydrate, polyphenol, and flavonoid components. LDH with an uniform size of 250 nm was prepared by hydrothermal method and calcined at 400°C to obtain layered double oxide (LDO) precursor. For hybridization, AGNF in 40% methanol was reacted with LDO powder at various AGNF/LDO weight ratios: 0.15, 0.30, 0.85, and 1.70. The hybrids were obtained in fine powder which had enhanced hydrophilicity and water dispersity compared with dried AGNF. The X-ray diffraction and scanning electron microscopic results revealed that the house-of-cards structure of nanomaterials could encapsulate AGNF moiety inside their cavity. Quantitative analyses using UV-Vis spectra exhibited that the content of AGNF in hybrid increased upon AGNF/LDO ratio in reactant increased. According to 1,1-diphenyl-2-picrylhydrazyl radical scavenging assay, AGNF/LDO showed higher antioxidant activity compared with an equivalent amount of AGNF itself.
Keywords: layered double hydroxide; Angelica gigas Nakai; flower extract; reconstruction; nanopowder
서 론
최근 나노기술의 급속한 성장과 함께 여러 분야에 나노 기술이 접목되어 높은 효율의 성능을 갖는 물질들이 개발 되고 있다(Taylor et al., 2008; Zhang et al., 2010; Gunjakar et al., 2011; Deng et al., 2014). 생명과학이나 식품 분야에서도 나노기술 적용된 연구개발이 활발히 진행되고 있는데, 나노기술 접목에 따라 유용한 성분들을 안정화하 고 취급을 용이한 형태로 제조하며, 체내 흡수율을 높이거 나 표적 기관으로의 전달 효율을 높이는 연구가 활발히 진 행되고 있다(Shi et al., 2011; Lee et al., 2015; Tae et al., 2015; Tang el al., 2015). 유용 성분의 경우 약물 활성을 갖는 저분자에서부터 항산화물질, 생체 고분자에 이르기까 지 다양한 물질들이 관심을 끌고 있는데, 최근 친환경, 웰 빙의 기조에 따라 천연 추출물을 유용성분으로 활용하고자 하는 시도가 다방면에서 이루어지고 있으며, 나노기술 역 시 천연 추출물의 활용도를 높일 수 있는 하나의 방안으로 제시되고 있다(Das et al., 2012; Zhai et al., 2012; Foglio et al., 2015).
천연 추출물의 경우 추출기법에 따라 달라질 수 있으나, 일반적으로 다량의 탄수화물 화합물이나 생체고분자를 포 함하며, 항산화 혹은 미백 기능성 물질들은 일부 포함되어 있다. 추출물을 구성하는 대다수의 탄수화물과 생체고분자 때문에 고형분으로 제조하는 경우 점성이 높은 형태로 존 재하여 보관이나 취급의 어려움이 있다. 최근 발표된 논문 에 의하면, 한약재와 같은 천연 성분에 리포좀, 마이크로에 멀젼, 콜로이드 나노젤, 나노마이셀 등의 나노물질 기술이 적용되면 적용하게 되면, 유용성분의 활성이 높아지고, 안 정성이 확보되며, 높은 수분산 안정성을 확보하는 등의 효 과가 있는 것으로 보고되고 있다(Ansari et al., 2012). 본 연구에서는 천연 추출물 중 항산화 효과 및 다양한 질환에 대한 치료 효과가 있는 것으로 보고되어 있는 참당귀 추출 물에 나노기술을 적용하여 보관과 취급이 용이한 나노분말 을 제조하고자 하였다. 우리의 기존 연구에 따르면 참당귀 의 뿌리 추출물을 금속이중층수산화물(layered double hydroxide, LDH) 나노물질로 캡슐화하게 되면 추출물 분 자를 나노공간 내에 재배열함으로서 안정하게 물성의 변화 를 유도할 수 있다(Kim et al., 2015). 본 연구에서는 약용 으로 사용되고 있는 참당귀의 부위 중 꽃 부위의 추출물을 활용하였다. 참당귀 꽃은 그 동안 가식부위에서 제외되어 왔으나, 기존 연구 결과에 따르면 용매 추출을 통해 얻은 참당귀 꽃 추출물이 항산화 활성이나 암세포 억제 등의 기 능성을 가진 것으로 알려져 있다(Park et al., 2011). 천연 유효성분 추출에 널리 사용되는 메탄올 추출법(Park et al., 2004, Sohn et al., 2005; An et al., 2014)을 활용하여 참 당귀 꽃 추출물을 확보하였으며, 나노물질로는 약물전달체 분야에서 많은 연구가 진행되고 있는 금속이중층수산화물 나노물질(Oh et al., 2009; Choi et al., 2010; Kim et al., 2014)을 사용하여 나노분말을 얻고, 수분산 안정성을 높이 는 한편, 항산화와 같은 기능성을 증진시킬 수 있음을 확 인하고자 하였다.
금속이중층수산화물은 Mg1-xAlx(OH)2x+의 화학식을 갖는 양이온성 나노층이 층간 음이온에 의하여 적층구조를 갖는 물질로서, 구조와 특성이 점토와 비슷하여 음이온성 점토 로도 알려져 있다(Cavani et al., 1991). 금속이중층수산화 물은 높은 생체친화성을 갖고 있는 것으로 알려져 있으며 (Choy et al., 2004; Duan & Evans, 2006; Oh et al., 2006; Choy et al., 2007; Xu et al., 2008; Oh et al., 2012), 특히 하이드로탈사이트로 명명되는 금속이중층수산 화물은 Mg, Al, 탄산이온을 주성분으로 하며, Bayer사에 의하여 Talcid®라는 제산제 제품으로 생산·판매되고 있기 도 하다. 금속이중층수산화물의 나노층이 갖는 양전하는 추출물 내의 탄수화물, 폴리페놀, 플라보노이드 등이 갖고 있는 C=O, C-O-C 및 C-OH 기능기들의 약한 음전하와 상호작용하여 유용 성분들을 나노층 표면에 부착하여 하이 브리드 물질로 제조할 수 있다. 또한, 나노층의 무질서한 배열을 통해 얻어지는 나노공간 내부에 추출물 성분들을 배열함으로서, 추출물의 소수성을 무기물질의 친수성으로 개질할 수 있으며, 입자가 고운 분말 형태로 얻을 수 있다.
금속이중층수산화물 나노물질에 유기물을 도입하는 반응 법은 다양한 방법이 보고되고 있는데, 금속이중층수산화물 을 형성하면서 물질을 담지하는 공침법, 기합성된 금속이 중층수산화물에 이온교환을 통해 도입하는 이온교환법, 그 리고 금속이중층수산화물을 열처리하여 산화물을 얻은 후 수화반응과 동시에 유기물을 도입하는 재건법이 대표적인 반응법이다(Rives et al., 2001). 이전 연구 결과에서 보고 된 바에 따르면 재건법을 사용할 경우 이온교환법에 비하 여 금속이중층수산화물 나노물질 내 유기물을 약 5배 가량 높은 함량으로 담지할 수 있으므로(Goswamee et al., 1998; Kang et al., 2013; Kang et al., 2015), 본 연구에서 는 천연 추출물을 하이브리드화하는 방법으로 재건법을 사 용하였다. 특히, 재건 과정 중에 나노입자들이 무질서하게 배향되면서 카드탑 형태의 구조를 이룰 수 있으며(Pan et al., 2010), 이로 인해 생성되는 나노공간에 참당귀 꽃 추출 물 분자를 담지하고자 하였다. 나노물질과 추출물의 다양 한 비율에 따라 하이브리드화 반응을 수행하여 나노분말을 제조하였으며, 반응비에 따른 추출물의 함량과 반응의 효 율을 평가하였다. 아울러, 나노분말화 된 하이브리드의 구 조와 성상을 분석하는 한편, 얻어진 나노분말의 친수성이 추출물에 비하여 증가함을 확인하였다.
재료 및 방법
재료 및 시약
질산마그네슘수화물(Mg(NO3)2·6H2O), 질산알루미늄수화 물(Al(NO3)3·9H2O), 탄산수소나트륨(NaHCO3)과 DPPH (1,1- diphenyl-2-picrylhydrazyl, C18H12N5O6)는 Sigma-Aldrich Co. LLC. (St. Louis, MO, USA)에서 수산화나트륨(NaOH)은 대정화금(주)(Daejung Chemicals & Metals Co. Ltd., Siheung, Korea)에서 구입하여 추가적인 정제 없이 사용하 였다. 참당귀 꽃 추출물은 메탄올 추출법을 이용해 추출하 였으며 건조된 참당귀(Angelica gigas Nakai) 꽃 50 g을 1,000 mL 메탄올에 넣은 후 2시간 동안 교반한 후에 거름 종이(Advantec MFS Inc., Dublin, CA, USA)를 이용해 걸 러주었다. 얻어진 참당귀 꽃 메탄올 추출물(AGNF)에 탈이 산화탄소 증류수를 첨가하여 메탄올:증류수(40:60, v/v) 용 액으로 제조하여 하이브리드화 반응에 사용하였다.
금속이중층수산화물의 합성과 참당귀 꽃 추출물과의 하이 브리드화
균일한 크기 및 성상을 가지는 금속이중층수산화물(LDH) 은 이전 연구를 참고하여(Oh et al., 2002) 다음과 같이 제 조하였다. 마그네슘(Mg2+)과 알루미늄(Al3+)이온을 각각 0.1875M, 0.0973M 농도로 포함하는 금속이온 수용액을 0.75M 농도의 염기용액(NaOH, NaHCO3)으로 pH가 9.5정 도가 될 때까지 적정하였다. 그 후 고온고압반응용기로 옮 겨 150°C 조건에서 48시간 동안 반응하였다. 이후 얻어진 혼탁액은 원심분리를 통해 분리하였고 탈이산화탄소 증류 수로 3회 이상 세척 후 동결건조하였다. 참당귀 꽃 추출물 과의 하이브리드화를 위하여 분말형태의 금속이중층수산화 물을 400°C에서 8시간동안 하소하여 금속산화물(LDO)을 확보하였다. 확보된 금속산화물분말은 참당귀 꽃 추출물 용액에 다양한 질량 비율(참당귀 꽃 추출물/금속산화물; 0.15, 0.30, 0.85, 그리고 1.70)로 혼합하였고, 질소조건하에 서 24시간동안 반응하였다. 최종적으로 얻어진 4가지 종류 의 하이브리드는 원심분리를 통해 분리하고 동결건조하였 다. 나노분말화 된 참당귀 꽃 추출물 하이브리드는 다음과 같이 LDH-AGNF-n (n = 1, 2, 3, 4)로 명명하며 정수(n) 1, 2, 3, 4는 반응에 사용한 참당귀 꽃 추출물/금속산화물 비율이 0.15, 0.30, 0.85, 1.70임을 나타낸다.
하이브리드 특성화
나노분말화 된 참당귀 꽃 추출물 하이브리드의 결정구조 분석을 위해 X-선 회절분석기(X-ray diffractometer, D2 Phaser with LYNXEYETM detector, Bruker AXS GmbH, Karlsruhe, Germany)를 활용하였다. X-선 회절패턴은 5°에 서 70° (2θ) 범위에서 0.5초당 0.02°의 증가비율로 측정하 였다. 전구체인 금속이중층수산화물과 참당귀 꽃 추출물 및 나노분말화 된 참당귀 꽃 추출물 하이브리드의 크기 및 성상을 평가하기 위해 주사전자현미경(Scanning electron microscope, Quanta 250 FEG, FEI, Hillsboro, OR, USA) 을 사용하였다. 각 분말형태의 샘플을 카본테이프에 접착 후 표면을 백금/팔라듐(Pt/Pd)을 활용해 50초간 코팅하였으 며 30 kV의 전자빔을 이용해 측정하였다.
하이브리드 내 추출물 함량 분석 및 반응 효율 평가
나노분말화 후 하이브리드 분말 내 참당귀 꽃 추출물의 함량을 평가하기 위해 자외선-가시광선 분광분석기(UV-Vis spectrometer, UV-1800, Shimazu, Kyoto, Japan)를 이용하 였다. 참당귀 꽃 추출물 용액(2.85-114 ppm)에 대하여 280 nm 및 324 nm 파장에서의 흡광도를 측정하였으며, 두 파 장대에서 모두 결정 계수 r2 값이 1.000의 보정곡선을 얻 었다. 참당귀 꽃 추출물이 약 80 wt%의 탄수화물과 약 5 wt%의 폴리페놀/플라보노이드를 갖고 있음을 감안하여 하 이브리드 내 탄수화물과 폴리페놀/플라보노이드 농도를 계 산하였다. 하이브리드의 금속이중층수산화물 성분을 녹여 내기 위하여 하이브리드를 pH 2.0 인산 완충용액에 처리하 였으며, 얻어진 용액 내 탄수화물과 폴리페놀/플라보노이드 양을 정량하고, 이 성분들의 합을 추출물의 함량으로 계산 하였다. 반응 효율은 반응에 사용된 추출물 중 하이브리드 화된 추출물 양의 비율을 의미하는 것으로 함량 정량 결과 를 바탕으로 계산되었으며 3회 반복 실험을 통해 평균값 및 표준편차를 구하였다.
항산화 활성 효과 평가
참당귀 꽃 추출물과 하이브리드의 항산화 활성은 항산화 성분이 DPPH (1,1-diphenyl-2-picrylhydrazyl) 라디칼에 전 자를 공여하여 자유기를 소거하는 활성을 측정해 평가하였 다(Lee et al., 2002). 100 μM의 DPPH 용액(80% 메탄올) 2.9 mL를 다양한 농도의 꽃 추출물(640-3,200 ppm) 0.1 mL 와 혼합 후 30분간 암소 보관하였다. 하이브리드 샘플의 경우 동량의 꽃 추출물을 포함하도록 하이브리드 서스펜션 을 제조하고, 서스펜션 0.1 mL와 2.9 mL의 DPPH 용액과 혼합 후 암소에서 30분간 보관한다. 자외선-가시광선 분광 분석기(UV-Vis spectrometer, UV-1800, Shiamzu, Kyoto, Japan)를 이용해 517 nm에서 흡광도를 구하고 아래의 수식 을 통해 항산화 활성을 평가하였으며 3회 반복 실험을 통 해 평균값 및 표준편차를 구하였다.
DPPH 항산화 활성 =
∬
Control 흡광도 -(시료의 흡광도 -DPPH 미첨가 시료)
Control 흡광도
×
100
결과 및 고찰
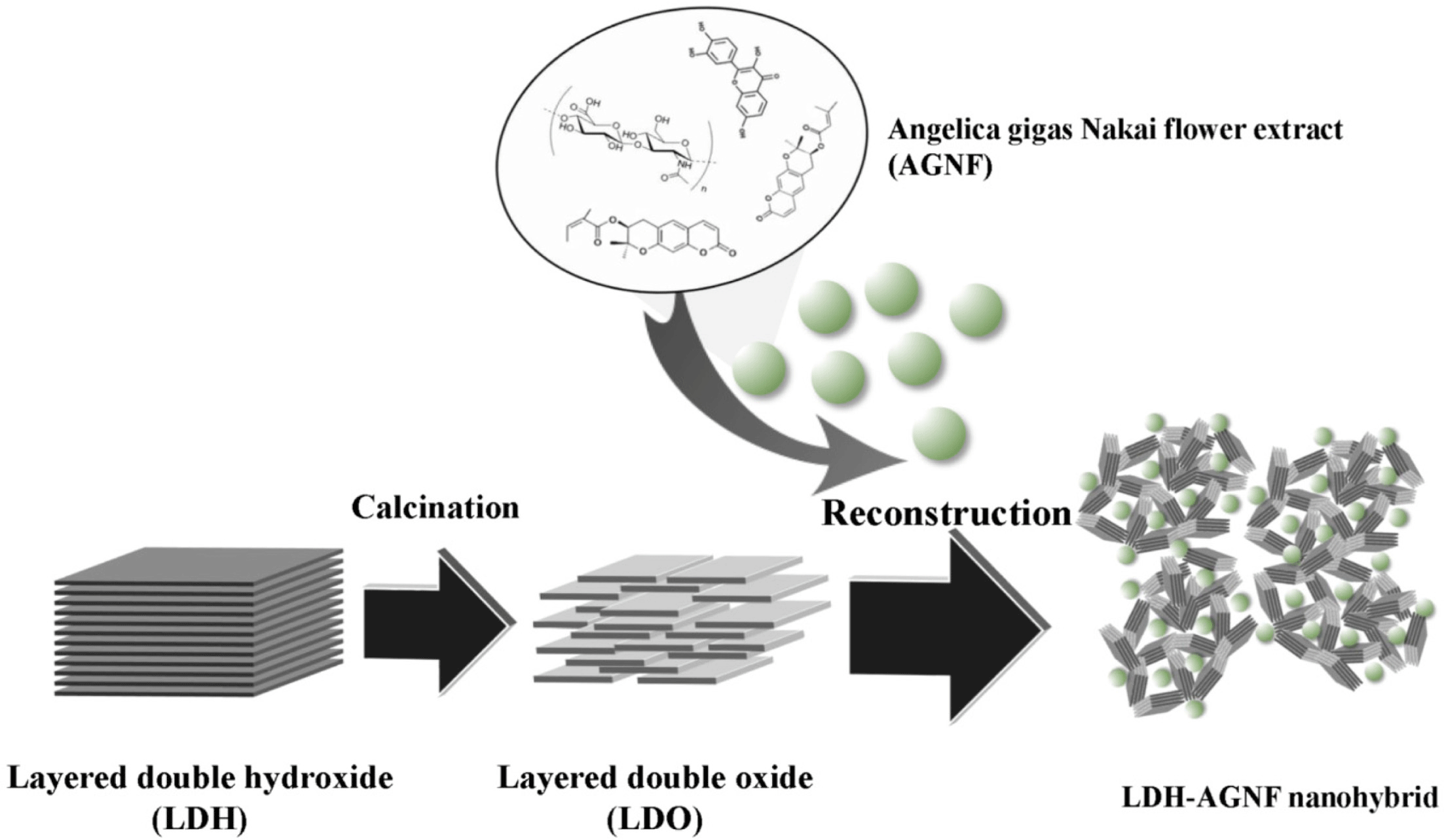
Fig. 1은 금속이중층수산화물을 이용해 나노분말화 된 참 당귀 꽃 추출물 하이브리드를 만드는 재건법의 모식도이 다. 균일한 크기 및 성상을 가지는 금속이중층수산화물을 전기로(furnace)에서 400°C의 온도로 8시간 하소하여 금속 산화물을 얻는다. 하소과정(calcination)을 통해 얻어진 금속 산화물은 금속이중층수산화물의 층간이온과 수분이 제거된 형태로 존재한다. 금속산화물을 음이온성 분자와 물분자가 존재하는 용액과 반응시키면, 음이온성 분자를 층간에 담 지한 형태로 원래의 금속이중층수산화물 구조를 회복하게 되는데, 이를 금속이중층수산화물의 메모리 효과라 하고, 이러한 과정을 통해 하이브리드를 얻는 과정을 재건법 (reconstruction)이라고 한다(Pérez-Ramírez et al., 2007). 문 헌에 의하면 재건법 과정 중 금속이중층수산화물 나노입자 의 모서리와 면 사이의 강한 상호작용에 의해 층들이 불규 칙적으로 쌓일 수 있으며, 이러한 불규칙적인 쌓임에 의해 크기가 큰 분자도 담지할 수 있는 내부공간의 형성될 수 있다(Pérez-Ramírez et al., 2007). 재건법을 통해 얻어진 나노분말은 추출물 내 존재하는 다양한 분자들을 금속이중 층수산화물 입자 사이의 나노공간에 배열함으로서 유기물 특유의 점도를 저해하여 분말 형태로 존재할 수 있게 하며, 하이브리드 표면에 존재하는 친수성 금속이중층수산화물 때문에 전반적으로 물분자와의 상호작용을 높일 수 있다.
Fig. 2는 참당귀 꽃 추출물 및 하이브리드의 건조상을 증류수에 분산한 사진이다. 나노분말화 추출물 하이브리드 및 건조상 추출물을 5 mg/mL의 농도로 수분산하였을 경우 하이브리드가 추출물에 비하여 높은 친수성을 가짐을 보인 다. 추출물은 물에서 일부 용해되지만 대부분 녹지 않는 고형분(Fig. 2e의 하단 원)으로 존재하는 반면, 하이브리 드는 잘 분산되어 서스펜션으로 존재한다. 하이브리드 서 스펜션이 안정한 상태로 침전을 보이지 않는 반면, 추출물 고형분은 침전을 보이는 것으로 미루어 보아, 참당귀 꽃 추출물은 하이브리드 반응에 의하여 친수성이 높은 미세분 말로 제조될 수 있음을 알 수 있다. Costantino 그룹은 발 색단을 갖는 염료 분자가 금속이중층수산화물 층간의 나노 공간에 배열될 경우 3차원적 배열이 2차원 배열로 변화하 면서 흡광 파장 및 형광 특성과 같은 물리화학적 성질이 변화됨을 보고한 바 있는데(Aloisi et al., 2002), 본 연구에 서의 하이브리드화도 이와 같이 추출물 분자의 배열을 변 화시켜 수분산 특성과 같은 물성에 변화가 생긴 것으로 판 단된다. 하이브리드 서스펜션은 제조 시 사용한 추출물의 양이 증가할수록 더 진한 색을 보여주는데 이는 하이브리 드 내 존재하는 참당귀 꽃 추출물의 양이 증가하기 때문인 것으로 예상된다. 이를 통해 참당귀 꽃 추출물이 금속이중 층수산화물과의 하이브리드를 통해 취급이 용이한 분말로 존재하며, 수분산성이 높아져 다양한 산업적 응용이 가능 할 것으로 예상된다.
Fig. 2.
Photographs of suspension: (a) LDH-AGNF-1, (b) LDH-AGNF-2, (c) LDH-AGNF-3, (d) LDH-AGNF-4, (e) AGNF itself in 5 mg/mL concentration.
White circle in (e) indicate undissolved lump of AGNF. (f) 40% MeOH AGNF solution.
Download Original Figure
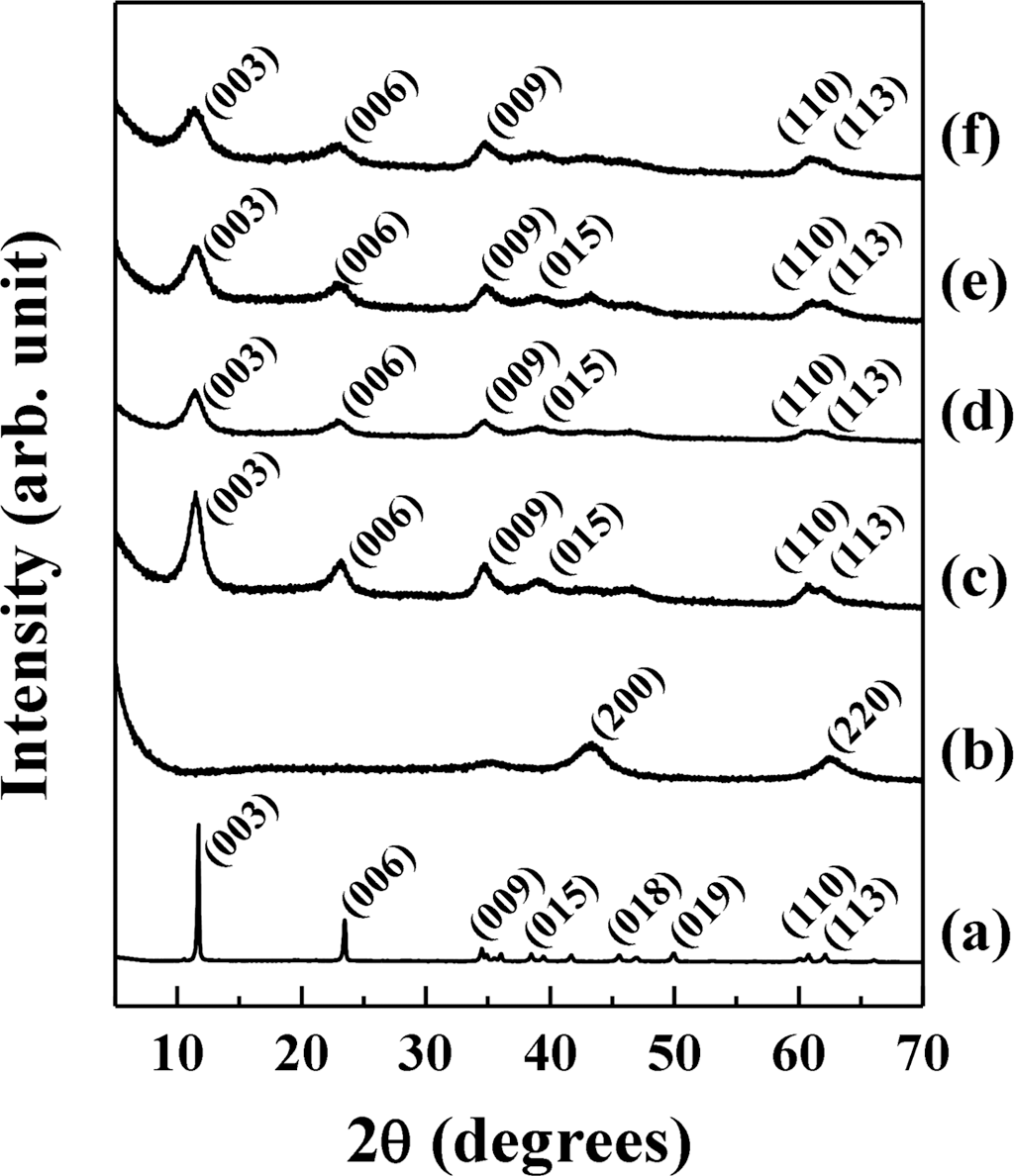
제조된 하이브리드의 결정구조를 확인하기 위하여 금속 이중층수산화물 전구체(LDH), 금속산화물(LDO) 및 나노분 말화 된 추출물 하이브리드에 대한 X-선 회절분석을 실시 하였다. 본 연구에서 사용한 전구체인 금속이중층수산화물 (Fig.3(a)의 X-선 회절패턴은 전형적인 하이드로탈사이트 (JCPDS No. 14-0191)의 피크를 나타내고 있으며 높은 결 정성을 가지는 것으로 보인다. 또한 결정학적 c축 방향의 피크인 (003)과 (006)가 11.6°와 23.4°에서 관찰되는 것으로 보아 0.3 nm의 층간 거리를 가지고 있는데, 이는 탄산이온 이 층간에 존재함을 보여준다. 금속이중층수산화물을 400°C에서 하소하면 물분자와 이산화탄소가 기화되어 금속 산화물이 얻어지는 것으로 알려져 있는데(Rey et al., 1992), 전구체 내의 금속이온이 마그네슘과 알루미늄이기 때문에 금속산화물은 산화마그네슘과 산화알루미늄의 혼합 형태를 띠게 된다. 금속산하물의 X-선 회절패턴(Fig. 3(b))은 전형적인 산화마그네슘(MgO, JCPDS No. 45-0946) 의 결정구조를 가지는 것으로 확인되었으며, 산화알루미늄 의 경우 무정형이기 때문에 패턴에서 드러나지 않았다. 나 노분말화 된 참당귀 꽃 추출물 하이브리드의 X-선 회절패 턴(Fig. 3(c)-(f))을 보면 금속산화물(Fig. 3(b))과 다른 패턴 을 보이며, 전구체 금속이중층수산화물의 특징적인 (003), (006), (009), (015), (110), (113) 피크들과 동일한 위치에서 피크를 나타냈다. 이는 참당귀 꽃 추출물과의 하이브리드 화를 통해 본래의 금속이중층수산화물 구조가 회복됨을 의 미한다. 그러나, 전구체 금속이중층수산화물에 비하여 하이 브리드의 전반적인 피크의 크기가 줄어들고, 반치폭이 증 가하는 경향이 보이는데, 이는 하이브리드 전후 금속이중 층수산화물의 결정성 변화에 기인하는 것으로 보인다.
Fig. 3.
Powder X-ray diffraction patterns of (a) pristine LDH, (b) LDO, (c) LDH-AGNF-1, (d) LDH-AGNF-2, (e) LDH-AGNF- 3 and (f) LDH-AGNF-4.
Download Original Figure
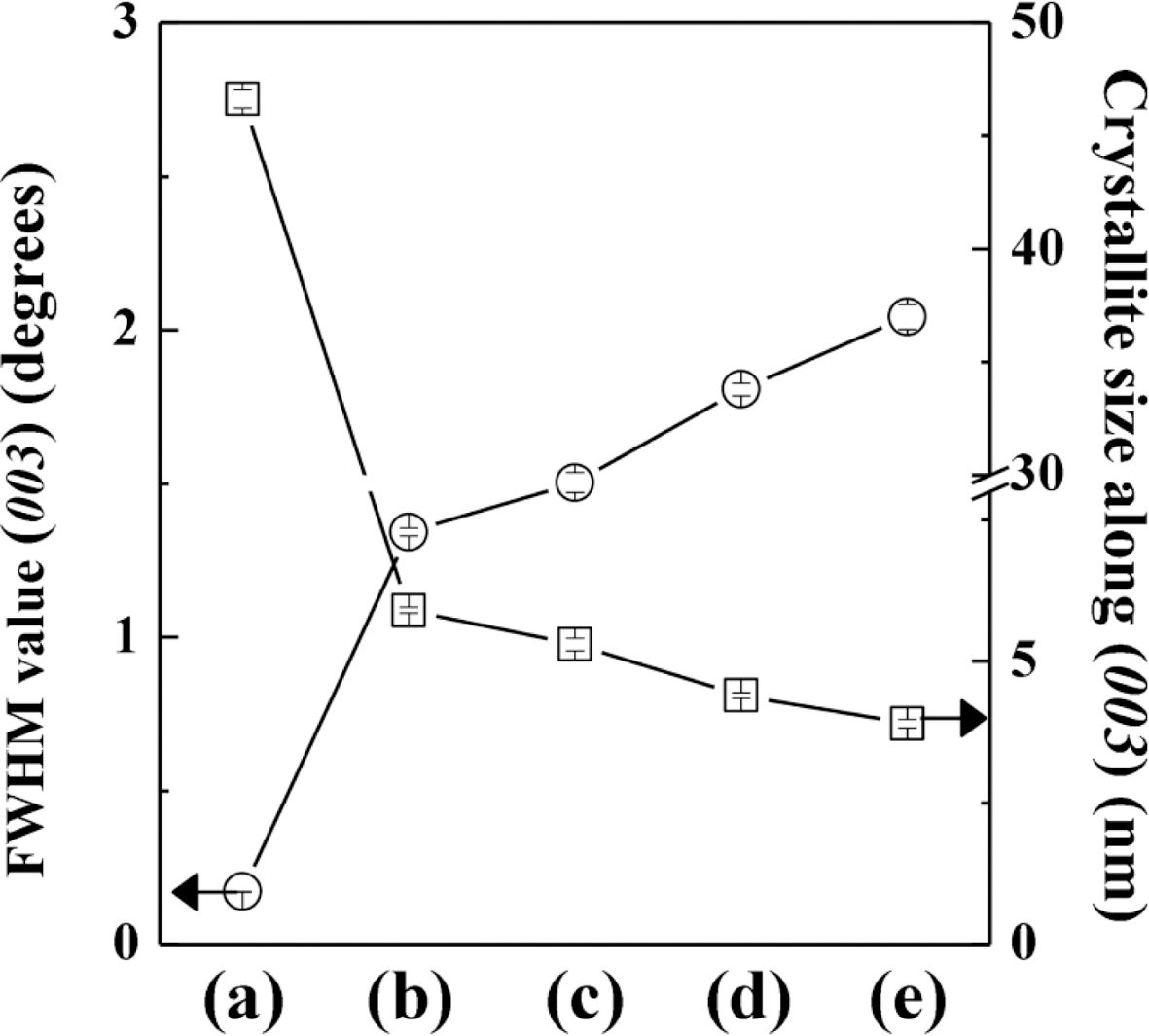
결정성 변화를 정량적으로 평가하기 위하여 Fig. 3의 대표 적 피크인 (003)에 대한 반치폭(full width half maximum, FWHM)과 이를 토대로 결정자 크기(crystallite size)를 계 산하였다(Fig. 4 ○) 전구체인 금속이중층수산화물은 0.17° 로 매우 좁은 피크의 너비를 보이는 반면, 하이브리드들은 추출물의 반응비에 따라 1.35°, 1.54°, 1.78° 및 2.00°으로 전구체 대비 매우 큰 값으로 반치폭이 증가함을 확인할 수 있다. X-선 회절에서 반치폭의 증가는 해당 결정면 방향의 배열이 무질서해지거나 결정자의 크기가 작아지는 것을 반 영하는데, Fig. 1의 모식도에서 나타낸 바와 같이 추출물과 의 하이브리드화 반응을 통해 금속이중층수산화물의 적층 개수가 줄어들고, 무질서한 방향으로 쌓여 있음을 알 수 있다. 결정학적 c축 방향의 결정자 크기를 좀 더 정량적으 로 분석하기 위하여 쉐러 식(Scherrer’s equation, eq 1)을 적용하였으며(Cullity, 2011), 3회 반복 실험을 통하여 평균 값을 취하였다.
Fig. 4.
Full width half maximum value (circles) and crystallite size (squares) along (003) with (a) pristine LDH, (b) LDHAGNF- 1, (c) LDH-AGNF-2, (d) LDH-AGNF-3 and (e) LDHAGNF- 4.
Download Original Figure
(t: 결정자 크기; λ: X-선 파장 1.5405 Å; β: 반치폭; θ: 브 래그 각)
Fig. 4의 결정자크기(Fig. 4 □) 변화를 살펴보면, 전구체 인 금속이중층수산화물의 결정자크기는 약 47 nm인 반면, 추출물 하이브리드는 매우 작은 결정자를 보이며, 반응 시 사용한 추출물의 양이 증가할수록 5.9, 5.2, 4.5 그리고 4.0 nm의 크기로 점점 작아지는 양상을 보였다. 이러한 양 상은 Fig. 1에서 나타낸 모식도처럼 금속이중층수산화물이 하소과정과 재건과정을 거치면서 일어나는 성상의 변화와 잘 부합한다.
이러한 구조 및 성상 변화를 가시화하기 위하여 전구체 인 금속이중층수산화물, 건조상 추출물 및 추출물 하이브 리드에 대한 주사전자현미경(scanning electron microscope) 연구를 수행하였다. 우선, 건조상 추출물은 매우 큰 크기의 입자(수 μm)를 보이며 불균일한 성상과 매끈한 표면을 보 이는 것으로 확인되었다(Fig. 5(a)). 대체적으로 무정형인 유기물 덩어리는 결정성장 면이 없으며, 분자간 강한 인력 으로 응집되기 때문에 이와 같은 영상이 다수 보고되어 있 으며(Hongal et al., 2014), 본 연구에서도 추출물 내 존재 하는 다양한 유기물 분자들이 서로 응집되어 이와 같은 영 상을 보이는 것으로 판단된다. 전구체인 금속이중층수산화 물의 경우 약 250 nm의 입자직경과 80 nm의 두께를 가지 며, 매우 균일한 입자 크기 분포를 보여주고 있다(Fig. 5(a)). 이는 Fig. 3의 X-선 회절패턴에서 나타난 높은 결정 성과 부합되는 결과이다. 추출물 하이브리드는 전구체 금 속이중층수산화물과는 달리 수백 nm 가량의 입자의 성상 을 보여주고 있는데, 이는 재건 반응 과정에서 전구체의 규칙적 적층구조가 변화하여 무질서한 배열을 이루고 있는 모식도(Fig. 1)과 유사한 결과이다 (Fig. 5(c)-(f)). 흥미로운 점은 반응에 사용된 추출물의 양이 증가할수록 하이브리드 가 점차 카드탑(house-of-cards) 성상과 유사하게 변화하는 것을 보여주고 있다. 이는 금속이중층수산화물의 얇은 나 노층이 추출물 분자를 담지하며 무질서하게 배열되기 때문 인 것으로 보인다. 반응에 사용한 추출물의 비율이 낮은 경우(LDH-AGNF-1과 2) 몇 개의 금속이중층수산화물 나노 입자의 응집체 표면을 추출물 분자가 뒤덮어 뭉쳐 있을 것 으로 생각되는 반면, 반응 시 추출물 비율이 높은 경우 (LDH-AGNF-3과 4) 더 많은 추출물이 나노입자 응집체 내 에 담지되어 층의 배열이 더욱 무질서하게 될 수 있다. 이 러한 불규칙적인 금속수산화물층의 배열은 유기물의 존재 하에서 금속이중층수산화물을 재건법을 이용해 하이브리드 화 될 때 금속수산화물 나노입자의 모서리-면 사이의 상호 작용이 강해지기 때문에 일어난다고 알려져 있으며(Pan et al., 2010) 이러한 성상의 변화는 X-선 회절분석을 통해 얻 어진 결정자 크기 및 반치폭의 변화 양상과 부합한다.
Fig. 5.
Scanning electron microscopic images of (a) AGNF, (b) pristine LDH, (c) LDH-AGNF-1, (d) LDH-AGNF-2, (e) LDH-AGNF- 3, and (f) LDH-AGNF-4.
Download Original Figure
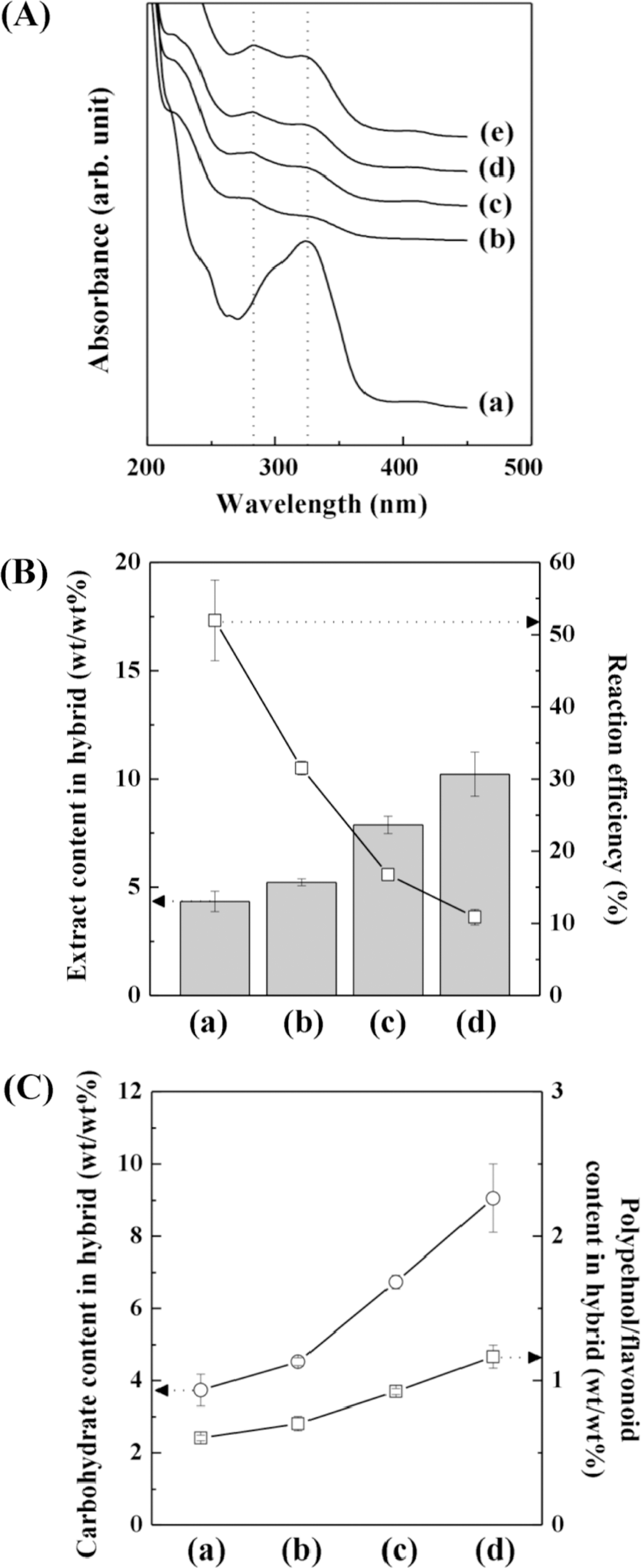
전자현미경 분석 결과 반응 시 사용한 추출물 비율이 높 을수록 좀 더 많은 추출물이 담지될 것으로 예상되는데, 이를 확인하기 위하여 하이브리드 내 추출물의 담지량 및 반응에 참여하는 추출물의 반응 효율을 자외선-가시광선 분광분석을 통해 평가하였다. 참당귀 꽃의 메탄올 추출물 의 자외선-가시광 흡광 곡선은 약 280 nm의 작은 흡광 봉우 리와 320 nm의 강한 흡광 봉우리를 보이는데(Fig. 6A(a)), 이는 각각 추출물 내에 존재하는 탄수화물(carbohydrate, 약 80 wt%)과 폴리페놀/플라보노이드(polyphenol/flavonoid, 약 5 wt%)에 해당하는 것으로 보인다(Markham & Mabry, 1975; Kirby & Wheeler, 1980; Albalasmeh et al., 2013). 추출물의 농도 및 성분의 함량을 이용하여 탄수화물은 2.30-92.34 ppm 사이 농도에서 보정 곡선을 얻었고, 폴리페 놀/플라보노이드는 0.17-6.61 ppm 사이에서 분석 가능한 보 정 곡선을 얻었다. 하이브리드에서 금속이중층수산화물을 제거하고 추출물만을 취해서 분석한 경우, 각각 탄수화물 과 폴리페놀/플라보노이드에 해당하는 320 nm, 280 nm의 흡광 봉우리를 보였다. 추출물 자체와 비교할 때 280 nm 부근의 흡광 봉우리가 상대적으로 증가한 것은 금속이중층 수산화물과의 하이브리드화함에 따라 폴리페놀/플라보노이 드가 탄수화물에 비해 더 효율적으로 담지되었기 때문이며, 이는 이전의 참당귀 뿌리 추출물 하이브리드 연구 결과와 일치한다(Kim et al., 2015). Fig. 6(B)의 막대그래프에서 보는 바와 같이 하이브리드 합성 시 추출물/금속산화물 비 율이 증가함에 따라 하이브리드 내 추출물의 함량이 3.8, 5.1, 7.9, 그리고 11.4 wt%의 증가 양상을 보이고 있으며, 주 사전자현미경의 결과에서 예측된 바와 부합한다. 재건반응 시 추출물의 반응 참여 비율(반응 효율, reaction efficacy) 은 향후 하이브리드화를 통한 분말화 응용에서 중요한 지 표이기 때문에, 함량 정량결과를 바탕으로 반응 효율을 계 산하였다. 반응 효율은 추출물 반응비가 낮은 경우 45.5% 부터 반응비가 높아질수록 12.1%까지 점차 감소하는 양상 을 보인다. 반응 시 높은 비율의 추출물을 사용하면 높은 하이브리드 내 함량을 얻을 수 있지만, 반응에 참여하지 않는 추출물의 양이 많아지므로, 적정한 비율을 선정할 필 요가 있다.
Fig. 6.
(A) UV-Vis spectra of (a) 40% MeOH AGNF and AGNF extracted from (b) LDH-AGNF-1, (c) LDH-AGNF-2, (d) LDH-AGNF-3, and (e) LDH-AGNF-4 hybrids. Dotted lines indicate 283 and 324 nm. (B) AGNF content (gray bars) and reaction efficiency (squares) of (a) LDH-AGNF-1, (b) LDH-AGNF-2, (c) LDH-AGNF-3, and (d) LDH-AGNF-4. (C) Carbohydrate content (circles) and polyphenol/flavonoid content (square) in (a) LDH-AGNF-1, (b) LDH-AGNF-2, (c) LDH-AGNF-3, and (d) LDH-AGNF-4.
Download Original Figure
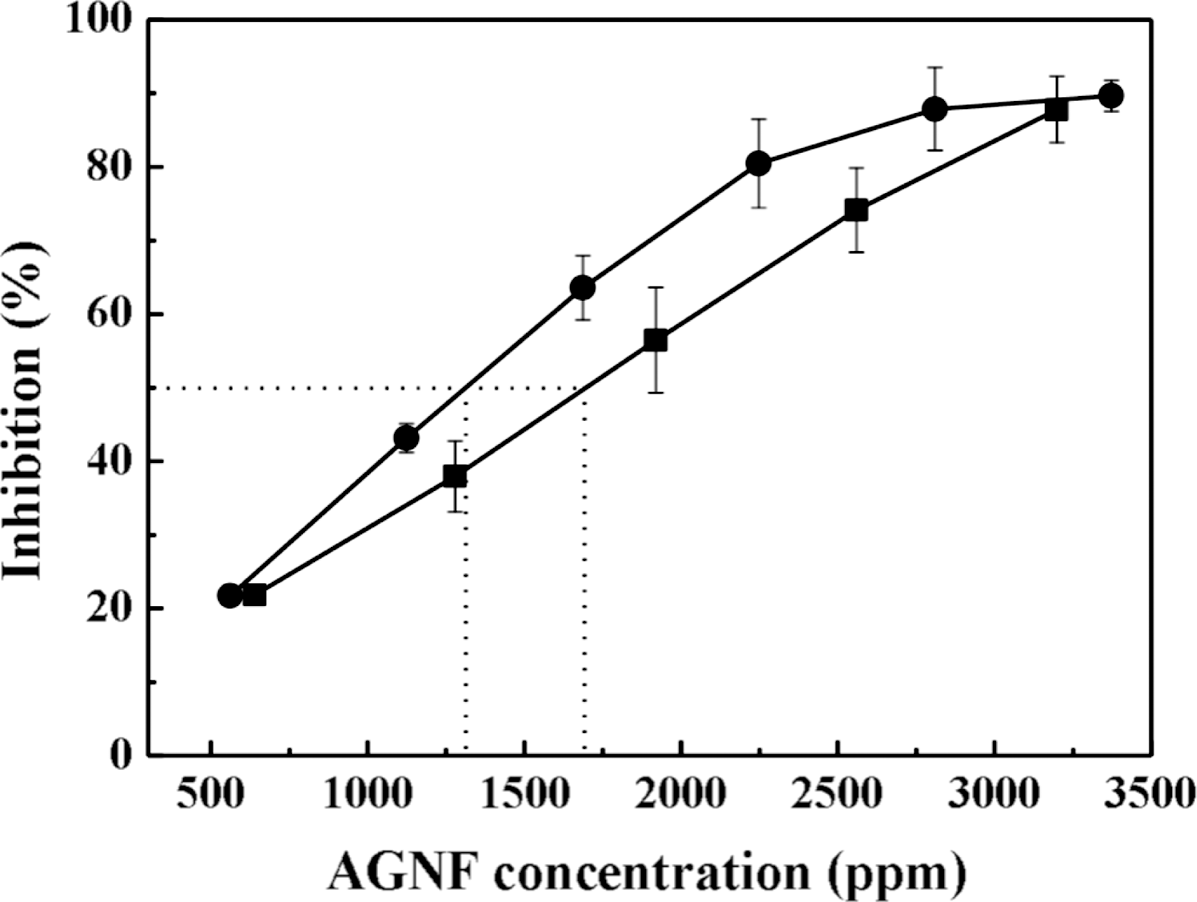
Fig. 7은 참당귀 꽃 추출물의 농도에 따른 추출물 자체 와 하이브리드의 DPPH 항산화 활성을 보여주는 그래프이 다. 꽃 추출물(Fig. 7 ■)은 농도가 증가함에 따라 항산화 활성이 증가함을 보여주고 있으며, 3,000 ppm 이상의 농도 에서 약 90% 정도의 항산화 활성으로 포화됨을 알 수 있 다. 하이브리드(Fig. 7 ●) 역시 추출물 성분의 농도가 증 가함에 따라 항산화 활성이 증가하고, 3,000 ppm 이상의 농도에서 항산화 활성이 90%로 포화되고 있으나, 꽃 추출 물 자체에 비하여 전반적으로 동일 추출물 성분일 경우 약 5-10% 정도 높은 항산화 활성을 나타내는 것으로 관찰되 었다. 항산화 활성이 50%가 되는 농도지점인 IC50의 경우 꽃 추출물 자체는 약 1,700 ppm이었으나, 하이브리드는 약 1,300 ppm으로 1.3배 가량 낮은 농도에서 항산화 활성을 보였다. 하이브리드의 경우 꽃 추출물 용액과 달리 나노공 간 내부에 존재하는 유효 성분들이 항산화 반응에 참여할 수 없음을 감안할 때, 하이브리드에서의 높은 항산화 활성 은 꽃 추출물 중 폴리페놀/플라보노이드 성분이 효율적으 로 담지 되었기 때문으로 예상된다.
Fig. 7.
Antioxidant activities of AGNF itself (squares) and LDH-AGNF hybrid (circles) with respect to concentration of AGNF components.
Download Original Figure
요 약
본 연구에서는 항산화 효과 및 다양한 질환에 대한 치료 효과를 가지고 있는 것으로 알려져 있는 천연 추출물 중 참당귀의 꽃 추출물에 금속이중층수산화물을 적용하여 나 노분말화를 수행하였다. 다양한 추출물/금속산화물의 비율 에 따라 확보된 하이브리드는 건조상 추출물과 달리 높은 친수성과 수분산성을 가지고 서스펜션 형태로 존재하였다. X-선 회절 분석법과 주사전자현미경 연구를 통하여 하이브 리드는 금속이중층수산화물 나노입자의 무질서한 배열을 통해 카드탑 구조를 형성하고, 구조 내 나노공간에 추출물 을 담지할 수 있는 것으로 판단되었다. 반응 시 사용한 추 출물의 비율이 증가할수록 하이브리드 내 추출물 함량은 증가하지만, 반응에 참여하는 추출물의 양은 줄어드는 양 상을 보였으며, 하이브리드화에 의하여 폴리페놀/플라보노 이드가 탄수화물에 비하여 더 효율적으로 담지될 수 있음 을 확인하였다. 또한 꽃 추출물과 하이브리드의 항산화 활 성 평가를 통해 하이브리드가 추출물과 비교 시 높은 항산 화 효율을 가지는 것으로 판단되었으며, 이는 하이브리드 내 존재하는 폴리페놀/플라보노이드의 함량이 추출물 대비 높기 때문으로 보여진다. 나노분말화 참당귀 꽃 추출물 하 이브리드는 분말 특성과 친수성 및 높은 수분산성으로 인 하여 취급이 용이해지고 다양한 산업에 응용될 수 있을 것 으로 예상된다.
감사의 글
본 논문은 농촌진흥청 연구사업(주관과제명: 수출입 대응 신선편이 농산물의 유통기한 설정 및 선도유지 기술 연구, 과제번호: PJ010502)의 지원에 의해 이루어진 것임.
REFERENCES
Albalasmeh AA, Berhe AA, Ghezzehei TA. A new method for rapid determination of carbohydrate and total carbon concentrations using UV spectrophotometry. Carbohyd. Polym. 2013; 97 p. 253-261.

Aloisi GG, Costantino U, Elisei F, Latterini L, Natali C, Nocchetti M. Preparation and photo-physical characterisation of nanocomposites obtained by intercalation and co-intercalation of organic chromophores into hydrotalcite-like compounds. J. Mater. Chem. 2002; 12 p. 3316-3323.

Ansari SH, Islam F, Sameem M. Influence of nanotechnology on herbal drugs: A review. J. Adv. Pharm. Tech. Res. 2012; 3 p. 142-146.

Cavani F, Trifirò F, Vaccari A. Hydrotalcite-type anionic clays: Preparation, properties and applications. Catal. Today. 1991; 11 p. 173-301.

Chen Y, Chen H, Ma M, Chen F, Guo L, Zhang L, Shi J. Double mesoporous silica shelled spherical/ellipsoidal nanostructures: Synthesis and hydrophilic/hydrophobic anticancer drug delivery. J. Mater. Chem. 2011; 21 p. 5290-5298.

Choy JH, Kwak SY, Park JS, Jeong YJ. Cellular uptake behavior of ((gamma)-32P) labeled ATP-LDH nanohybrids. J. Mater. Chem. 2001; 11 p. 1671-1674.

Choy JH, Jung JS, Oh JM, Park M, Jeong J, Kang YK, Han OJ. Layered double hydroxide as an efficient drug reservoir for folate derivatives. Biomaterials. 2004; 25 p. 3059-3064.

Choy JH, Choi SJ, Oh JM, Park T. Clay minerals and layered double hydroxides for novel biological applications. Appl. Clay Sci. 2007; 36 p. 122-132.

Choi HY, Kim GH. Inhibitory Effects of Allium senescens L. Methanol extracts on reactive oxygen species production and lipid accumulation during differentiation in 3T3-L1 cells. Korean J. Food Sci. Technol. 2014; 46 p. 498-504.

Choi SJ, Oh JM, Choy JH. Biocompatible nanoparticles intercalated with anticancer drug for target delivery: Pharmacokinetic and biodistribution study. J. Nanosci. Nanotechno. 2010; 10 p. 2913-2916.

Cullity BD. Elements of X-Ray Diffraction. 2011BiblioBazaarCharleston. USA.

Das J, Das S, Samadder A, Bhadra K, Khuda-Bukhsh AR. Poly (lactide-co-glycolide) encapsulated extract of Phytolacca decandra demonstrates better intervention against induced lung adenocarcinoma in mice and on A549 cells. Eur. J. Pharm. Sci. 2012; 47 p. 313-324.

Deladino L, Anbinder PS, Navarro AS, Martino MN. Encapsulation of natural antioxidants extracted from Ilex paraguariensis. Carbohyd. Polym. 2008; 71 p. 126-134.

Deng H, Zhong Y, Du M, Liu Q, Fan Z, Dai F, Zhang X. Theranostic self-assembly structure of gold nanoparticles for NIR photothermal therapy and X-Ray computed tomography imaging. Theranostics. 2014; 4 p. 904-918.

Duan X, Evans DG. Layered Double Hydroxides. 2006SpringerHeidelberg. Berlin.

Georgetti SR, Casagrande R, Souza CRF, Oliveira WP, Fonseca MJV. Spray drying of the soybean extract: Effects on chemical properties and antioxidant activity. LWT-Food Sci. Technol. 2008; 41 p. 1521-1527.

Goswamee RL, Sengupta P, Bhattacharyya KG, Dutta DK. Adsorption of Cr(VI) in layered double hydroxides. Appl. Clay Sci. 1998; 13 p. 21-34.

Gunjakar JL, Kim TW, Kim HN, Kim IY, Hwang SJ. Mesoporous layer-by-layer ordered nanohybrids of layered double hydroxide and layered metal oxide: Highly active visible light photocatalysts with improved chemical stability. J. Am. Chem. Soc. 2011; 133 p. 14998-15007.

Guo C, Yang C, Li Q, Tan Q, Xi Y, Liu W, Zhai G. Development of a Quercetin-loaded nanostructured lipid carrier formulation for topical delivery. Int. J. Pharm. 2012; 430 p. 292-298.

Hongal S, Torwane NA, Goel P, Chandrashekar B. The effect of 30% ethanolic extract of Indian propolis on replica of human dentin compared against commercially available desensitizing agent: A methodological SEM study in vitro. Pharmacogn. Res. 2014; 6 p. 113-119.

Kang D, Yu X, Tong S, Ge M, Zuo J, Cao C, Song W. Performance and mechanism of Mg/Fe layered double hydroxides for fluoride and arsenate removal from aqueous solution. Chem. Eng. J. 2013; 228 p. 731-740.

Kang H, Kim HJ, Yang JH, Kim TH, Choi G, Paek SM, Choi AJ, Choy JH, Oh JM. Intracrystalline structure and release pattern of ferulic acid intercalated into layered double hydroxide through various synthesis routes. Appl. Clay Sci. 2015; 112-113 p. 32-39.

Kim DO, Lee KW, Lee HJ, Lee CY. Vitamin C equivalent antioxidant capacity (VCEAC) of phenolic phytochemicals. J. Agric. Food Chem. 2002; 50 p. 3713-3717.

Kim TH, Kim HJ, Choi AJ, Choi HJ, Oh JM. Hybridization between natural extract of Angelica gigas Nakai and inorganic nanomaterial of layered double hydroxide via reconstruction reaction. J. Nanosci. Nanotechno. 2015; 15


Kim TH, Lee GJ, Kang JH, Kim HJ, Kim TI, Oh JM. Anticancer drug-incorporated layered double hydroxide nanohybrids and their enhanced anticancer therapeutic efficacy in combination cancer treatment. BioMed Research International. 2014; 2014-11.

Kirby W, Wheeler RE. The extraction of beer polyphenols and their assay by HPLC. J. Inst. Brew. 1980; 86 p. 15-17.

Kosaraju SL, D'Ath L, Lawrence A. Preparation and characterization of chitosan microspheres for antioxidant delivery. Carbohyd. Polym. 2006; 64 p. 163-167.

Kuo YM, Kuthati Y, Kankala RK, Wei PR, Weng CF, Liu CL, Sung PJ, Mou CY, Lee CH. Layered double hydroxide nanoparticles to enhance organ-specific targeting and the antiproliferative effect of cisplatin. J. Mat. Chem. B. 2015; 3 p. 3447-3458.

Lee JH, Sahu A, Jang C, Tae G. The effect of ligand density on in vivo tumor targeting of nanographene oxide. J. Control. Release. 2015; 209 p. 219-228.

Lim SY, Rhee SH, Park KY. Inhibitory effect of methanol extract of Doenjang on growth and DNA synthesis of human cancer cells. J. Korean. Soc. Food. Sci. Nutr. 2004; 33 p. 936-940.

Markham KR, Mabry TJ. Ultraviolet-Visible and Proton Magnetic Resonance Spectroscopy of Flavonoids. 1975SpringerNew York. USA.

Oh JM, Choi SJ, Lee GE, Han SH, Choy JH. Inorganic drug-delivery nanovehicle conjugated with cancer-cell-specific ligand. Adv. Funct. Mater. 2009; 19 p. 1617-1624.

Oh JM, Hwang SH, Choy JH. The effect of synthetic conditions on tailoring the size of hydrotalcite particles. Solid State Ionics. 2002; 151 p. 285-291.

Oh JM, Park M, Kim ST, Jung JY, Kang Y, Choy JH. Efficient delivery of anticancer drug MTX through MTX-LDH nanohybrid system. J. Phys. Chem. Solids. 2006; 67 p. 1024-1027.

Oh JM, Park DH, Choi SJ, Choy JH. LDH nanocontainers as bio-reservoirs and drug delivery carriers. Recent Pat. Nanotechnology. 2012; 6 p. 200-217.

Pan D, Zhang H, Zhang T, Duan X. A novel organic–inorganic microhybrids containing anticancer agent doxifluridine and layered double hydroxides: Structure and controlled release properties. Chem. Eng. Sci. 2010; 65 p. 3762-3771.

Park YH, Lim SH, Kim HY, Park MH, Lee KJ, Kim KH, Kim YG, Ahn YS. Biological activities of extracts from flowers of Angelica gigas Nakai. J. Korean. Soc. Food. Sci. Nutr. 2011; 40 p. 1079-1085.

Pérez-Ramírez J, Abelló S, Van der Pers NM. Memory effect of activated Mg–Al hydrotalcite: In situ XRD studies during decomposition and gas-phase reconstruction. Chem-Eur. J. 2007; 13 p. 870-878.

Rey F, Fornes V, Rojo JM. Thermal decomposition of hydrotalcites. An infrared and nuclear magnetic resonance spectroscopic study. J. Chem. Soc. Faraday Trans. 1992; 88 p. 2233-2238.

Rives V. Layered Double Hydroxides: Present and Future. 2011Nova Science PublishersNew York, NY, USA.

Servat-Medina L, González-Gómez A, Reyes-Ortega F, Sousa IMO, Cássia Almeida Queiroz N, Zago PMW, Jorge MP, Monteiro KM, Carvalho JE, Román JS, Foglio MA. Chitosan–tripolyphosphate nanoparticles as Arrabidaea chica standardized extract carrier: synthesis, characterization, biocompatibility, and antiulcerogenic activity. Int. J. Nanomed. 2015; 10 p. 3897-3909.

Sohn HY, Kwon CS, Son KH, Kwon GS, Kwon YS, Ryu HY, Kim EJ. Antithrombosis and antioxidant activity of methanol extract from different brands of rice. J. Korean. Soc. Food. Sci. Nutr. 2005; 34 p. 593-598.

Taylor KML, Kim JS, Rieter WJ, An H, Lin W, Lin W. Mesoporous silica nanospheres as highly efficient MRI contrast agents. J. Am. Chem. Soc. 2008; 130 p. 2154-2155.

Xu H, Yang D, Cai C, Gou J, Zhang Y, Wang L, Zhong H, Tang X. Dual-responsive mPEG-PLGA-PGlu hybrid-core nanoparticles with a high drug loading to reverse the multidrug resistance of breast cancer: An in vitro and in vivo evaluation. Acta Biomater. 2015; 16 p. 156-168.

Xu ZP, Niebert M, Porazik K, Walker TL, Cooper HM, Middelberg APJ, Gray PP, Bartlett PF, Lu GQ. Subcellular compartment targeting of layered double hydroxide nanoparticles. J. Control. Release. 2008; 130 p. 86-94.

Yang JH, Lee SY, Han YS, Park KC, Choy JH. Efficient transdermal penetration and improved stability of L-ascorbic acid encapsulated in an inorganic nanocapsule. Bull. Korean Chem. Soc. 2003; 24 p. 499-503.

Zhang L, Xia J, Zhao Q, Liu L, Zhang Z. Functional graphene oxide as a nanocarrier for controlled loading and targeted delivery of mixed anticancer drugs. Small. 2010; 6 p. 537-544.