서 론
황색포도상구균(Staphylococcus aureus)은 독소형 식중독 균으로서 우리나라뿐만 아니라 전 세계적으로 문제시되는 주요 식중독 원인균 중 하나이다(Bae et al., 2007).
황색포도상구균 관련 식중독은 해당균이 세포 밖으로 분 비하는 장독소(Enterotoxin, Exotoxin)에 의해 발병하며, 독 소의 발현과정은 원인균으로부터 오염, 오염된 식품에서의 원인균의 증식 및 장독소 생산의 3단계를 거치게 된다 (Cho et al., 2011). 장독소는 16가지(A, B, C1, C2, C3, D, E, G, H, I, J, K, L, M, N, O)가 확인된 상태이며 이 중 Staphylococcal enterotoxin A (SEA), Staphylococcal enterotoxin B (SEB), Staphylococcal enterotoxin D (SED) 형에 의한 식중독 발생 사례가 많은 것으로 보고되고 있다.
SEB는 분자량이 가장 작으나 내열성이 가장 강하고, 식품 중 생성되는 독소량이 SEA와 비슷한 수준이어서 SEB만으 로도 식중독을 일으킬 수 있는 물질로 보고되었다(Lee et al., 1988a). 또한 SEB는 흡입 중독으로 단시간 내에(24시 간) 다수의 환자를 만든다는 특징이 있다(BWC, 2014). 식 중독을 일으키기 위한 장독소의 양은 약 1 μg이며, 이러한 정도의 장독소를 생성하기 위해서는 황색포도상구균이 105-106 cells/g 수준으로 성장해야 한다(Jung et al., 2005). 발병은 오염된 식품 섭취 후 2-6시간 이내에 일어나며, 8- 24시간 이내에 증세가 완화된다(FDA, 2011; MFDS, 2010). 주요 증세는 메스꺼움(nausea), 구토(vomiting), 구역질 (retching), 경련성 복통(abdominal cramps), 탈진(prostration) 등이다(WHO, 2008). 생성된 독소는 냉장, 냉동, 상온, 열, 낮은 수분활성도(건조) 등 대부분의 유통조건에서 안정하 며 방사선에 의해서도 잘 파괴되지 않기 때문에 독소 발현 제어에 각별한 주의가 요구된다(Cho et al., 2011).
미국 질병관리본부(CDC)에 의하면 황색포도상구균 식중 독의 발생건수 당 환자 수가 평균 21명에 달한 것으로 나 타났다(CDC, 2011; CDC, 2012). 최근 5년간 우리나라 식 중독 발생 통계에서도 황색포도상구균에 의한 식중독 발생 건수는 연간 평균 10건으로 지속적으로 발생하고 있으며, 발생건수 당 환자 수는 연평균 약 29명으로 전체 식중독 발생 건수 당 평균 환자수인 25명보다 높아 황색포도상구 균 식중독 발생 시 피해가 매우 큰 것임을 알 수 있다 (MFDS, 2014).
이러한 황색포도상구균에 대한 규제 현황은 식품공전 ‘제 5. 식품별 기준 및 규격’에서 규격이 정하여지지 않은 식품 은 ‘음성’이어야 하며, 황색포도상구균 독소에 대한 국내 규제 현황은 식품공전에서 상품화된 키트를 사용할 수 있 다고 명시되어 있을 뿐 정량적 수치는 정해져 있지 않다 (MFDS, 2014). 식품공전의 황색포도상구균 독소 시험법은 확인시험 등 과정이 복잡하고 장시간이 소요되며 대략적 인 균의 농도로 독소량을 추정해 내는 방법이기 때문에 식 중독 발생 시 원인규명에 적용할 수 있는 시험법으로 최적 화되어 있지 않다는 문제점을 가지고 있다. 현재까지 개발 된 독소검출 키트는 ELISA, gel-diffusion method, reversed passive latex agglutination (RPLA) 등이 개발되었으나, 수입 제품이고 수입 절차가 까다로워 신속한 사용에 제약 이 있다. 따라서 국내에서도 황색포도상구균 장독소를 신 속하게 검출할 수 있는 진단키트의 개발 필요성이 제기되 고 있다.
황색포도상구균 장독소의 신속 검출법을 개발하기 위해 서는 표준 독소가 반드시필요하지만, 현재 생물무기금지협 약(biological weapons convention, BWC)에서 규제 대상 물질로 분류되어 수입이 매우 까다롭다(BWC, 2014). 따라 서 신속검출 키트 개발에 필요한 표준 독소를 확보하기 위 해서는 황색포도상구균 생성물로부터 표준 독소를 분리 정 제하는 기술 개발이 선행되어야만 한다.
국내에서는 1950년대 말부터 침전과 이온교환수지, 겔 여과 등을 이용한 황색포도상구균 장독소 정제에 관한 연 구가 보고되고 있으나 장시간의 정제과정으로 인한 독소의 약화와 단백질 변성이 초래되어 정제도가 좋지 못하여 향 후 빠르고 순수한 독소 정제에 대한 연구의 필요성이 제기 된 바 있다(Lee, 1988b).
본 연구는 황색포도상구균 장독소 중 특히 내열성이 강 하고 흡인 중독 위험이 높은 SEB를 대상으로 독소 분리 및 정제방법을 확립함으로써 향후 기타 장독소 분리에 활 용할 수 있으며 더 나아가 독소의 신속 진단기술 개발 및 항체 생산 연구에 효율을 높이고자 수행되었다.
재료 및 방법
SEB 생산을 위한 균주는 한국 미생물보존센터(Korean culture center of microorganisms, KCCM)로부터 분양 받 은 Staphylococcus aureus KCCM 41331 (ATCC 14458)을 사용하였다. 독소 생산을 위해 37℃에서 48시간 이상 배양 하였으며, 증균에 brain heart infusion 배지(BD Diagnotics, Sparks, MD, USA)를 이용하였다.
황색포도상구균 증균배지로부터 분비된 SEB만을 분리하 기 위하여 직경 0.45 μm 필터(Advantec, Tokyo, Japan)를 이용하여 황색포도상구균 등을 제거하였다.
제균한 시료에서 염도를 낮추어 컬럼 결합을 유도하면서 필터에서 걸러지지 않은 고분자 물질 제거 목적으로 Slide-ALyzer gamma irradiated dialysis cassette (Thermo Scientific, Rockford, IL, USA)를 이용하여 탈염(dialysis) 및 완충액 치환(buffer exchange)을 실시하였다. 완충액은 sodium phosphate monobasic (Sigma-Aldrich, St. Louis, MO, USA) 과 sodium phosphate dibasic (Sigma-Aldrich)을 각각 20 mM로 조제한 후 각각의 용액을 혼합하여 20 mM sodium phosphate 완충액(pH 7.5)으로 pH 조정한 후에 10 mM sodium phosphate 완충액(pH 7.5)으로 희석하여 사용하 였다.
본 연구에서는 fast protein liquid chromatography (FPLC) 기법으로 단백질을 신속하게 정제하였다. Liquid chromatography (LC) 분석은 가열과정이 필요 없어 단백질이 안정 화된 온도에서 실험이 가능하고, 시료의 손실이 적어 회수 율이 높으며 소량으로 단시간 내에 분리가 가능하다는 장점 이 있다. FPLC 기법의 종류는 단백질을 크기별로 분리하는 gel filtration (GF), 등전점과 단백질의 이온화 성질을 이용 한 ion exchange chromatography (IEX), 단백질 표면의 소 수성 성질을 이용한 hydrophobic interaction chromatography (HIC), 특이 결합성을 이용한 affinity chromatography (AC), 위의 방법들을 혼합하여 사용하는 mixed mode chromatography (MMC) 등이 있다. 독소를 분리하는데 있 어서 GF를 실시하기 전에 IEX를 거치면 정제율을 90% 이상으로 향상시킬 수 있었기 때문에(Lee et al., 1988b) 본 실험에서는 IEX와 GF를 함께 사용하였다.
Cation exchange chromatography (CIEX)는 IEX의 한 종 류로 (+)전하를 띄는 단백질을 컬럼에 결합시키는 결합용 완충액과 결합된 단백질을 용출시키는 용출용 완충액이 사 용된다. 결합용 완충액은 시료의 염농도와 비슷하도록 저 농도 염을 사용하고, 용출용 완충액은 단백질을 용출시키 기 위해 고농도 염을 사용하여 경쟁적으로 단백질이 용출 될 수 있도록 유도한다. SEB의 등전점(isoelectric point, pI)이 8.55-8.9인 것을 바탕으로 CIEX에서 결합 및 용출용 완충액은 pH 6.7-7.7에서 사용 가능한 phosphate를 선택하 였다(Brehm et al., 1990). 시료는 5 mM sodium phosphate 로 10배 희석하고, 결합 및 용출 완충액은 각각 5 mM, 20 mM sodium phosphate를 사용하였다. 용출용 완충액에는 SEB가 수지로부터 분리될 수 있도록 1 M NaCl을 첨가하 였고, SEB가 분리되는 염 농도를 파악하면 컬럼 크기가 달라져도 SEB 분리가 용이하므로 용출용 완충액으로 전체 완충액의 농도를 구배별 변화를 주어서 SEB가 분리되는 염 농도를 선정하였다.
CIEX에서 얻은 독소 분획물은 GF를 사용하여 크기별로 나누었으며, 분리과정에서는 물을 완충액으로 사용하였다.
CIEX로 (+)전하를 띄는 단백질을 분리해낸 후, GF를 이용하여 단백질을 크기별로 분리하여 분획을 얻었다. 단 시간 내에 적절한 유속과 좋은 분리능을 위해 AKTA prime plus (GE Healthcare, UK)를 사용하였다. CIEX에 서 SEB를 분리해내는 최적 수지 선정을 위해 WorkBeads 40S (Bio-works, Uppsala, Sweden), CM sepharose HP (GE Healthcare, Uppsala, Sweden), Cellufine C-500 (JNC corporation, Tokyo, Japan) 등을 사용하여 분리능을 비교하 였다. 또한, 수지에 SEB가 잘 결합할 수 있도록 완충액의 pH를 pH 6.83과 pH 7.5으로 비교실험 하여 최적의 정제조 건을 수립하였다. GF는 1-100 kDa의 단백질을 크기별로 분리할 수 있는 Sephacryl S-100 (GE Healthcare, Uppsala, Sweden)을 사용하였다.
컬럼으로 분리된 분획물은 Tecra kit (3M, Maplewood, MN, USA)를 사용하여 색변화를 관찰하였으며 키트에 포 함된 표준 독소(Positive control)가 발현한 색 이상의 색변 화가 있어야 독소가 분리된 분획으로 판단하였다. 염 농도 별 독소 분리능과 정제량 확인을 위해 형광분광분석기 (Infinite M1000 PRO, Tecan, Männedorf, Switzerland)를 사용하여 450 nm에서 흡광도를 측정하였다. CIEX에서 (+) 전하를 띄는 단백질을 농도 구배별로 회수하여 Tecra 키트 로 정성실험 한 후 SEB로 간주되는 피크의 분획의 정제도 를 높이기 위하여 GF 분석하여 다시 한 번 정성 분석 하 였다.
결과 및 고찰
시료 준비단계에서 염도를 저하시켜 컬럼 결합율을 높 이기 위해 시료를 10 mM sodium phosphate 완충액(pH 7.5)으로 탈염 및 완충액 치환을 하였다. CIEX로 분리된 SEB포함 용액의 일부 분획으로 독소확인 시험 결과 검 출되는 SEB의 양이 적었고, 이는 투석 및 완충액 치환 과정 중 단백질의 손실을 가져오는 것으로 판단되므로 효율성이 낮은 것으로 판단된다. 그래서 추가적인 투석 방법을 사용하지 않고 제균 후 크로마토그래피를 진행하 였다.
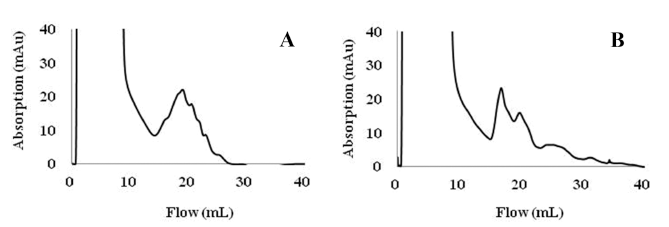
CIEX는 SEB와 완충액의 전하, 그 반대의 전하를 띄는 컬럼의 전하 사이의 가역적인 상호반응을 기반으로 (+)전 하를 띄는 단백질을 분리한다. 완충액의 pH는 pH 6.83으 로 조정하고, (+)전하를 띄는 단백질을 잡을 수 있는 WorkBeads 40S, CM sepharose HP, Cellufine C-500 컬럼 을 이용하여 SEB를 분리하였다. 컬럼의 충진재 종류와 버 퍼의 pH에 따른 SEB분리 정도는 Tecra 키트로 조사하였 고, 색변화 결과를 정량적으로 표시하기 위하여 측정한 흡 광도 값을 Table 1에 나타내었다. WorkBeads 40S를 이용 한 크로마토그램에서는 시료주입 19 mL 지점에서 분리된 분획에서 독소 분리가 확인되었으나 CM sepharose HP, Cellufine C-500을 이용한 크로마토그램에서는 분리된 분획 에서 독소가 검출되지 않았다(Fig. 1).
| Resin | CM sepharose HP | Cellufine C-500 | WorkBeads 40S | CM sepharose HP | Cellufine C-500 | WorkBeads 40S | NC1) | PC2) |
|---|---|---|---|---|---|---|---|---|
| Buffer pH | 6.83 | 7.50 | ||||||
| (A450) | 0.1 | 0.2 | 0.9 | 0.1 | 0.3 | 0.8 | 0.1 | 0.4 |
완충액 pH를 7.5로 높여서 분리한 결과 CM sepharose HP와 Cellufine C-500 컬럼에서는 완충액이 pH 6.83일 때 와 같이 SEB가 컬럼에 결합하지 못하고 모두 용출됨을 독 소확인 시험으로 파악할 수 있었으며, WorkBeads 40S 컬 럼에서 독소가 분리됨을 확인하였다(Fig. 1). 하지만 Fig. 2A와 Fig. 2B에서 보듯이 독소를 함유한 용액의 분리 분 획이 pH 7.5에서 보다 명확히 분리되었다. 그 이유는 완충 액 pH와 SEB pI 값의 차이가 좁혀짐으로써 분리가 유도 된 것으로 판단된다.
또한 1M NaCl을 사용하여 15%, 30%, 45%로 염 농도 구배를 변화시키고 분리된 분획의 SEB 포함여부를 분석한 결과 15% 염 농도에서 분리된 분획이 SEB인 것으로 확인 되었다(Fig. 3).

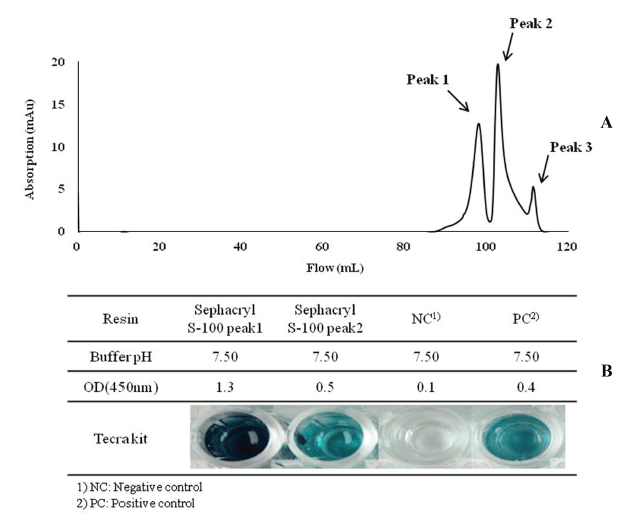
더욱 순수한 SEB를 분리하기 위하여 CIEX에서 분리된 (+)전하를 띄는 단백질을 GF을 사용하여 단백질 크기별로 분리하였다(Fig. 4A). 사용한 시료는 CIEX로 실험한 WorkBeads 40S 컬럼의 15% 염 농도에서의 분획이며, Sephacryl S-100 컬럼을 사용하여 분자량이 26-29 kDa인 SEB를 분리 하였다(Fig. 4B). Kim (1994)에 따르면 투석 을 거친 시료를 Sephacryl S-100 컬럼에 통과시킨 결과 SEB가 분리된 분획을 획득하여 본 실험과 일치한 결과를 보였다. 해당 연구에서는 Sephacryl S-100에서 획득한 분 획으로 SDS-PAGE를 하여 분자량이 다른 여러 단백질로부 터 SEB를 분리해내어 정제율을 높였다.
요 약
황색포도상구균 식중독은 해당 균이 세포 밖으로 분비 하는 장독소에 의해 발병되며, 지금까지 밝혀진 16가지 독소 중 내열성이 가장 강하고 흡입중독으로 쉽게 질환을 일으킬 수 있는 Staphylococcal enterotoxin B형을 분리해 내는 방법에 대해 연구하였다. 분자량 26-29 kDa의 단순 단백질인 SEB를 분리 및 정제하기 위한 방법으로 fast protein liquid chromatography (FPLC)를 이용하였으며, 정제율을 높이기 위해 ion exchange chromatography와 gel filtration chromatography의 두 과정을 거쳤다. 실험 결과 SEB의 분리 조건은 CIEX에서 WorkBeads 40S컬럼 의 분리능이 가장 좋았고, 염 농도 15%에서 SEB가 분리 됨을 확인하였다. CIEX에서 획득한 분획으로 단백질을 크기별로 나누는 GF를 실시하였을 때, Sephacryl S-100 컬럼을 사용하여 정제된 SEB를 획득할 수 있었다. 시료 가 컬럼을 통과할 때 염 농도가 효율적으로 조절될 수 있 도록 하고 SEB를 농축하려 시도한 투석 및 완충액 치환 방법은 전체적인 단백질량 손실을 가져오는 것으로 나타 났다. 본 연구에서 개발된 독소 분리 및 정제 방법은 향 후 다른 장독소 분리에도 활용할 수 있으며, 식중독 신속 진단법 개발 및 항체 생산 발전에 효율을 높일 수 있을 것으로 기대된다.
