서 론
알로에는 전 세계적인 대표적 건강기능식품, 제약 및 화 장품 소재임에도 불구하고 아직도 알로에 겔의 기능성분(또 는 지표성분)에 대한 분석법은 통일 또는 표준화되어 있지 않다(Lee et al., 2012). 특히, 알로에 생잎의 겔은 매우 낮 은 유효성분(주로 아세틸화된 다당) 함량을 가지며, 저장환 경조건에서 빠르게 실활될 뿐 아니라 재배방법, 수확시기, 수 확 후 취급방법 등에 따른 성분함량 변화가 매우 현저하다 (www.nancykbrown.com, 2003; Ramachandra & Rao, 2008).
따라서 원료 알로에의 유효 다당성분을 측정하는 신속하 고도 효율적인 방법의 개발은 매우 중요하다. 특히, 알로에 는 비교적 단순가공에 의해 제조되므로 원료의 품질수준이 직접적으로 최종 제품의 품질에 미치는 영향이 매우 크기 때문에 알로에의 품질 및 생산관리 측면에서 더욱 중요하다.
알로에의 주요 활성성분인 아세틸화된 다당의 검증을 위 해 최근 1H NMR법이 이용되고 있으나(Diehl & Teichmuller, 1998; Bozzi et al., 2007; Davis & Goux, 2009; Jiao et al., 2010) 고가의 장비 및 전문적 분석기술이 필요하다. 따라서, 현재 국내 및 중국의 경우는 총 다당체 함량의 측정법이 이용되고 있다(KFDA, 2011). 이는 알로에 겔 시료의 투석 단계(3.5 kD, 24시간, 3회 외액교체) 또는 알코올 침전처 리(95%, 12시간)를 거쳐 투석내액 또는 알코올 침전물의 총 다당체 함량을 총 페놀-황산법(Dubois et al., 1956)으로 측정하는 방법이다. 이들 방법은 전처리를 요하며, 그 조건 이 복잡하고, 오랜 시간이 소요된다. 또, 시약, 초자 및 기 구의 요구도가 높을 뿐 아니라 표준용액의 조제나 총 다당 체의 시험조작이 필요하다.
하지만 이들 문제점의 해결을 위한 효율적 품질평가 기 술의 연구개발에 대해서는 전혀 이루어지지 않고 있는 실 정이다.
이러한 관점에서 본 연구에서는 생잎 알로에 겔의 bentonite 현탁액(1%, w/v)의 응집특성을 조사하였고, 이에 근거하여 생잎 알로에의 품질특성을 평가하는 신속 및 간편 법을 개발하고자 하였다.
Bentonite(H2Al2O6Si)는 주로 montmorillonite로 구성(70- 90%)되는 콜로이드성 점토이다(Akther et al., 2008). 물속 에서의 강력한 팽창에 기인하여 비교적 낮은 농도(4-5%)에 서 겔 유사구조를 형성하고 매우 안정한 현탁액을 유지하므 로, 응집연구의 대상 시료로서 널리 사용되어 왔다(Akther et al., 2008; Sarkar et al., 2008; Ali & Singh, 2009). 응집에 의 해 수용액에 현탁된 콜로이드 입자가 응결되므로 응집은 현 탁고체 및 금속이온을 제거하기 위한 공통적이고 효율적인 방법이다(Rattanakawin & Hogg, 2001). 그러므로 고분자의 생물응집제는 물 및 폐수처리에 주로 이용되며, 발효공정에 서 미생물 세포를 수확하기 위한 원심분리 및 여과의 대체 법으로도 활용될 수 있다(Wu & Ye, 2007).
그동안 Lee et al.(1998)의 연구에 의하면, 다당을 함유한 신선한 알로에 점질물(1%, v/v 이하의 농도)도 1% bentonite 및 0.5% kaolin 현탁액에 첨가할 때, 현탁액 입자를 빠르게 (5-30 min) 응집시키는 매우 우수한 응집능을 나타내었다. 또, 응집능은 가열 또는 건조 등에 따라 크게 변하여 알로 에의 신선도의 한 지표가 될 수 있음을 보였다.
하지만 알로에 겔의 정량적 관점에서의 광범위한 응집거 동에 대해서는 검토되지 않았고, 추가 검토의 필요성이 매 우 높다.
본 연구에서는 상기의 관점으로부터 알로에 겔에 의한 bentonite 현탁액의 침강거동을 관찰하고, 침강된 응집물의 형태 및 크기분포 특성, FT-IR 스펙트럼 특성, 열중량 특 성을 규명하였다. 또, 응집율과 침강속도에 미치는 시료 및 각종 시험조건 등을 검토, 확립하여, 이 확립된 조건하에서 서로 다른 알로에 다당수준과 알로에 겔의 응집특성을 비 교, 조사하고, 그 상관관계를 밝혔다. 아울러, 이로부터 아 직까지 보고된 바 없는 알로에 원료 겔의 신속, 간편 및 저비용의 효율적 in situ 품질수준 평가를 위한 신규방법으 로의 사용 가능성을 도출하였다.
재료 및 방법
본 연구에 사용한 알로에는 (주) KJM사의 제주농장에서 재 배한 국내산 알로에 베라(Aloe vera Linne)이며, 회사로부터 직 접 제공받아 4℃의 저온실에 보존하면서 실험에 사용하였다. 또 응집시험에 사용한 clay는 주요 광석이 montmorillonite인 bentonite (Daejung Chemicals & Metals Co. Ltd., Siheung, Korea)로, 제품규격으로 입자크기 200mesh, 팽윤성 10-16배, 수분함량 8-14%의 것을 사용하였다.
Bentonite 현탁액은 실험실시 직전 적정부피의 증류수에 bentonite 분말을 혼합하여 조제하였으며(10 g/L), 즉각 침 전되는 큰 clay 입자를 제거한 현탁액을 사용하였다.
한편, 알로에 겔은 알로에 베라 생잎의 껍질을 제거하고 내부의 겔을 믹서기(EBR 400, Electrolux, Sweden)로 균질 화하여 조제하였다. 균질화된 시료는 원심분리(10000 rpm, 30분)하고 섬유질을 제거하였으며, 상징액을 취하여 겔 시 료로 하였다. 또 서로 다른 다당함량 수준의 시료는 각 원 료 알로에 겔 시료를 증류수로 1/100-1/2배 희석하여 조제 하였다.
각종 알로에 겔 시료의 glucomannan 함량은 Congo-red [sodium 4,4'-diphenyl-2,2'diazo-bis-1-naphthalamino-4-sulfonate] 시약(Sigma C6767, St. Louis, MO, USA)을 이용한 비색법 (Eberendu et al., 2005)에 의해 정량하였다. Glucomannan 함량 은 다음 식에 의해 계산하였다.
a: 시험 용액에서의 농도 측정치(mg/mL)
V: 최종 시험 용액의 부피(mL)
S: 시료 량(g)
응집율의 측정: Bentonite 현탁액에서 알로에 겔의 응집능 은 Wu & Ye(2007)에 의해 보고된 방법에 기초하여 측정하 였다. 일반적으로 10 g/L bentonite 현탁액 6-9.5 mL를 시험 관에 넣고 여기에 4-0.5 mL의 응집제 용액을 넣어 혼합하였 다. 혼합물은 5초 동안 Vortex mixer로 교반한 다음 1, 3, 5, 10 및 30분간 정치시키면서 상징액의 흡광도를 UV-VIS spectrometer(Spectronic Genesis 5®, Rochester, NY, USA)로 550 nm에서 측정하였다. 모든 분석은 3회 측정되었고, 응 집율(%)은 다음 식을 사용하여 구하였다.
Flocculating rate(%) = [(B − A)/B]×100
여기서 A와 B는 각각 550 nm에서의 시료 및 대조구의 OD이다.
침강속도의 측정: 침강시험은 응집에 의해 투명한 계면 이 일어났던 모든 실험에서 이 계면의 높이를 시간의 함수 로서 측정하였고, 최종적으로 30분에 측정하였다. 이 계면 이 시간경과에 따라 직선적으로 급격히 이동되는 속도는 계면높이를 시간으로 나누어 구하였고, 초기 침강속도(cm/ min)로 하였다.
응집물의 크기분포: 각 응집물의 크기는 시료를 1750 rpm 으로 교반하면서 입도분석기(Mastersizer 2000, Malvern Instruments Ltd, Worcestershire, U.K)를 사용하여 입도분포 를 분석하여 산출하였다.
응집물의 형태 관찰: 응집물의 형태관찰은 Image capturing board를 사용하여 PC에 연결한 시스템(Optimas Co., Washington, USA)으로 촬영하여 관찰하였다. 즉, 응집물 시료 1mL를 무작위로 취한 다음 고정화없이 glass tube(4 cm× 3 cm×1.5 cm)에 넣고 CCD 카메라의 화상을 640×640 pixels 및 256 grey level의 해상도로 촬영하였으며, 오차를 최소화 하기 위해 400×400 pixels로 수정하였다.
응집물의 FT-IR(Fourier transform infrared spectroscopy) 분석: FT-IR 분석은 응집물 시료를 동결건조 한 후, 200 mesh 체를 통과시켜 얻은 분말시료 2mg을 이용하여 KBr disc를 제조하고 4 cm-1의 해상도로 500-4000 cm-1 파장 범위에 서의 투광도를 Bio-Rad Model 12 EXCALIBER(Cambridge, USA) 기기를 사용하여 측정, 분석하였다.
응집물의 TGA(Thermo gravimetric analysis) 분석: TGA 분석은 시료를 동결건조 한 후, 200 mesh 체를 통과시켜 얻은 분말시료 3-8 mg을 백금 팬을 이용하여 N2(100 mL/ min.) purge gas로 하고, 25-600℃의 범위에서 ramp rate 20℃/min의 조건으로 Model SDT Q60(TA Instruments, Delaware, USA)기기를 사용하여 분석하였다.
결과 및 고찰
각종 시료 및 서로 다른 시험 조건하에서 알로에 겔이 1% bentonite 현탁액의 침강거동에 미치는 영향을 조사하 고 침강형태를 종합한 결과는 Fig. 1과 같다.

시료를 첨가하지 않은 대조구(control)인 1% bentonite 현탁액은 시간 경과에 따른 침강없이 균일한 현탁상태를 잘 유지하였다. 그러나 알로에 겔 첨가구(a-d)는 시간경과 에 따라 서로 다른 형태의 침전물을 용기 밑바닥에 축적하 였으며, 시험관의 밑바닥으로부터 꼭대기까지 2-3개의 계 면층을 형성하였다. 이들 침강거동은 Ma & Pierre(1997)가 전해질에 의한 kaolinite 현탁액의 침전거동으로 보고한 바 있는 축적침전, 응집침전 및 혼합침전과 잘 일치하였다 (Fig. 1a, b 및 c). 응집-침전은 (a)에서 보는 바와 같이, 단 일의 침강층을 형성하며 침전물이 투명한 상징액 영역을 갖는 sharp한 계면에 의해 분리되는 침강거동을 보였다. 반 면, 축적-침전은 (b)에서와 같이, 실린더의 밑으로부터 꼭대 기까지 연속적인 현탁상태를 유지하면서 침강하며, 축적된 침강물과 잔존 현탁액의 계면은 불분명한 침강거동을 나타 내었다. 또, 혼합-침전은 (c)에서와 같이, 침전물과 잔존 현 탁액사이에서 sharp한 계면을 가지나 현탁액의 상부 꼭대 기 층에서 일부 투명한 영역이 관찰되는 침강거동이었다. 이외에도 드물게 응집물이 부유되는 응집거동(Fig. 1d)도 관찰되었다.
응집-침전물은 적정 알로에 겔 농도 및 첨가량에서 관찰 되었고, 적정 농도 및 첨가량보다 높거나 낮은 경우 혼합 및 축적-침전거동이 관찰되었다. 반면, 응집물의 부유거동 은 주로 측정온도가 높은 경우에 관찰되었으며, 겔의 첨가 량이 적정량보다 높은 경우에도 관찰되었다.
한편, 이들 침강거동에 의해 침전된 침전물의 특성을 규 명하고자 먼저, 침전물의 형태를 조사하였으며, 그 결과는 Fig. 2와 같다.

Fig. 2는 CCD 카메라로 촬영한 후 영상분석으로 얻은 침전물의 형태로, fractal dimension의 매우 불규칙한 형태 를 보였다. 대체로 응집-침전물은 크기가 큰 응집물을 형 성하였으며, 이 침전물은 실린더를 기울일 때 쉽게 흘렀다. 반면, 축적-침전물은 작은 크기의 응집물을 형성하였고, 축 적된 침전물은 실린더를 기울일 때 쉽게 흐르지 않았으며, 혼합-침전물은 이들의 중간수준이었다.
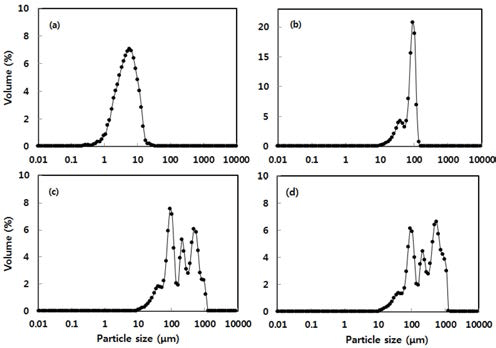
한편, Fig. 3은 이들의 입도크기와 분포의 분석결과이다. Bentonite의 입자크기분포는 1-10 μm에서 단분산 곡선분포 를 보였고, 보고된 값 범위이었다(Sakar et al., 2008). 축적- 침전물은 쌍봉분산곡선분포를 보였으나 입자크기는 10- 100 μm이었다. 반면, 응집침전물은 91.2 μm, 208 μm 및 549.5 μm의 3봉 분산 곡선분포를 보였다. 혼합-침전물도 응 집-침전물과 마찬가지의 3봉 분산 곡선분포를 보였으나 입 자크기는 다소 낮았으며, Fig. 2의 결과와 잘 일치하였다. 따라서 축적 침전에서는 큰 입자들이 주로 침강되는 반면, 응집 또는 혼합 침전물에서는 bentonite 입자와 알로에 겔이 흡착되어 큰 응집물 형태를 나타냄을 알 수 있었다.
또, 이들 침전물의 FT-IR 특성을 bentonite 및 native 알 로에와 비교하면서 조사한 결과는 Fig. 4와 같다.
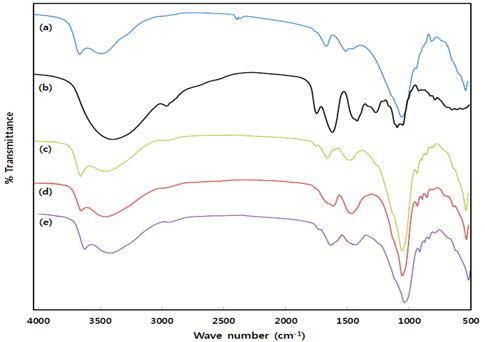
Bentonite의 IR 스펙트럼(Fig. 5a)은 4000-500 cm-1로 주 사되었을 때, 3630, 3456 및 1033 cm-1에서의 전형적인 피크 를 나타내어 보고사실과 잘 일치하였다(Andini et al., 2006; Tunc & Duman, 2008). 이들 피크는 각각 montmorillonite의 신장진동 OH, 고체표면에 흡착된 물 분자의 H-O-H 진동 및 Si-O-Si(silicate moiety)의 굽힘진동을 나타낸다. 또, 1638 cm-1에서의 밴드는 물의 굽힘진동의 배진동(overtone) 을 반영하며, 916 cm-1은 Al-O(OH)-Al의 신장진동이다 (Tunc & Duman, 2008).
반면, Fig. 4b는 알로에 겔의 IR 스펙트럼으로, 수소결합의 O-H 신장진동에 기인한 3366 cm-1 및 관련 굽힘진동의 1080 cm-1, 2933 cm-1에서의 신장진동과 대응하는 굽힘진동의 1402 cm-1 등 C-H기의 기능기가 발견되어 전형적인 알로에 다당의 특성을 나타내었다. 또 carbonyl 관능기 및 아세틸화 시료의 C-O-C 신장이 각각 1726 및 1232 cm-1에서 관찰되어 아세틸화 특성이 잘 관찰되었다(McAnalley, 1993).
축적-침전물의 FT-IR 스펙트럼 특성(Fig. 4c)은 bentonite 특성과 비슷하여 현탁액 중의 큰 입자들이 침강된 것으로 생각되었다. 반면, 혼합-침전물(Fig. 4d) 및 응집-침전물 (Fig. 5e)의 경우는 알로에 겔의 FT-IR 특성도 관찰되어 알 로에 겔-bentonite의 흡착체 형태를 나타내었다.
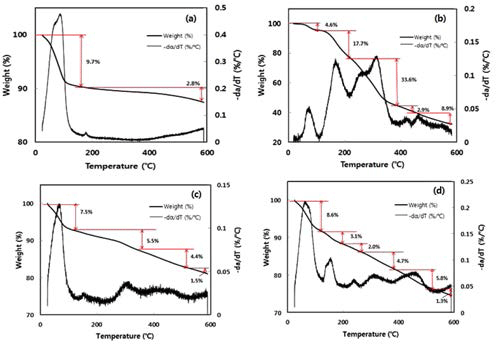
이를 보다 더 명확히 규명하기 위해 열중량 분석을 수행 하였으며, 그 결과는 Fig. 5와 같다.
Bentonite(Fig. 5a)는 두 단계의 무게소실을 나타내었다. 20 및 162.4℃ 사이의 첫번째 무게소실 단계는 bentonite 층간수의 유리에 기인하며, 층간수의 비율은 9.7%이었다. 400℃ 이상에서의 분해는 열에 의한 탈수산화반응에 기인 하는 것으로 보고되었는데, 본 실험에서도 미미하나마 이 러한 분해현상이 관찰되었다(Olalekan et al., 2010).
반면, 알로에 겔(Fig. 5b)은 20-600℃에서 주요 3단계의 무게소실을 보였다. 즉 온도범위 20-109.2℃(DTG peak = 73.8℃), 109.2-214.7℃(DTG peak = 192.7℃) 및 214.7- 396.2℃(DTG peak = 314.1℃)에서 3개의 주요 DTG peak 를 나타내었다. 첫 번째 peak는 수분증발에 기인하며, 가장 큰 세 번째 peak는 보고된 알로에 표준다당의 분해온도 구 간과 비교적 일치하여 알로에의 bioactive 다당인 acemannan 인 것으로 생각되었다. 그러나 두 번째 peak는 정제 다당에 서 관찰되지 않으므로 acemanann 이외의 알로에 성분으로 보인다. 이밖에 400-500℃에서의 minor peak는 Ca-oxalate에 해당하는 것으로 보고되었으며, 이들 결과는 알로에 다당인 Carrysin에 대한 보고와 비교적 잘 일치하였다(McAnalley, 1989).
한편, 축적-침전물(Fig. 5c)의 경우는 bentonite의 TGA 곡선과 유사하여 주로 bentonite의 큰 입자들의 침강에 의 한 것으로 보이는 반면, 응집침전물(Fig. 5d)의 TGA 곡선 은 알로에 다당의 것과 유사하여 bentonite-알로에 겔 흡착 체로 볼 수 있었다. 혼합-침전물은 자료로 나타내지는 않 았으나 대체로 이들 두 침전물 사이의 중간적 특성을 보였 으며, FT-IR 스펙트럼의 결과와도 잘 일치하였다.
이상에서 살펴본 바와 같이, 특정 시료 및 시험 조건에 서 알로에 겔 첨가에 따른 bentonite 현탁액의 응집현상이 관찰되었으므로 이의 응집현상을 더 정량적으로 관찰할 필 요가 있었다.
이를 위해 먼저, 시험관 시험에 의한 현탁액의 응집특 성(응집율과 초기 침강속도)을 조사하였다. 이 때, 시험관 의 벽면에서는 벽면효과(wall effect)가 작용하므로, 시험관의 적정 dimension을 결정하기 위해 시험관의 L/D(높이/내경) 비가 응집율과 초기 침강속도에 미치는 영향을 조사하였으 며, 그 결과는 Fig. 6과 같다.
초기 침강속도(Fig. 6a)는 응집제가 얼마나 빨리 현탁액 으로부터 콜로이드 입자를 제거할 수 있는지를 나타내는 지표값으로, L/D 비 값이 높은 경우(L/D=13)는 벽면효과 에 의해 침강속도가 매우 낮았다(0.57 cm/min). L/D 비 값 이 매우 낮은 경우(L/D=1.5)에서도 침강속도는 낮은 편이 었으며(0.88 cm/min), L/D 비가 2.7 및 5.0에서 서로 비슷 한 가장 높은 초기 침강속도(1.26-1.33 cm/min)를 보였다. 응집율도 초기 침강속도와 마찬가지의 경향을 보여 L/D 비=13일 때 응집율은 약 65%이었으나 L/D 비=5.0일 때는 약 91%로 가장 높아서 L/D 비=13에서보다 1.4배나 더 높았다. 이들 결과는 대체로 응집물의 침강속도가 높을수 록 응집제의 응집성능이 더 좋은 것으로 알려진 사실과 잘 일치하였다(Ali & Singh, 2009).
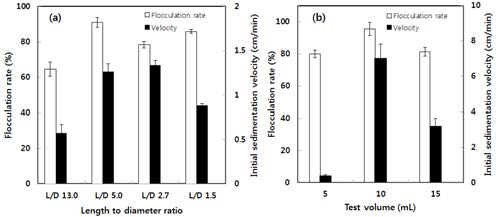
또, 이 조건하에서 총 시험용량(5-15 mL)이 응집율 및 초기 침강속도에 미치는 영향을 조사한 결과(Fig. 6b)에서 는 10 mL의 총 용량이 가장 높은 응집율과 침강속도를 나 타내었다.
따라서 이하에서는 최대의 침강속도와 응집율을 나타낸 L/D 비=5.0의 시험관을 사용하였고, 총 시험용량은 10 mL 로 하여 실험을 실시하였다.
상기에서 결정한 L/D 비=1.5의 시험관 및 총 시험액량 10 mL를 사용하여 알로에 겔의 첨가량(0.5-4 mL)이 1% bentonite 현탁액의 응집율 및 초기 침강속도에 미치는 영 향을 조사하였으며, 그 결과는 Fig. 7과 같다.
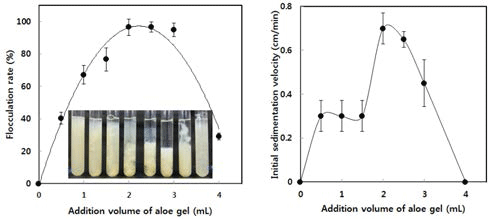
Fig. 7a의 inset에서 보는 바와 같이, 시료를 첨가하지 않 은 대조구는 균일한 현탁상태를 유지하였으나 시료의 첨가 구는 첨가량의 증가에 따라 침전물과 상징액의 두 층으로 분리되었으며, 이 때 상징액의 투명도는 서로 다름을 관찰 할 수 있었다. 이에 기초하여 각 시료의 응집율을 측정한 결과, 알로에 겔의 첨가량을 증가시켰을 때 응집율은 서서 히 증가하여 2 mL 첨가시에 최대값을 보였고, 이 보다 더 첨가하게 되면 다시 급격하게 저하하였다. 초기 침강속도 (Fig. 7b)도 응집율과 마찬가지로 총 10 mL의 시험용액 중 의 알로에 겔 첨가량이 증가할수록 현저하게 증가하였으나 첨가량이 너무 높으면 다시 급격히 감소하였다. 따라서 최 적의 첨가량이 존재하였으며, bentonite 현탁액: 알로에 첨 가량의 비가 8:2(v/v), 즉 총 시험용량 10 mL 중에 2 mL의 알로에 겔을 첨가할 때, 최대의 응집율과 침강속도를 나타 내었다.
한편, 알로에 겔의 농도 효과를 보기 위해 생잎 알로에 겔을 희석하고 서로 다른 희석율(1-1/5)의 알로에 겔이 응 집율 및 초기 침강속도에 미치는 영향을 조사한 결과는 Fig. 8과 같다. 이 때 첨가량은 2 mL로 고정하였다.
Fig. 8a에서 보는 바와 같이, 각 희석 시료의 침전물과 상부의 투명액을 구분짓는 계면높이는 희석율에 따라 현저 한 차이를 보여서 희석율이 너무 높거나 낮은 시료에서는 시간에 따른 계면높이의 변화가 적었으나 3/4 또는 1/2로 희석한 시료에서는 30초 이내에 급격히 증가하였다.
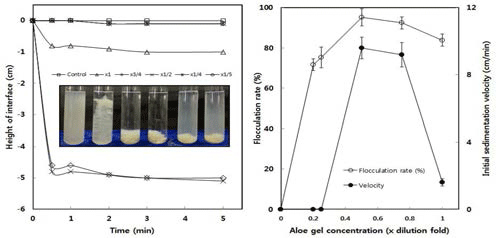
응집율(Fig. 8b)도 알로에 겔의 희석율을 증가시켰을 때 서서히 증가하여 1/2로 희석하였을 때 최대값을 보였고, 이 보다 더 희석하면 응집율이 비교적 크게 저하하였다. 이는 낮은 농도에서는 응집부위가 적기 때문이며, 고농도 에서는 재분산(re-dispersion)이 일어나기 때문이다(Poirier, 2001). 또, Fig. 8a의 시간경과에 따른 계면높이 변화의 초 기 직선의 기울기로부터 구한 초기 침강속도(Fig. 8b)도 응 집율과 거의 비슷한 경향을 보였으나 겔 농도에 더욱 민감 하여 1/2-3/4 희석액에서 최대값 범위이었으며, 이의 전후 에서는 급격히 저하되었다. 그러나 침전된 침전물의 부피 는 희석율의 증가에 따라 감소하는 경향을 보여 농도 의존 성을 나타내었다. 따라서 알로에 겔의 응집특성은 특정 희 석농도에서 최대의 응집율과 침강속도를 나타나는 특징을 보임을 알 수 있었다.
알로에 겔의 최대 응집율과 침강속도는 특정 희석농도에 서 나타났으므로 이번에는 시료간의 차이를 알아보았다. 즉, 서로 다른 시기에 수확한 5종의 원료 생잎 겔들에 대 해 응집시험 5분 후의 응집율을 비교하였으며, 그 결과는 Fig. 9와 같다.
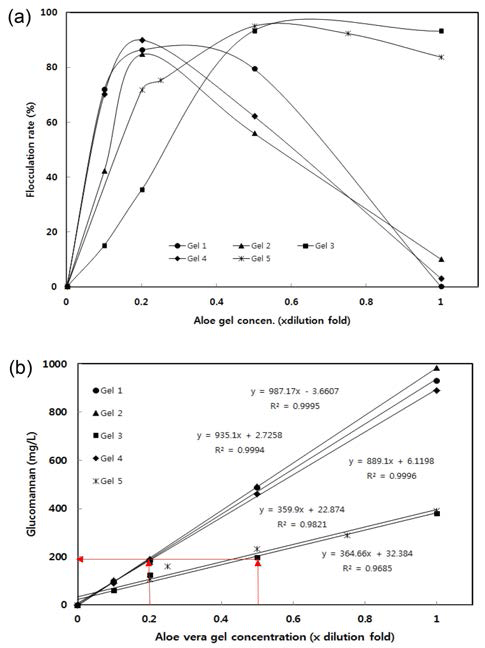
5종 시료의 응집율은 크게 두 그룹으로 나뉘었다(Fig. 9a). 즉, 알로에 겔의 어떤 희석율에서 최대값을 갖거나 (Gel 1,2,4), 낮은 희석율에서는 서로 비슷한 높은 응집율을 유지하지만 어떤 희석율 이상에서 응집율이 급격히 저하하 는(Gel 3,5) 두 가지 경우로 구분되었다. 전자의 경우는 최 대 응집율(84.8-90%)을 나타내는 희석율이 1/5이었고, 후자 의 경우는 최대 응집율(93.4-95.1%)을 유지하는 희석율이 1/2이었다.
일반적으로 고분자 응집제는 전하중화, 정전기적 patch, 가교(bridge) 혹은 고갈응집(depletion flocculation, 입자간의 약한 응집)을 통해서 콜로이드 입자를 탈안정화시키는데. 비이온성 고분자에 의한 응집은 주로 가교기작에 의한다 (Yan et al., 2004; Tripathy & De, 2006).
고분자 응집제에 의한 가교기작의 경우, 첨가농도에 따 른 응집율의 관계는 underdose 영역, optimal dose 영역 및 overdose 영역의 세 영역으로 관찰된다. Overdose 영역은 고분자에 의한 현탁액의 재분산(re-dispersion)에 기인하는 것으로 잘 알려져 있다(Poirier, 2001). 즉, 고분자 응집제가 현탁입자에 대해 흡착에 기초한 접착 및 가교에 의해 응집 을 일으키는데, 응집제가 과잉으로 존재하면 현탁입자 표 면에 있는 흡착활성점의 대부분이 응집제 분자에 의해 점 유되어 응집제 본래의 가교작용은 일어나지 않는다. 하지 만 응집제 자체는 주로 고분자 전해질이거나 강한 친수성 이어서 보호콜로이드의 기능을 나타내므로 현탁입자를 둘 러싸게 되고, 결국 이들을 안정화시켜서 현탁입자는 분산 상태로 존재하게 된다. 반면, 응집제가 소량인 경우는 상호 인접한 현탁입자의 흡착활성점을 결합해서 가교하므로 응 집작용이 주로 일어나게 된다(Oomori, 1986).
따라서 본 시료의 응집거동은 이러한 고분자(알로에의 경우 다당류)에 의한 현탁액의 응집-분산 거동에 의한 것 으로 생각되었다. 또, 이에 근거하면 생잎 알로에 겔 시료 의 고분자 함량은 최대의 응집율과 초기 침강속도를 나타 내는 희석율과 밀접한 상관관계를 가짐을 유추할 수 있다.
알로에의 고분자는 다당(특히, glucomannan)이므로 Fig. 9a의 5종 gel 시료 및 이들의 여러 희석율 시료에 대해 glucomannan 함량을 측정하고, 희석율과 다당함량 사이의 관계를 도시한 결과(Fig. 9b), 각 시료 모두 희석율에 따른 glucomannan의 함량은 직선관계를 보였다(R2> 0.969). 그러 나 시료에 따라 그 기울기 값은 달라서 Gel 1, 2 및 4시 료는 높은 기울기값(889.1-987.17)을 가졌으며, 희석하지 않은 원래 시료의 glucomannan 함량이 889.6-983.8 mg/L 로 높았다. 반면, Gel 3 및 5 시료는 낮은 기울기 값 (359.9-364.66)을 나타내었으며, 원 시료의 glucomannan 함 량도 379.5-391.2 mg/L로, Gel 1, 2 및 4 시료보다 약 2.5 배나 낮았다. 특히, 2.5배의 차이는 시료의 최대 응집율을 나타낸 희석율의 비[(1/2)/(1/5)]와 잘 일치하는데, 빠르게 침 강하여 최대 응집율을 나타내는 희석율에서의 glucomannan 함량은 시료에 상관없이 약 195.7±21.4 mg/L로 동일하였다.
이상의 사실들을 종합하면 최대 응집율과 침강속도를 나 타내는 알로에 겔의 희석율은 알로에 다당함량의 수준과 관 계되며 매우 빠르게(3분 이내) 최대의 응집율을 나타내는 희석율이 낮을수록 그 시료의 glucomannan 함량이 높은 것 을 의미한다. 이는 빠르게 응집하여 최대의 응집율을 나타 내는 희석율을 찾음으로써 알로에 겔 시료의 다당 수준을 간편하고 신속하게 예측할 수 있음을 지적하는 사실이다.
이상의 본 시험 절차는 현행 총 다당체 측정법에 비해 전처리 조작이 불필요하며, 특정 시험조작없이 간편하고, 값싼 비용으로 신속하게(3분 이내) 알로에 겔의 다당 수 준을 판단할 수 있다. 따라서 본 방법은 아직 보고된 바 없는 알로에 겔의 신속, 간편 및 저비용의 in situ 품질수 준평가의 신규방법으로 산업현장에서 효율적으로 사용할 수 있을 것으로 판단하였다.
결 론
Clay 현탁액(bentonite, 10 g/L)에 대한 생잎 겔의 응집특 성을 조사한 결과, 어떤 특정조건하의 시료군에서만 빠르 게 응집하여 침강되는 현상이 관찰되었다. 침강거동은 보 고된 응집-침전, 축적-침전 및 이들이 혼합된 혼합-침전의 3종 침강거동과 잘 일치하였다. 특히, 응집-침전거동에서는 침전물과 상등액의 두 층으로 분리되고, 이 때 상등액의 투명도가 서로 다르게 응집되는 현상을 관찰할 수 있었는 데, 이 현상은 응집율과 초기 침강속도에 의해 잘 특성화 되었다.
3분 이내에 빠르게 침강되어 응집물을 형성하였으며, 최 대 응집율을 나타내는 현상은 총 시험 용량이 10 mL이고, 높이/내경 비(L/D)가 5.0인 시험관을 사용하여 알로에 겔과 bentonite 용액비를 2:8(v/v)로 하였을 때, 생잎 알로에 겔의 희석배수에 현저하게 의존함을 확인할 수 있었다. 또, 서로 다른 생잎 알로에 겔의 최대 응집율을 나타내는 겔 농도(희 석배율)와 유효성분인 다당함량 수준의 관계는 기울기가 서 로 다른 양의 상관성(R2> 0.969)을 보였으며, 시료에 상관없 이 빠르게 침강하여 최대의 응집율을 나타내는 희석율에서 의 다당함량은 약 195.7±21.4 mg/L로 동일하였다. 따라서 원료 알로에의 다당 함량수준은 희석배수가 큰 시료일수록 높은 것을 확인할 수 있었으며, 이는 단순히 최대 응집율 (>90%)을 나타내는 겔의 희석배수만을 구함으로써 원료 겔 의 다당함량 수준을 예측할 수 있음을 지적한다.
그러므로 알로에 생잎 겔의 bentonite 현탁액의 응집율 및 침강속도의 측정은 저비용으로 빠르고 간편하며, 또 효율적 으로 알로에의 원료 품질을 평가하는 새로운 측정법으로서 알로에 산업현장에서의 실제적 응용의 가능성을 보였다.